苏沃雷生性质、用途与生产工艺
Suvorexant是由美国制药巨头默沙东公司研发的一种新型催眠药物,与其他催眠药物不同的是,一般催眠药物是按需服用(也就是说只在需要时服用,治标不治本),但默沙东的Suvorexant则是一种治疗性药物,需长时间服用。
该药能够阻断Orexins(神经肽)传递讯息。Orexins(神经肽)通常向人体传递各种保持清醒的讯息,因此是导致人们失眠的罪魁祸首。
杜克大学医学研究中心的Andrew Krystal教授表示,默沙东的这款药物将成为受患者青睐的新药。
默沙东神经学科和眼科部门负责人Darryle Schoepp表示,该药物尤其适用于那些整夜无法睡眠,接受现有药物治疗但疗效甚微的患者。
默沙东表示,有2000多名非其他医学问题造成的失眠症患者参加了Suvorexant的这两次后期试验。该药最常见的副作用是疲倦和头痛。
2014年08月13日,美国FDA批准默沙东研发的Belsomra (Suvorexant)上市,用于治疗入睡及睡眠困难(失眠症)患者。Belsomra是一种食欲素受体拮抗剂,是该类药物中首款获得批准的药物。食欲素是参与调节醒睡周期的化学物质,在保持人觉醒方面起重要的作用。Belsomra可改变食欲素在大脑中的信息行为。
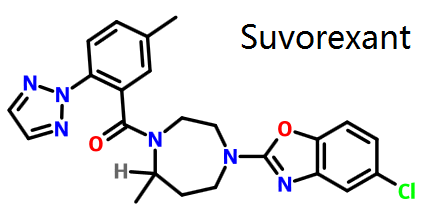
图1为suvorexant结构式。
美国食品药品管理局(FDA)批准了一种新型催治疗失眠症药物suvorexant(Belsomra),该药物属于食欲素受体拮抗剂。
Suvorexant是首个获批的食欲素受体拮抗剂,它通过阻断神经肽食欲素A和B与食欲素受体的结合而抑制神经元对唤醒系统的激活作用。
据suvorexant生产商默克公司称,FDA建议将其列入管控物质,DEA在今年早些时候提议,按照《管控物质法》应纳入IV类管控物质之列。
2012年底默沙东公司向美国食品药品管理局(FDA)提交该药的上市申请。2013年5月,FDA外周与中枢神经系统药品专家委员会对该公司建议的起始剂量的安全性提出质疑。数月后,FDA建议默克公司对大多数患者的起始剂量设定为10mg。
该公司此前没有准备生产该剂量的制剂,因此重新设计生产了几种新规格制剂。
目前,据FDA药品评价与研究中心药品评价I室主任Ellis Unger博士称,“FDA批准了4种规格——5、10、15和20 mg的Belsomra。”Unger博士在声明中指出,“使用最小有效剂量可减少副作用风险,如次日早晨的困倦。”
FDA和默克公司称,每晚仅需在睡前半小时至起床前至少7小时内服用suvorexant 1片,每天不得超过20 mg。
困倦是最常见的副作用。在FDA要求开展的次日驾驶行为研究中,服用20 mg的患者能力受损。FDA称,应警告服用20mg的患者次日勿从事驾驶或任何需要警觉的活动。
该药物还可能导致FDA所称的“睡眠驾驶和其他在没有完全觉醒的状态下的复杂行为”,包括做饭和饮食、打电话或性行为。如果出现上述行为,患者及其家人应告知医生。
Suvorexant发放时配送一份患者用药指南,其中包括了详细的安全性信息。
FDA称,尽管针对该药开展了3项试验研究,但均未与其他已获批催眠药物进行对比研究,因此,尚不清楚该药物的对比有效性。
有关新型催眠药物suvorexant(Belsomra)的适应症,用量,药理作用信息由ChemicalBook的彤彤编辑。
Suvorexant (MK-4305)是一种有效的OX receptor双重拮抗剂,作用于OX1受体和OX2受体, K
i分别为0.55 nM和0.35 nM。Phase 3。
在大鼠体内,Suvorexant具有优异的被动渗透性和口服生物利用度,并有利于睡眠。此外,suvorexant显著并剂量依赖性减少大鼠(10,30,和100毫克/千克),狗(1和3毫克/公斤),和猕猴(10毫克/千克)的运动活性,同时促进其睡眠。
双OX拮抗剂对睡眠的调节目前处于III期临床试验。
苏沃雷生
上下游产品信息
上游原料
下游产品