大豆苷是豆科属植物大豆异黄酮的主要活性成分之一,具有扩张冠状动脉和脑血管,增加心、脑血流量和降低心肌耗氧量,抗动脉粥样硬化和促进血液循环等作用。
【大豆异黄酮】
大豆苷(Daidzin)是大豆黄素(Daidzein)的β-葡萄糖苷,是大豆异黄酮的主要存在形式。大豆异黄酮是大豆中的一种特殊生物活性成分,流行病学调查、动物实验和癌细胞培养实验均证实大豆异黄酮具有众多的生物活性功能,包括抑制乳腺癌、前列腺癌、白血病及一些肝癌、胃癌细胞系的生长和增殖,对抗胆固醇。保护心血管、预防动脉栓塞,预防骨质疏松,提高畜禽生产机能,调节女性经期不适。大豆苷提取来源为豆科植物大豆(Glycine max(L) merr)的种皮黄色的种子。常见的分离及纯化方法有:有机溶剂萃取法、超声波辅助法、酸解法、酶解法、高速逆流色谱法、大孔树脂吸附法等。
【基本信息与理化性质】
中文名称: 大豆苷
英文名称: Daidzin
CAS号: 552-66-9
分子式:C21H20O9
分子量:416.38
熔点:234-236 oC
旋光度:-24 º (C=0.1g/100ml,dimethylsulfoxide)
外观:白色粉末
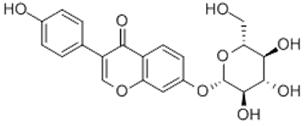
图1为大豆苷化学结构图
【分离及纯化】
大豆苷的分离和纯化包括两个步骤:首先制备大豆异黄酮的粗提物;再进行大豆异黄酮的分离和大豆苷的纯化。
第一步:大豆异黄酮粗提物制备[3]
用来提取大豆异黄酮的实验原料应预先经过脱脂处理,如大豆粉、豆粕等,粒径最好在 0.5~0.8mm,最大不超过 1mm。粒径过大,传质面积太小,不利于加强提取过程的传质;粒径过小,粉末度过高,虽然传质面积很大,但是原料对溶质的吸附作用也会增强,此外还会给后续分离操作带来困难。
最常用的从大豆或大豆相关产品中提取异黄酮的方法微有机溶剂萃取法。溶剂萃取法所采用的溶剂有甲醇、乙醇、甲醇水溶液、乙醇水溶液、丙酮和弱碱性水溶液。溶剂提取物中除含有大豆异黄酮外还含油脂、蛋白质、纤维素、多肽、多糖等杂质。
①甲醇提取法
徐德平等将2.5kg 大豆胚芽放入 10L 的玻璃瓶中,加入甲醇至满,不定期搅拌,浸提 72 小时后将甲醇滤出,回收甲醇。向玻璃瓶中继续补充新甲醇至满,不时搅拌,浸提 72 小时,滤出甲醇,重复 3 次,合并甲醇提取液,旋转蒸发,得到异黄酮粗提物。
②乙醇提取法
在充分考虑溶剂提取后续操作的难易程度、操作成本以及溶剂的毒性等因素,在溶剂提取法中最常用的是乙醇水溶液。从经济性和工艺优化角度考虑,需要经过实验考察乙醇浓度、料液比、温度、时间和提取次数等因素对异黄酮收率的影响,最终来确定最佳工艺条件。乙醇浓度一般为 40~80%,料液比为(8~16):1(体积 ml/重量 g),提取温度 40~90℃,提取时间为 1~10h,提取次数为1~3 次,可以将原料中 90%以上的大豆异黄酮提取出来。
③丙酮提取法
丙酮对异黄酮有良好的溶解选择性,可使乙醇提取物中大部分杂质在不被溶解的情况下而除去,异黄酮则部分或全部溶解于丙酮中,而且实验可以在室温下进行,来提纯异黄酮。王晓玲等采用丙酮加酸的条件下能使粗提物中异黄酮含量提高到 25.6%,因此丙酮可以用于异黄酮的精制过程。
第二步:大豆异黄酮的分离和大豆苷的纯化
江和源等人[4]采用高速逆流色谱法(HSCCC)分离大豆异黄酮中的大豆苷。采用半制备型高速逆流色谱仪进行分离制备。首先将乙酸乙酸、醋酸、水(体积比为5:1:10)置于分液漏斗中,充分振摇后静置分层,待平衡一段时间后,将上相和下相分开,取上相作为固定相,下相作为流动相。称取300mg 大豆异黄酮粗提物溶解于20ml 流动相中,待用。
进样前,先用泵将固定相(上相)以10ml/min的流速注入色谱分离柱,然后将柱的首端与六通进样阀相接,调节主机转速为800r/min,再以1.5ml/min 的流速泵入流动相(下相) ;待整个系统建立动态平衡后,由六通进样阀进样(20ml) ;然后根据紫外检测图谱,接收目标成分,检测波长为254nm。收集到的各部分样品溶液,用旋转蒸发仪蒸干有机相,水相用F T S 冷冻干燥仪干燥。所得样品,用高效液相色谱法检测纯度。
由色谱图可知,选择合适的溶剂系统,高速逆流色谱法分离纯化大豆苷和染料木苷,所得两成分的纯度均很高,大豆苷纯度达到98.2%。
另外,也可通过对大豆苷粗品重结晶的方法进行纯化。郭艳艳等人[5]对得到的大豆苷粗品,选用甲醇-乙酸系统重结晶对粗品进行进一步纯化。当甲醇:乙酸为10:1 时结晶效果最佳,此时的结晶为无色长针状结晶,HPLC测定结晶纯度达86.4 %, 且收率为78.6 %。用其对粗品大批量反复重结晶,得到终产品纯度为96.4 %。
【检测方法】
①高效液相色谱法[4]
色谱柱:Hypersil BDS(250×4.6mm ID:5μm,大连依利特有限公司),流动相:MeOH:HAC:H2O(30:1.5:68.5),流速:0~8.5min时1.0ml/min,8.5~30min时1.5ml/min,柱温:50oC,检测波长:254nm,进样量10μl;样品采用流动相溶解。典型色谱图如下图所示:
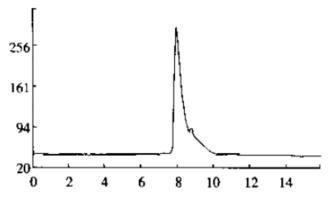
图2为大豆苷高效液相色谱图
②分光光度法[6]
在pH 6.5的Na2HPO4 -NaH2PO4 缓冲溶液中,Fe(Ⅲ)-BPR及Al(Ⅲ)-BPR 与大豆苷形成有色络合物,络合物的最大吸收波长分别为550 nm 和580 nm,摩尔吸收系数分别为5.88×102 和3.71 ×102 m2·mol-1(摩尔吸光系数分别为5.88×103 和3.71 ×103L·mol-1·cm-1)。在pH 10.5 的NH3-NH4Cl缓冲介质,孔雀绿,罗丹明B,结晶紫,甲基紫和乙基罗丹明B均可与大豆苷缔合显色,但灵敏度以后者为最高,摩尔吸收系数达1.74 ×103 m2·mol-1(摩尔吸光系数1.74×104 L·mol-1·cm-1)。
【用途】
大豆苷(daidzin)是豆科属植物大豆异黄酮的主要活性成分之一,具有扩张冠状动脉和脑血管,增加心、脑血流量和降低心肌耗氧量,抗动脉粥样硬化和促进血液循环等作用。[7]
【储存】
2-8oC,干燥、避光、密封储存。
【参考资料】
1 闵嘉霖, 曾爱武, 袁希钢 等. 大豆异黄酮的提取[J]. 粮油加工与食品机械, 2006 (1): 47-50
2 Catherine A, Rice-Evans, Lester Packer. Flavonoids in Health and Disease[M]. York Basel HongKong: Marcel Dekker, 1998
3 左玉帮.从豆粕中提取大豆异黄酮的研究. 天津大学 2008 博士学位论文
4 江和源, 台建祥, 吕飞杰. 高速逆流色谱法分离制备大豆异黄酮中的大豆苷和染料木苷. 食品科学 2004 25(1):85-88
5 郭艳艳, 王俊儒, 薛亚峰. 葛根中大豆苷的分离纯化工艺研究. 西北农业学报 2009 18(1): 252-254
6 卢业玉, 罗宗铭, 黄池宝, 等. 分光光度法测定大豆苷的研究[J]. 广东工业大学学报, 2001 18(3): 81-84
7 吴志生, 章靓, 陈旺,等. 激光光散射与荧光光谱法研究大豆苷与牛血清蛋白作用及聚集态. 化学学报 2009 67(14):1609-1614
8 http://www.chemicalbook.com/ProductChemicalPropertiesCB8447760.htm
9 http://baike.baidu.com/view/2804870.htm