氯仿是良好的有机溶剂,能溶解各种有机物(包括油脂、蜡等),还能溶解有机玻璃、树脂、油漆、橡胶等高分子材料,可用作它们的粘合剂。三氯甲烷也是有机合成的重要原料,是制造二氟氯甲烷(氟利昂-22)和四氟乙烯的原料,还可做青霉素、香精油、生物碱等的萃取剂。
【理化性质】
氯仿是甲烷中3个氢原子被氯原子取代所形成的化合物,又名三氯甲烷,亦称“哥罗仿”。化学式CHCl3。无色、透明、易挥发、不易燃烧、稍有甜味的液体。折光性强。相对分子质量119.38。相对密度1.4984(15℃)。熔点-63.5℃。沸点62℃。难溶于水:0℃时1.062、10℃时0.895、20℃时 0.822、30℃时0.776,能与乙醇、乙醚、石油醚、苯、四氯化碳和二硫化碳等有机溶剂混溶。在光的作用下,能被空气氧化成剧毒的光气(COCl2)。可在氯仿中加入1~2%的乙醇作稳定剂,使生成的光气转化成碳酸二乙酯,从而消除毒性。具有麻醉性,过去常用作麻醉剂,能刺激粘膜并较快从兴奋状态变为困倦、眩晕、麻醉,严重时可致死。因具毒性,现已不用于麻醉,但在制药、塑料、油料添加剂和有机合成等化工业中仍常用作溶剂。是大气与水环境中常见的污染物。1.9μg/L的浓度使癌症危险增加十万分之一。饮用水中不应含有氯仿,但氯化消毒含有机污染物的饮用水时,常能生成色谱法可以检出浓度的氯仿。因此,饮用水用臭氧消毒较用氯化消毒在卫生上更为合理。空气中最高允许浓度为50毫克/千克。
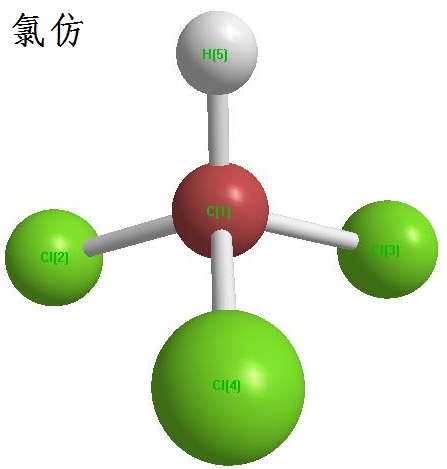
图1为氯仿化学结构式。
【化学反应】
三氯甲烷由于三个氯原子的诱导效应,化学性质活泼。易水解,生成甲酸和氯化氢;在碱催化剂作用下,可发生加成作用,例如氯仿和丙酮在氢氧化钾作用下,于50℃发生加成反应;在碱溶液中,三氯甲烷与伯胺反应,形成胩,胩有特殊气味,用以检查伯胺的存在。三氯甲烷进一步氯化,可生成四氯化碳。
在碱溶液中三氯甲烷与酚反应,生成羟基芳香醛。
在无水三氯化铝的催化作用下,三氯甲烷与苯反应,可生成三苯(基)甲烷。这是制备三苯甲烷染料的一种重要方法。
氯仿在光照条件下可被空气中的氧气氧化成剧毒的光气。密封在棕色瓶中保存。如有部分氧化,可加 1%乙醇以破坏光气(生成无毒的碳酸二乙酯)。
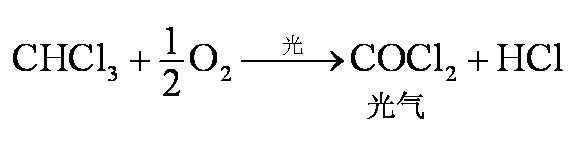
图2为氯仿在光照条件下化成剧毒的光气
在烯烃聚合反应中用作调聚剂。在过氧化物引发下烯烃分子可以成百成千聚合成高聚物,如果加入氯仿,可使烯烃聚合的分子数控制在10以下或50以上,称之为调节聚合反应,使聚合反应能按要求进行。它也是重要的有机合成试剂。在碱的作用下,与烯烃反应生成卤代三员环化合物,为合成三员环状化合物的重要方法。在光照下会氧化成有剧毒的光气,反应式为:2CHCl3+O22COCl2+2HCl。
【产品质量标准】

图3为沪Q/HG11—006—82产品质量标准
【麻醉剂】
氯仿在历史上曾作为麻醉剂用于外科手术。1847年英国医生辛普逊正在寻找更佳的麻醉剂,法国化学家杜马寄给他一种药物,他和二位同事亲自试验,这药物挥发产生一股微甜而有特殊味道的气体,他们吸进以后,都相继睡去。这就是氯仿,由此而发现了它可以作为麻醉剂。危险的实验换来成功的发现,幸好初试用量得当,不曾发生意外。辛普逊后又摸索出用量和药效情况,并应用于临床。现发现它对肝、肾有一定毒性,并有致癌可能而很少使用。
【氯仿的提纯】
(1) 光气和游离氯的检验
1) 光气检验: 光气易溶于苯和甲苯,难溶于冷水,遇热水发生水解,具有特别难闻的气味。取2ml氯仿于试管中,加入3滴蒸馏水和1滴硝酸银溶液 (0.2mol/l)。若出现白色混浊,说明有光气存在。
2) 游离氯的检验: 因为光气分解后生成氯气和一氧化碳,通过氯的检验能间接证明光气是否存在。于试管中滴入3滴氯仿、5滴蒸馏水和1滴碘化钾溶液 (0.5mol/l)。振摇后若氯仿因析出碘而变为玫瑰色或紫色,说明氯仿中有游离氯存在。
(2) 蒸馏法提纯
氯仿中含有水、乙醇、光气和游离氯等杂质。先在分液漏斗中用酚钠洗涤除去光气,用水洗除乙醇,也可用浓硫酸洗涤,水洗涤5~6次,每次用量为氯仿体积的一半,浓硫酸洗涤2次,每次用量为氯仿体积的5%。然后用氢氧化钠稀溶液洗两次、水洗 2~3次,再经无水氯化钙 (或无水硫酸钠、碳酸钾) 脱水后,进行蒸馏,蒸馏速度为1~2滴/s,收集沸程为60~62℃的馏出液,贮存于棕色磨口试剂瓶中。
蒸馏法若不能除去有机杂质可用活性炭吸附提纯。
【制备方法】
工业上氯仿可由甲烷氯化得到,也可由乙醇或乙醛与次氯酸钠作用制取:
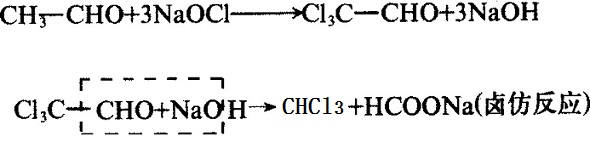
图4为工业制备氯仿化学反应路线图
① 以乙醛为原料,在碱性溶液中,与次氯酸钙反应,可制得氯仿[1]。也可以丙酮为原料,与次氯酸钙反应。
② 以甲烷为原料,直接氯化。此反应是一种强烈的放热反应,为了增加[1]的得率及减少副产物(一氯甲烷、二氯甲烷及四氯化碳),应严格控制甲烷与氯的摩尔比,同时控制反应温度,即使是这样,也不可能是单一的产品,只不过[1]的产率高些。
③ 六氯丙酮与氢氧化钠反应,可制得[1]。 CCl3COCCl3+NaOH→[1]+CCl3COONa
④ 以四氯化碳为原料,与氢氧化亚铁反应,可制得[1]。
⑤ 以四氯化碳为原料,在紫外光照射下,与乙醇反应,可制得[1]。CCl4+CH3CH2OH→[1]+ClCH2CH2OH
⑥ 四氯化碳在催化剂锌粉的作用下,用氢气还原,可制得氯仿[1]。
【危险情况】
(1)蒸气有毒,吸入会引起中毒。具有麻醉性。摄入或较长时间吸入会致死。美国食品药品管理局禁止在食品、药品和化妆品的包装,包括止咳药、牙膏等的包装中使用本品。
(2)不燃,但较长时间暴露于火焰或高温下能燃烧,发出剧毒和刺激性烟雾。如露置在日光、氧气、湿气中,特别是和铁接触时,则产生光气使人中毒。在高热作用下,能生成氯化氢和光气。空气中的容许浓度美国为10ppm (50mg/m3),我国有资料记载为50ppm (240mg/m3)*。
【侵入途径】 氯仿能迅速从肺部吸收,并广泛分布全身,也可经消化道或无损伤的皮肤吸收。停止接触后吸入的30~50%在15分钟内以原形随呼气排出,小部分在体内分解,以氯化物的形式由尿排出。蒸气吸入,摄入,与皮肤和眼接触。
【侵害部位】 神经系统,肝,肾,心脏,眼,皮肤。
【氯仿中毒和有害影响】
氯仿对皮肤有刺激作用,先出现烧灼感,以后发生红斑、水肿、起泡,也可引起皮肤干燥、皲裂,但无永久性损害。
氯仿在高浓度时具有较强的麻醉性,能刺激粘膜,并较快地从兴奋状态转为困倦、眩晕、至麻醉状态或终于致死。氯仿用作麻醉剂而造成的意外死亡,一般多由于对肝和心脏的损害。短时暴露于氯仿中能引起眩晕、倦怠、消化障碍、智力迟钝,乃至昏迷。慢性过量暴露能引起肝和肾损害。嗜酒者会使氯仿的影响更快和更严重。严重暴露所引起的肝功能障碍比中枢神经系统抑郁或肾损害更为明显。一般来说,氯仿的慢性中毒主要表现为呕吐、消化不良、食欲减退、虚弱,严重者出现精神异常。氯仿是已知致癌物。
本品如经燃烧特别是发生火灾时,则会产生光气。
【急救】
治疗主要为对症治疗。急性中毒禁用肾上腺素。贮存时可加入1~2%乙醇,使生成的光气与乙醇反应而形成无毒的碳酸乙酯[CO(OC2H5)2]。
此化学品如进入眼中,立即用水冲洗; 如接触皮肤,迅速用肥皂和水清洗干净; 如大量吸入蒸汽,立即移离现场至新鲜空气处,严重时输氧或进行人工呼吸; 如误被吞服,催吐,洗胃,严重者不进行催吐,立即送医院救治。
【防护措施】 生产设备要密闭化,生产现场加强通风,操作时要加强个人防护,穿适当工作服,并戴防护眼镜。工作者如皮肤被弄湿或受到污染,应迅速冲洗。可渗透的工作服如被弄湿或受到污染,迅速脱去。
【医学监护】 就业前和定期体检时应包括肝和肾功能的检查,应特别注意神经系统、皮肤疾病和酒精中毒史。检测呼气和血液中氯仿含量有助于鉴定急性暴露。
【测定方法】
(1) 在空气中的测定: 用活性炭吸附,CS2处理,气相色谱法分析。
(2) 在水中的测定: 用气相色谱法或气相色谱-质谱联用法分析。
【贮存】 用玻璃瓶或金属桶盛装,可加5%无水酒精作稳定剂。存放在阴凉、干燥、通风良好的地方。与强碱类物品隔开。为防止生成光气,应避光、隔热贮存。
【废弃物建议处理方法】 焚烧; 如与其他易燃燃料混合后焚烧更为可取。必须注意,要保证完全燃烧,以防止光气产生。为除去所产生的氢卤酸,装置酸涤气器是必要的。凡有可能,应进行回收,通过蒸馏提纯,送回供应厂。
【使用注意事项】
(1)氯仿为有机毒品,其主要毒害人的中枢神经系统,具有麻醉作用,可造成人的心、肝、肾的损害。 (2)氯仿遇紫外线或高热可形成光气,光气有剧毒,应注意。
(3)空气中最高允许浓度为50ppm。
(4)失火可用沙土、雾状水、二氧化碳扑救。
【参考资料】
罗明泉,俞平 编.常见有毒和危险化学品手册.北京:中国轻工业出版社.1992.第382-383页。
袁运开,顾明远 主编.科学技术社会辞典·化学.杭州:浙江教育出版社.1992.第223页。
http://www.chemicalbook.com/ProductChemicalPropertiesCB5413313.htm
http://baike.baidu.com/view/323925.htm