急性冠状动脉综合征(ACS)是一种常见的严重心血管疾病,临床上包括药物治疗、介入治疗及搭桥治疗等治疗方案,其中药物治疗是治疗的基石。原因可归因于该疾病的病理改变为动脉粥样硬化,因此延缓动脉粥样硬化进程是治疗的根本。血小板受体拮抗药作为抗血小板聚集药在ACS的治疗过程中发挥了重要作用。目前主要使用的血小板受体拮抗药为血小板细胞膜上ADP受体亚P2Y12的阻断剂―噻吩并吡啶类药物,噻吩并吡啶类药物的典型代表-氯吡格雷联合阿司匹林的双联抗血小板治疗是目前最常用的抗血小板治疗药,对ACS患者的治疗和预后产生了积极的作用。但是氯吡格雷具有某些局限性,氯吡格雷发挥作用需要肝脏代谢酶―细胞色素P450酶的激活,因此其起效慢,容易导致缺血危险的增加,与血小板受体的结合不可逆导致了撤药以后血小板功能恢复的渐进性,对于接受冠状动脉介入治疗的患者产生不利影响,在个体间具有广泛的可变性,在某些患者中容易发生氯吡格雷抵抗。
替格瑞洛(Ticagrelor),商品名为倍林达,是由英国阿斯利康公司研制开发的一种新的治疗急性冠脉综合征的药物,于2011年7月被美国FDA批准上市,上市后被众多国际治疗指南推荐用于ACS患者的治疗,包括欧洲心脏病学会ESC指南、美国心脏病学会ACC指南和美心脏协会AHA指南等,2012年11月替格瑞洛又获得了国家食品药品监督管理局SFDA颁发的进口药品许可证, 获准在中国正式上市。
替格瑞洛为环戊基三唑嘧啶类新型口服抗血小板药物,于2010年12月在欧洲上市,目前已在包括美国在内的85个国家批准上市,用于ACS的治疗,本身即为活性药物,通过直接可逆地结合到ADP结合点的P2Y12 受体上,有效地抑制ADP 介导的P2Y12 受体激活,受体在替格瑞洛脱离后依然具有功能,ADP 仍然能与原结合点结合 ;同时替格瑞洛的活性代谢产物AR-C124910XX(经CYP3A 途径代谢 ) 同样可拮抗P2Y12 受体,从而增强抗血小板功能。相对氯吡格雷,替格瑞洛具有如下优势 :一是直接对P2Y12 受体快速产生抑制效应而不需经代谢活化,相比氯吡格雷能更强效抑制血小板聚集 ;二是可逆性,抑制程度反映血浆浓度,在停药后循环中所有血小板均可恢复功能。
替格瑞洛无需肝药酶代谢活化且能快速可逆地拮抗P2Y12受体,从而避免了在代谢活化过程中因代谢酶活性差异而导致药物疗效的个体差异,故氯吡格雷抵抗的患者获益更多。由于替格瑞洛主要经肝脏清除,且目前尚未在严重肝损害患者中评估其安全性,故对这类患者禁用;此外替格瑞洛经CYP3A4代谢,故不建议与CYP3A4强效抑制剂或诱导剂合并使用。替格瑞洛的药动学参数和药效学不受治疗前是否服用氯吡格雷或对氯吡格雷低反应性的影响,这表明如果有需要患者可直接将氯吡格雷更换为替格瑞洛进行治疗;药效学的数据表明与氯吡格雷相比替格瑞洛可快速持续有效的产生剂量依赖性的血小板抑制作用,显著降低ACS患者,包括心血管死亡心肌梗死和脑卒中在内的主要复合终点,不明显增加大出血的风险,且其作用不受CYP2C19和ABCB1基因型的影响,因此,新型抗血小板药物替格瑞洛由于其独特的药动学和药效学特征而有望使更ACS患者获益。
氯吡格雷
氯吡格雷是ADP诱导的血小板聚集抑制剂,其通过直接抑制二磷腺苷与其受体结合以及继发ADP介导的糖蛋白GPⅡb/ Ⅲa复合物活化而起作用,可选择性地抑制二磷腺苷(ADP)与它的血小板受体的结合及继发的ADP介导的糖蛋白GPⅡ b/Ⅲa复合物的活化,因此可抑制血小板聚集。氯吡格雷必须经生物转化才能抑制血小板的聚集,但是还没有分离出产生这种作用的活性代谢产物。除ADP外,氯吡格雷还能通过阻断由释放的ADP引起的血小板活化的扩增,抑制其他激动剂诱导的血小板聚集。氯吡格雷不能抑制磷酸二酯酶的活性。临床上用于有过近期发作的卒中、心肌梗死和确诊外周动脉疾病的患者,可减少动脉粥样硬化性疾患的发生(如心肌梗死、卒中和血管性死亡)。
氯吡格雷经胃肠吸收后在肝脏内迅速代谢,血浆中原形药物浓度极低,其药代动力学资料多以主要循环代谢产物——无活性的SR26334为代表。口服给药后,F约50%。需经肝细胞色素P450酶系(可能主要是CYP1A亚家族)转化后产生具有活性的代谢产物。SR26334的Tmax约为1 h,T1/2为7~8h,重复给药3~7d后达到稳态,此时血小板聚集抑制率平均可达 40%~60%。停药后,一般于5~8d 内血小板聚集性(和出血时间)逐渐恢复至基线水平。首剂给予氯吡格雷负荷量(300~400 mg),继以75 mg,qd维持,其作用可提前于给药30 min内出现,2h内达到稳态水平,且耐受良好,尤其适用于紧急状况(如急性心梗、支架植入术后)。
阿司匹林并不增强氯吡格雷抑制 ADP诱导的血小板聚集作用,但二药合用在抑制胶原和凝血酶诱导的血小板聚集、活化方面较各自单用均明显增强。
药代动力学
替格瑞洛在人体内被迅速吸收,稳态分布容积为87.5L,中位达峰时间约为1.5h,ARC124910XX亦在体内快速形成,中位达峰时间约为2.5h,血药浓度约为替格瑞洛的30%~40%,二者主要分布于血液系统,性别、年龄、严重肾功能损害及轻度的肝功能损害不影响它们与血浆蛋白的结合。在健康人群中的研究表明,替格瑞洛及AR-C124910XX的血药浓度与口服剂量成正比,提示替格瑞洛及AR-C124910XX的药代动力学具有线性特征,高脂饮食不影响健康受试者替格瑞洛最大血药浓度(Cmax)及AR-C124910XX血药浓度时间曲线下面积(AUC),但与饥饿状态下相比,高脂饮食可使替格瑞洛AUC增加21%,同时使AR-C124910XX的Cmax降低22%,这对替格瑞洛的临床疗效影响较小。
替格瑞洛主要经CYP3A4代谢,ARC124910XX也主要由CYP3A4介导形成,而它们与其他CYO3A4底物之间的相互作用有激活,也有抑制,且二者均为弱效的P-糖蛋白抑制剂。替格瑞洛主要经肝脏代谢消除,其平均半衰期为7.2h,AR-C124910XX平均半衰期为8.5h,口服放射性标记的替格瑞洛后,放射活性的平均回收率大约为84%(粪便57.8%,尿液26.5%)。
药物相互作用
1.替格瑞洛与常用心血管药物的相互作用
替格瑞洛主要经CYP3A4代谢,其他经CYP3A介导的药物可能与替格瑞洛发生相互作用,从而改变替格瑞洛的药代动力学性质。有研究显示,经CYP3A途径代谢的药物约占所有药物的50%,药效学研究亦表明冠心病治疗中常用的几种药物与P2Y12受体拮抗剂有相互作用,这些相互作用的临床意义已引起了人们的关注。
非二氢吡啶类钙拮抗剂地尔硫卓为中度CYP3A4抑制剂,有研究表明,地尔硫卓可使替格瑞洛的AUC和Cmax分别增加174%和69%,使AR-C124910XX的AUC和Cmax分别降低13%和38%,这些差异临床意义较小,而替格瑞洛对地尔硫的血浆水平无影响,故维拉帕米或地尔硫卓可以与替格瑞洛联用。
体外研究表明,替格瑞洛是P-糖蛋白的底物及弱抑制剂,一项在健康志愿者中进行的随机、双盲、交叉研究表明,当与地高辛合用时,与安慰剂组相比,替格瑞洛可使地高辛的Cmax和AUC分别增加75%和28%,但地高辛经肾清除率不受替格瑞洛影响,地高辛对替格瑞洛及AR-C124910XX的代谢无影响。由于地高辛的治疗范围窄、易产生心脏毒性,故替格瑞洛与地高辛联用时应严密监测血药浓度,并观察其不良反应的发生情况,慎与其他P-糖蛋白抑制剂(如异博定和奎尼丁)联用。
2.替格瑞洛与CYP酶抑制剂或诱导剂的相互作用
(1)替格瑞洛与CYP酶抑制剂环孢菌素是CYP3A4强抑制剂,研究表明,环孢菌素显著升高替格瑞洛及ARC124910XX的血药浓度,而替格瑞洛对环孢菌素的药代动力学参数无影响。因合并用药会使替格瑞洛及AR-C124910XX血药浓度显著升高,进而增加患者出血风险,因此,应避免环孢菌素与替格瑞洛联合应用或适当调整用药剂量。
抗真菌药伊曲康唑、酮康唑、伏立康唑及抗逆转录病毒药物安普那韦、地瑞那韦等都是CYP3A4强抑制剂,与替格瑞洛联用时,酮康唑可使替格瑞洛的AUC和Cmax分别升高7.3倍和2.4倍,同时使AR-C124910XX的AUC和Cmax分别降低56%和89%,预期其他CYP3A4强抑制剂有类似作用,均应避免与替格瑞洛联用。
葡萄柚汁是CYP3A4抑制剂,研究表明,葡萄柚汁可使替格瑞洛的血药浓度增加2倍,提高替格瑞洛抗血小板作用,延长其抗血小板作用时间,二者联用时需谨慎。
(2)替格瑞洛与CYP酶诱导剂
一项关于血小板聚集的研究表明,苯妥英诱导替格瑞洛代谢,减弱其抗血小板作用,预期其他CYP3A4诱导剂(如地塞米松、卡马西平和苯巴比妥等)也会降低替格瑞洛的血药浓度,应避免替格瑞洛与此类药物的联用。
利福平可使替格瑞洛的Cmax、AUC、t1/2分别降低73%、86%、67%,对AR-C124910XX的Cmax无影响,但可使其AUC降低46%,当两药联用时,替格瑞洛最大血小板聚集抑制率(IPA)不受影响,该研究结果提示,利福平可显著降低替格瑞洛血药浓度,使其疗效下降,强的CYP3A/P-糖蛋白诱导剂应避免与替格瑞洛联合应用。
(3)替格瑞洛与其他经CYP酶代谢药物CYP酶在质子泵抑制剂(PPIs)的代谢起重要作用,研究表明,替格瑞洛与PPIs联用1年后,与只接受替格瑞洛治疗的患者相比,心血管事件(心血管死亡、心肌梗死、卒中)的发生率增加;均予以替格瑞洛时,在接受非PPI类胃肠道药物治疗的患者与接受一种PPI药物相比心血管事件发生率相似,在没有接受胃肠道药物治疗的患者心血管事件发生率显著降低。但PPIs对替格瑞洛血小板聚集抑制率的影响仍缺乏药代动力学研究。
甲苯磺丁脲是CYP2C9酶作用底物,一项随机、双盲、交叉研究表明,替格瑞洛对甲苯磺丁脲及4-羟基甲苯磺丁脲的药代动力学参数无影响,甲苯磺丁脲对替格瑞洛及AR-C124910XX的代谢亦无影响,该研究提示替格瑞洛并不是CYP2C9的抑制剂,且不改变经CYP2C9介导的药物代谢,如华法林等,故二者可以联用。
左炔诺孕酮和炔雌醇是目前使用最广泛的口服避孕药。CYP3A参与乙炔雌二醇和左炔诺孕酮的代谢,研究表明,与替格瑞洛联用时炔雌醇的AUC和Cmax分别增加20%和31%,替格瑞洛对左炔诺孕酮的药代动力学参数无影响,提示当与炔雌醇/左炔诺孕酮联合用药时,替格瑞洛可能对后者的避孕效果及安全性无影响。
咪达唑仑的代谢主要经CYP3A4介导,两项随机交叉研究证实:替格瑞洛轻度激活咪达唑仑1'-羟基化反应,同时轻度抑制咪达唑仑4'-羟基化反应,此外替格瑞洛影响肝脏和胃肠道CYP3A酶的活性。
合成路线
2-[( ( 3aR,4S,6R,6aS) -6-[( 5-氨基-6-氯-2-丙硫基) 嘧啶氨基]-2,2-二甲基四氢-3aH-环戊基[d][1,3]二氧-4-基) 氧]-1-乙醇(5)的合成
将化合物3、化合物4及异丙醇(IPA) 加入到反应釜中,搅拌,加入二异丙基乙胺(DIPEA),N2保护并密封,缓慢升温,搅拌。冷却至室温,减压蒸除溶剂,得棕红色固体,加入乙酸乙酯和水,搅拌,分得有机层,乙酸乙酯萃取水层,合并有机相,饱和氯化钠溶液洗涤,无水硫酸钠干燥,减压蒸除溶剂,正庚烷重结晶得5。
2-[( ( 3aR,4S,6R,6aS) -6-( 7-氯-5-丙硫基-3H-[1,2,3]三唑[4,5-d]嘧啶-3-基) -2,2-二甲基四氢-3aH-环戊基[d][1,3]二氧-4-基) 氧]-1-乙醇(6) 的合成
将5加入到水和冰乙酸中,再加入溴化钠冰浴下搅拌,缓慢滴加亚硝酸钠水溶液,室温搅拌。TLC检测至反应完毕,加入乙酸乙酯,滴加碳酸钾水溶液调至pH8-9。分得有机层,乙酸乙酯萃取水层,合并有机相,依次用碳酸钾水溶液、氯化钠溶液洗涤,无水硫酸钠干燥,减压蒸除溶剂,得6。
2-[( ( 3aR,4S,6R,6aS) -6-( 7-[( 1R,2S) -2-( 3,4-二氟苯基) 环丙胺基]-5-丙硫基-3H-[1,2,3]三唑[4,5-d]嘧啶-3-基) -2,2-二甲基四氢-3aH-环戊基[d][1,3]二氧-4-基) 氧]-1-乙醇(7)的合成
将化合物2加入到乙酸乙酯中,15-20℃ 搅拌,缓慢滴加三乙胺,滴毕搅拌。缓慢滴加乙酸乙酯溶液,滴毕,室温搅拌。TLC检测至反应完毕,加入水,分得有机层,乙酸乙酯萃取水层,合并有机相,依次用乙酸水溶液、饱和氯化钠洗涤,经无水硫酸钠干燥,减压蒸除溶剂,得7。
替格瑞洛(1)的合成
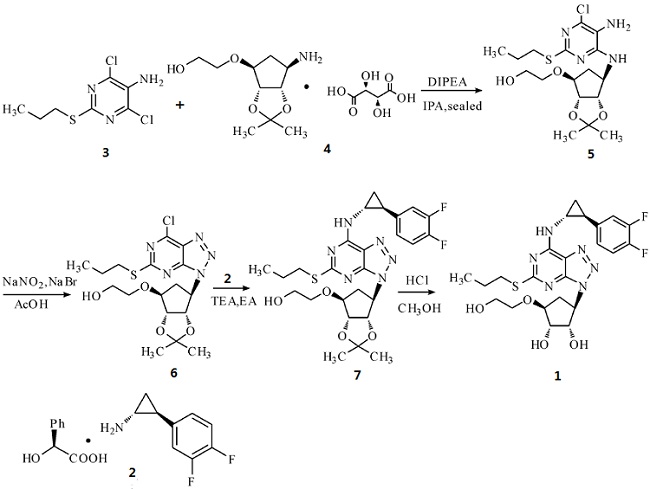
图1为替格瑞洛的合成路线
【主要参考资料】
http://www.chemicalbook.com/ProductChemicalPropertiesCB51509134.htm
[1] 邱怡敏等. 抗血小板新药替格瑞洛的应用现状及前景. 世界临床药物. 2015,36(11):784-788.
[2] 王仙等. 抗血小板聚集新药―替格瑞洛. 中国医院药学杂志. 2013,33(11):900-902.
[3] 李慕鹏等. 抗血小板药物替格瑞洛药代药效动力学及遗传药理学研究进展. 中国临床药理学与治疗学. 2014,19(2):214-221.
[4] 曾志旋等. 替格瑞洛的合成工艺改进.化学研究与应用. 2015,27(3):373-375.
[5] 陆凤翔,杨玉 主编.临床实用药物手册.南京:江苏科学技术出版社.2008.
[6] 周文,周序斌,韩文修 主编.最新药物手册.济南:山东科学技术出版社.2005.
[7] 王丹利等.替格瑞洛的药代动力学及与其他药物的相互作用。2015,31(6):623-626.