16728-64-6
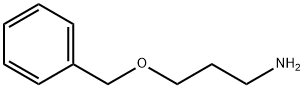 16728-64-6 结构式
16728-64-6 结构式
基本信息
3-苯甲氧丙基1-胺
3-苄氧基-1-丙胺
[3-(苄氧基)丙基]胺盐酸盐
3-(苄氧基)丙-1-胺盐酸盐
3-Benzyloxypropane-1-amine
3-(benzyloxy)-1-propanamine
3-phenylmethoxypropan-1-amine
1-Propanamine, 3-(phenylmethoxy)-
4-Benzofuranpropanenitrile,β-oxo-
[3-(benzyloxy)propyl]amine hydrochloride
3-(benzyloxy)propan-1-amine hydrochloride
物理化学性质
制备方法
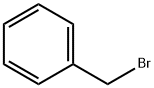
100-39-0

156-87-6

16728-64-6
在室温下,将60%氢化钠分散体(4g,0.1mol)缓慢加入搅拌中的3-氨基-1-丙醇(7.51g,0.1mol)的四氢呋喃(THF,150mL)溶液中。反应混合物在氮气保护下搅拌30分钟后,加入溴化苄(11.9mL,0.1mol)。继续在室温下搅拌反应10小时,随后进行真空浓缩。将浓缩后的残余物在1N盐酸水溶液和二氯甲烷(CH2Cl2)之间分配。水层用10%氢氧化钠水溶液调节至pH 10,随后用二氯甲烷(3×100mL)萃取。合并有机相,用硫酸镁(MgSO4)干燥,真空浓缩。通过硅胶柱色谱法,使用二氯甲烷/甲醇(3:1至2:1,v/v)作为洗脱剂,纯化残余物,得到3-(苄氧基)丙胺(8.3%收率),为黄色油状物。在0℃下,将1,3-二环己基碳二亚胺(14.4mg,0.07mmol)的二氯甲烷(2mL)溶液滴加到化合物5(32mg,0.07mmol)、3-(苄氧基)丙胺(0.07mmol)和1-羟基苯并三唑水合物(9.5mg,0.07mmol)的二氯甲烷(5mL)溶液中。反应混合物在室温下搅拌18小时后,进行真空浓缩。通过硅胶柱色谱法,使用二氯甲烷/甲醇(30:1,v/v)作为洗脱剂,纯化残余物,得到化合物8(36mg,85%收率),为浅黄色液体。1H NMR(CDCl3)δ 8.05(s,1H,H4),7.44(d,1H,H5,J = 8.7Hz),7.19-7.28(m,11H,H6 + 2×OCH2Ph),6.78-6.82(m,3H,H2' + H5' + H6'),6.06(AB,2H,3',4'-OCH2O-,J = 6.9Hz,J = 1.5Hz),5.84(AB,2H,7,8-OCH2O-,J = 4.2Hz,J = 1.5Hz),4.45(s,4H,2×OCH2Ph),4.38(s,2H,2-CH2OBn),3.55(m,4H,3-CONHCH2CH2CH2OBn),1.87(五重峰,2H,3-CONHCH2CH2CH2OBn,J = 6.3Hz);MS(FAB,阳性)m/z 604 [M + H]+。
参考文献:
[1] Journal of Medicinal Chemistry, 2005, vol. 48, # 2, p. 534 - 546
[2] Patent: WO2005/107742, 2005, A1. Location in patent: Page/Page column 40-41
