195202-08-5
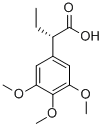 195202-08-5 结构式
195202-08-5 结构式
基本信息
2(S)-2-(3,4,5-三甲氧基苯基)丁酸
(S)-2-(3,4,5-TRIMETHOXYPHENYL)BUTYRIC ACID
(S)-2-(3,4,5-Trimethoxyphenyl)butanoic acid
(2S)-2-(3,4,5-Trimethoxyphenyl)butyric acid
(2S)-2-(3,4,5-Trimethoxyphenyl)butanoic acid
(2S)-2-(3,4,5-Trimethoxyphenyl)butanoic acid 98%
Benzeneacetic acid, α-ethyl-3,4,5-trimethoxy-, (αS)-
Benzeneacetic acid, a-ethyl-3,4,5-triMethoxy-, (aS)-
物理化学性质
制备方法
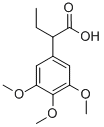
195202-06-3

195202-08-5
以2-(3,4,5-三甲氧基苯基)丁酸为原料合成(S)-2-(3,4,5-三甲氧基苯基)丁酸的一般步骤(1g): 步骤7. (S)-2-(3,4,5-三甲氧基苯基)丁酸(AP17360)的合成。将AP14900 [195202-08-5](500g,1.97摩尔)和(-)-辛可尼定(580g,1.97摩尔)加入装有机械搅拌的10L反应器中。加入乙腈(7500mL)并将混合物加热至回流30分钟。使均相溶液冷却至室温,形成盐。过滤固体,并使用乙腈(7000mL、7000mL、6500mL、6500mL和5000mL)作为溶剂进行5次重结晶。将非对映体盐悬浮于水(1400mL)和二氯甲烷(600mL)中,搅拌至盐完全溶解。通过加入浓盐酸调节搅拌的混合物至pH 2,分离有机层,水层用二氯甲烷(2×300mL)萃取。合并有机层,用1N盐酸溶液(2×200mL)洗涤以除去残留的(-)-辛可尼定。酸洗液再用二氯甲烷(100mL)萃取,合并所有二氯甲烷溶液。合并的有机溶液用10%碳酸氢钠水溶液(200mL)洗涤,经无水硫酸镁干燥,旋转蒸发浓缩至约250mL,加入己烷(500mL)。溶液加热后冷却,再加入己烷(200mL)。旋转蒸发浓缩至出现固体,静置过夜。过滤所得固体,用己烷(2×300mL)研磨,50℃真空干燥84小时,得到产物(105.0g,21%),为灰白色固体:[α]22D +54.8(c=1.07,甲醇,30分钟,99.1%ee);1H NMR(DMSO-d6,300MHz)δ 6.34(s,2H),3.52(s,6H),3.40(s,3H),3.11(t,J=7.6Hz,1H),1.76-1.64(m,1H),1.46-1.36(m,1H),0.60(t,J=7.3Hz,3H);13C NMR(DMSO-d6,75MHz)δ 175.1,153.1,136.9,135.8,105.4,60.3,56.2,53.1,26.7,12.4。元素分析(C13H18O5)计算值:C,61.41;H,7.13。实测值:C,61.47;H,7.20。
参考文献:
[1] Patent: WO2012/103279, 2012, A2. Location in patent: Page/Page column 11-12
