290307-40-3
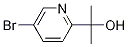 290307-40-3 结构式
290307-40-3 结构式
基本信息
2-(5-溴吡啶-2-基)丙-2-醇
2-(5-溴-2-吡啶基)-2-丙醇
2-(5-溴吡啶-2-基)丙烷-2-醇
2-(5-Bromo-2-pyridyl)-2-propanol
2-(5-Bromo-2-pyridyl)propan-2-ol
2-(5-Bromopyridin-2-yl)propan-2-ol
2-Pyridinemethanol, 5-bromo-α,α-dimethyl-
5-Bromo-2-(1-hydroxy-1-methylethyl)pyridine
1-(5-bromopyridin-2-yl)-3-methylbutan-1-one
5-Bromo-2-(1-hydroxy-1-methylethyl)pyridine ISO 9001:2015 REACH
物理化学性质
制备方法
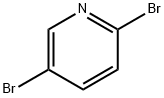
624-28-2
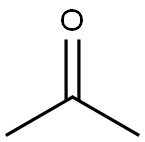
67-64-1
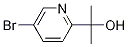
290307-40-3
1. 在2L圆底烧瓶中,将2,5-二溴吡啶(54g,228mmol)溶解于甲苯(600mL)中,形成无色溶液。将反应体系冷却至-78℃,并控制温度不超过-70℃,缓慢加入正丁基锂(2.5M己烷溶液,100mL,251mmol)。反应混合物在-78℃下搅拌30分钟后,迅速加入丙酮(20.08mL,274mmol)。继续搅拌30分钟,随后用饱和氯化铵水溶液淬灭反应。分离有机层,用盐水洗涤,无水硫酸钠干燥,减压浓缩除去溶剂。粗产物通过柱色谱法纯化(洗脱剂:20-50%乙酸乙酯/庚烷),得到2-(5-溴吡啶-2-基)-2-丙醇(42.5g,产率86%)。 2. 在1L圆底烧瓶中,将2-(5-溴吡啶-2-基)-2-丙醇(10g,46.3mmol)与4-甲基-3-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂环戊烷-2-基)苯胺(11.87g,50.9mmol)溶于二恶烷(300mL)中,加入饱和碳酸氢钠水溶液(150mL)。反应混合物经氮气脱气后,加入四(三苯基膦)钯(2.67g,2.314mmol)。加热至回流,反应液先变稠后溶解。回流2小时后,冷却至室温,减压浓缩除去溶剂。残余物用乙酸乙酯和水分配,有机层用无水硫酸钠干燥,减压浓缩,得到2-(5-(5-氨基-2-甲基苯基)吡啶-2-基)-2-丙醇。 3. 将上述粗产物溶解于二恶烷(30mL)中,冷却至0℃。通过加料漏斗缓慢加入硫酸,初始需手动搅拌至完全溶解。反应放热至30℃,搅拌30分钟。通过LC/MS监测反应完成后,将反应液倒入冰上,用乙酸乙酯(2×200mL)萃取。水相用50%氢氧化钠溶液调节pH至9-10,再用乙酸乙酯萃取。合并有机层,用盐水洗涤,无水硫酸钠干燥,减压浓缩。粗产物通过柱色谱法纯化(洗脱剂:0-100%乙酸乙酯/庚烷),得到4-甲基-3-(6-(丙-1-烯-2-基)吡啶-3-基)苯胺(9g,两步总产率86%)。 4. 将4-甲基-3-(6-(丙-1-烯-2-基)吡啶-3-基)苯胺(9g,40.1mmol)溶于乙醇(100mL)中,加入10%钯碳(0.5g)。在30psi氢气压力下氢化2小时。反应完成后,过滤除去催化剂,滤液浓缩,得到3-(6-异丙基吡啶-3-基)-4-甲基苯胺(8g,产率88%)。
参考文献:
[1] Patent: US2010/41642, 2010, A1. Location in patent: Page/Page column 22
[2] Patent: WO2010/62571, 2010, A1. Location in patent: Page/Page column 94-95
[3] Journal of Medicinal Chemistry, 2015, vol. 58, # 13, p. 5323 - 5333
[4] Tetrahedron Letters, 2000, vol. 41, # 22, p. 4335 - 4338
[5] Patent: WO2005/92899, 2005, A1. Location in patent: Page/Page column 81

