868539-96-2
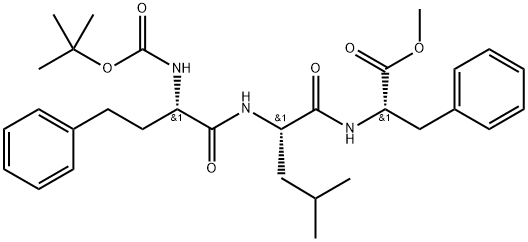 868539-96-2 结构式
868539-96-2 结构式
基本信息
PR171关键中间体IV
PR171(卡非佐米)关键中间体
N-[(S)-2-(叔丁氧羰基氨基)-4-苯基丁酰基]-L-亮氨酰-L-苯丙氨酸甲酯
(6S,9S,12S)-甲基 12-苄基-9-异丁基-2,2-二甲基-4,7,10-三氧代-6-苯乙基-3-氧杂-5,8,11-三氮杂十三烷-13-酸酯
Carfilzomib Impurity 70
methyl ((S)-2-((tert-butoxycarbonyl)amino)-4-phenylbutanoyl)-L-leucyl-L-phenylalaninate
N-[(S)-2-(tert-Butoxycarbonylamino)-4-phenylbutanoyl]-L-leucyl-L-phenylalanine methyl ester
L-Phenylalanine, (αS)-α-[[(1,1-dimethylethoxy)carbonyl]amino]benzenebutanoyl-L-leucyl-, methyl ester
(S)-methyl 2-((S)-2-tert.butoxycarbonyIamino-4-phenylbutanamido-4-methylpentanamido)-3-phenylpropanoate
Methyl N-[(2S)-2-({[(2-methyl-2-propanyl)oxy]carbonyl}amino)-4-phenylbutanoyl]-L-leucyl-L-phenylalaninate
(6S,9S,12S)-Methyl 12-benzyl-9-isobutyl-2,2-dimethyl-4,7,10-trioxo-6-phenethyl-3-oxa-5,8,11-triazatridecan-13-oate
物理化学性质
制备方法
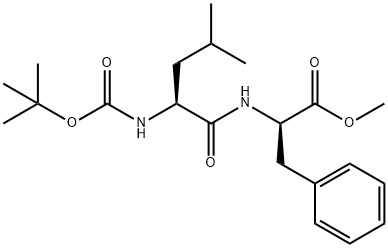
15136-32-0
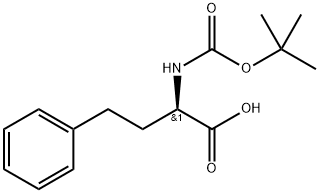
82732-07-8

868539-96-2
1. 在500 mL DMF中溶解NBoc亮氨酸(11.56 g, 50.0 mmol)和苯丙氨酸甲酯(10.78 g, 50.0 mmol),加入羟基苯并三唑(HOBT)(10.81 g, 80.0 mmol)和N,N-二异丙基乙胺(DIEA)(25.85 g, 35 mL, 200.0 mmol)。 2. 将反应混合物置于冰水浴中冷却至0℃,在5分钟内分批加入苯并三唑-1-基氧基三(二甲基氨基)鏻六氟磷酸盐(BOP)(35.38 g, 80.0 mmol)。 3. 在氩气保护下,将反应混合物搅拌过夜。 4. 反应完成后,用1000 mL盐水稀释反应混合物,并用乙酸乙酯(EtOAc)(5×200 mL)萃取。 5. 合并有机层,依次用水(10×100 mL)和盐水(2×150 mL)洗涤,用无水硫酸镁(MgSO4)干燥。 6. 过滤除去MgSO4,减压浓缩去除溶剂,得到化合物A(18.17 g)。 7. 将化合物A(18.0 g, 45.86 mmol)溶解于50 mL预冷至0℃的80%三氟乙酸(TFA)/二氯甲烷(DCM)溶液中。 8. 搅拌反应混合物,并在2小时内缓慢升温至室温。 9. 减压浓缩去除挥发物,得到油状物。 10. 向油状物中加入Boc-D-高苯丙氨酸(BocNHhPhe)(12.81 g, 45.86 mmol)、DMF(500 mL)、HOBT(9.91 g, 73.37 mmol)和DIEA(23.70 g, 32.0 mL, 183.44 mmol)。 11. 将反应混合物置于冰水浴中冷却至0℃,在5分钟内分批加入BOP(32.45 g, 73.37 mmol)。 12. 在氩气保护下,将反应混合物搅拌过夜,并缓慢升温至室温。 13. 反应完成后,用1500 mL水稀释反应混合物,并用二氯甲烷(DCM)(5×300 mL)萃取。 14. 合并有机层,依次用水(6×300 mL)和盐水(1×300 mL)洗涤,用无水硫酸镁(MgSO4)干燥。 15. 过滤除去MgSO4,减压浓缩去除溶剂,得到黄色固体。 16. 将黄色固体溶解于200 mL 95%乙醇(EtOH)中,加热至65℃使固体完全溶解。 17. 将热溶液缓慢倒入1000 mL冷水中,收集析出的沉淀,得到化合物B(21.59 g)。
参考文献:
[1] Patent: KR2015/131405, 2015, A. Location in patent: Paragraph 0447-0450
[2] Journal of Medicinal Chemistry, 2018,
