879275-33-9
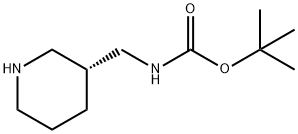 879275-33-9 结构式
879275-33-9 结构式
基本信息
R-3-N-BOC-氨甲基哌啶盐酸盐
(R)-N-BOC-1-(3-哌啶基)甲胺
(R)-[[哌啶-4-基]甲基]氨基甲酸叔丁酯
(R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯
N - [(3R) - 哌啶-3-基甲基]氨基甲酸叔丁酯
-tert-Butyl (piperidin-3-ylmethyl)
(R)-N-Boc-1-(3-piperidyl)methanamine
R-3-N-BOC-AMINOMETHYL PIPERIDINE-HCL 97+%
tert-Butyl (R)-piperidin-3-ylmethylcarbamate
tert-butyl N-[(3R)-piperidin-3-ylmethyl]carbamat
tert-butyl N-[(3R)-piperidin-3-ylMethyl]carbaMate
1,1-Dimethylethyl N-[(3R)-3-piperidinylmethyl]carbamate
-[(3R)-3-PIPERIDINYLMETHYL]-CARBAMIC ACID 1,1-DIMETHYLETHYL ESTER
N-[(3R)-3-PIPERIDINYLMETHYL]-CARBAMIC ACID 1,1-DIMETHYLETHYL ESTER
物理化学性质
制备方法
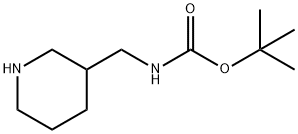
142643-29-6
![(R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯](/CAS/GIF/879275-33-9.gif)
879275-33-9
以3-Boc-氨甲基哌啶为原料合成(R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯的一般步骤如下:实施例3(3R)-N-(叔丁氧基羰基)-3-氨基甲基哌啶(化合物4)的合成;将4N-(叔丁氧基羰基)-3-氨基甲基哌啶(10g,1当量,47mmol)与(+)-0,0'-二对甲苯基-D-酒石酸(15.52g,1当量,47mmol)在干燥的甲醇(100ml)中混合,缓慢加热至回流,形成溶液。将溶液冷却至室温并在该温度下搅拌5-6小时,得到白色悬浮液,过滤并用最小量的无水甲醇洗涤。粗盐通过甲醇重结晶一次,将得到的盐悬浮于蒸馏水(25ml)中并冷却至0℃。随后分批加入10%碳酸钠溶液(100ml)直至悬浮液呈强碱性。反应混合物继续搅拌10分钟,用乙酸乙酯(5×50ml)萃取。合并有机层,用无水硫酸钠干燥,减压浓缩,得到化合物4。产量:3.2g,收率62%。[α]D°C:-8.97(c=1.0;甲醇)。熔点:64-66°C。IR(Neat):3362, 2970, 1703, 1520, 1454, 1365, 1172 cm-1。1H NMR(CDCl3, 300MHz)δ1.00-1.22(m, 2H, H-4);1.40(s, 9H, -O-C(CH3)3);1.57-1.72(m, 3H, H-3, H-5);2.21-2.32(m, 1H, CHaNHBoc);2.44-2.57(m, 1H, CHbNHBoc);2.92-3.05(m, 4H, H-2, H-4);4.72(brs, 1H, NH)。13C NMR(CDCl3, 300MHz)26.56, 29.03, 29.58, 38.44, 44.99, 47.46, 51.16, 79.73, 156.72。FAB MS(m/z):215 [M+1]+。
参考文献:
[1] Patent: WO2012/104866, 2012, A1. Location in patent: Page/Page column 16-17
[2] Patent: WO2006/28904, 2006, A1. Location in patent: Page/Page column 280
| 报价日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
| 2025/12/22 | XW0287927533904 | (R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯 (R)-tert-Butyl (piperidin-3-ylmethyl)carbamate | 879275-33-9 | 25g | 1001元 |
| 2025/12/22 | XW0287927533903 | (R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯 (R)-tert-Butyl (piperidin-3-ylmethyl)carbamate | 879275-33-9 | 10g | 401元 |
| 2025/12/22 | XW0287927533902 | (R)-[[哌啶-3-基]甲基]氨基甲酸叔丁酯 (R)-tert-Butyl (piperidin-3-ylmethyl)carbamate | 879275-33-9 | 5g | 208元 |

