880769-95-9
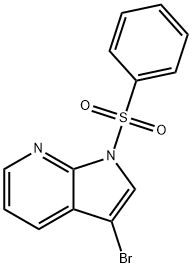 880769-95-9 结构式
880769-95-9 结构式
基本信息
3-溴-1-甲基磺酰基-1H-吡咯并[2,3-B]吡啶
1-(苯磺酰基)-3-溴-1H-吡咯并[2,3-B]吡啶
1-苯磺酰基-3-溴-1H-吡咯[2,3-B]吡啶,95%
1H-吡咯并[2,3-B]吡啶, 3-溴-1-(苯基磺酰基)-
3-溴-1-甲基磺酰基-1H-吡咯并[2,3-B]吡啶 10G
3-Bromo-1-phenylsulfonyl-7-azaindole,95%
3-BroMo-1-phenylsulfonyl-7-azaindole, 95%
1-(Benzenesulfonyl)-3-bromo-pyrrolo[2,3-b]pyridine
3-Bromo-1-(phenylsulfonyl)-1H-pyrrolo[2,3-b]pyridine
1-(Benzenesulfonyl)-3-bromo-1H-pyrrolo[2,3-b]pyridine
1H-Pyrrolo[2,3-b]pyridine, 3-bromo-1-(phenylsulfonyl)-
1-Phenylsulfonyl-3-broMo-1H-pyrrolo[2,3-b]pyridine, 95%
物理化学性质
制备方法
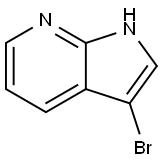
74420-15-8
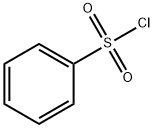
98-09-9
![3-溴-1-甲基磺酰基-1H-吡咯并[2,3-B]吡啶](/CAS/GIF/880769-95-9.gif)
880769-95-9
在氮气保护下,将3-溴-1H-吡咯并[2,3-b]吡啶(175 mg,0.89 mmol)、四丁基溴化铵(10 mg,0.03 mmol)、精细研磨的氢氧化钠(107 mg,2.67 mmol)和二氯甲烷(5 mL)加入干燥的圆底烧瓶中,搅拌混合。将反应混合物置于冰浴中冷却至0℃,随后缓慢滴加苯磺酰氯(0.142 mL,1.11 mmol)。滴加完毕后,将反应混合物逐渐升温至室温,并在此温度下持续搅拌1小时。反应完成后,加入水(6 mL)淬灭反应,用二氯甲烷萃取两次。合并有机层,依次用水和饱和氯化钠溶液洗涤,无水硫酸镁干燥。减压浓缩有机层,得到橙色固体粗产物。将粗产物在戊烷中研磨,过滤,用戊烷洗涤并干燥,最终得到294 mg目标化合物3-溴-1-(苯基磺酰基)-1H-吡咯并[2,3-b]吡啶,收率98%。产物经1H NMR(300 MHz,CDCl3)表征,化学位移δ(ppm)如下:8.48(dd,J = 1.5, 4.8 Hz,1H),8.24-8.17(m,2H),7.82(dd,J = 1.5, 8.0 Hz,1H),7.79(s,1H),7.60(dd,J = 7.5 Hz,1H),7.54-7.46(m,2H),7.27(dd,J = 4.8, 8.0 Hz,1H)。
参考文献:
[1] European Journal of Medicinal Chemistry, 2016, vol. 108, p. 701 - 719
[2] Patent: US2006/100218, 2006, A1. Location in patent: Page/Page column 52
[3] Patent: US2011/15173, 2011, A1. Location in patent: Page/Page column 30
[4] Patent: US2011/257187, 2011, A1. Location in patent: Page/Page column 21-22
[5] Patent: US2011/257189, 2011, A1. Location in patent: Page/Page column 35
