930785-40-3
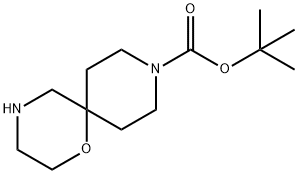 930785-40-3 结构式
930785-40-3 结构式
基本信息
1-氧杂-4,9-二氮杂螺[5.5]十一碳-9-甲酸叔丁酯
1-氧杂-4,9-二氮杂螺[5.5]十一烷-9-甲酸叔丁酯
叔丁基 1-氧杂-4,9-二氮杂螺[5.5]十一烷-9-甲酸酯
叔丁基 3,4-二氢-2H-螺[萘-1,4'-哌啶]-1'-甲酸酯
9-Boc-1-Oxa-4,9-diazaspiro[5.5]undecane
1-Oxa-4,9-diazaspiro[5.5]undecane,N9-BOCprotected
TERT-BUTYL 1-OXA-4,9-DIAZASPIRO[5.5]UNDECANE-9-CARBOXYLATE
1-Oxa-4,9-diaza-spiro[5.5]undecane-9-carboxylic acid tert-butyl ester
1-Oxa-4,9-diazaspiro[5.5]undecane-9-carboxylic acid, 1,1-diMethylethyl ester
物理化学性质
制备方法
![叔丁基 3-氧代-1-氧杂-4,9-二氮杂螺[5.5]十一烷-9-甲酸酯](/CAS2/GIF/1160247-07-3.gif)
1160247-07-3
![1-氧杂-4,9-二氮杂螺[5.5]十一烷-9-甲酸叔丁酯](/CAS/GIF/930785-40-3.gif)
930785-40-3
该反应分12批进行,具体步骤如下:将硼烷-二甲硫醚络合物(10M,溶于二甲基硫醚中,75mL,750mmol)缓慢滴加到叔丁基 3-氧代-1-氧杂-4,9-二氮杂螺[5.5]十一烷-9-甲酸酯(50g,180mmol)的四氢呋喃(1.5L)溶液中。反应混合物在70℃下回流加热6小时,随后在25℃下搅拌10小时。反应完成后,用甲醇(500mL)淬灭反应,继续在25℃下搅拌30分钟,之后在减压下浓缩。所得白色固体溶于甲醇(1L)中,加入N,N'-二甲基乙烷-1,2-二胺(65g,740mmol),在70℃下回流加热16小时。将12批反应混合物合并,真空浓缩,得到淡黄色油状物。将此油状物溶解于二氯甲烷(4L)中,用氯化铵水溶液(4×2L)洗涤,硫酸钠干燥,过滤后减压浓缩。残余物与石油醚(500mL)在25℃下研磨30分钟,得到白色固体产物(304g)。研磨后的滤液经真空浓缩,残余物用石油醚(200mL)在25℃下研磨36小时,得到额外的白色固体产物(135g)。总产率:439g,1.71mol,77%。LCMS m/z 257.2 [M + H]+。1H NMR(400MHz,CDCl3)δ3.85-3.59(m,4H),3.14(br dd,J = 11,11Hz,2H),2.84(dd,J = 4.9,4.6Hz,2H),2.68(s,2H),2.02-1.84(br m,2H),1.47-1.33(m,2H),1.45(s,9H)。
参考文献:
[1] Bioorganic and Medicinal Chemistry Letters, 2010, vol. 20, # 24, p. 7458 - 7461
[2] Patent: WO2017/21805, 2017, A1. Location in patent: Page/Page column 83; 85
[3] Patent: US2018/208608, 2018, A1. Location in patent: Paragraph 0243; 0244; 0246
[4] Patent: WO2015/185207, 2015, A1. Location in patent: Page/Page column 190; 191
[5] Patent: WO2015/185208, 2015, A1. Location in patent: Page/Page column 147; 148
