二硝酸亜鉛 化学特性,用途語,生産方法
種類
硝酸亜鉛は、一般的には主に六水和物として販売されています。研究開発用試薬製品や、産業用薬品として販売されている物質です。
1. 研究開発用試薬製品
研究開発用試薬製品としては、10g、25g 、500gなど、実験室で取り扱いやすい容量で提供されています。冷蔵保管が必要な製品として取り扱われることの多い物質です。
試薬製品独自の用途としては、プラズマ発光分光分析法及び原子吸光分光分析法により共存する不純物金属イオンを定量するのに用いられることがあります。
2. 産業用薬品
産業用薬品としては、20kgPE袋や、25kg紙袋など、比較的大型の容量で提供されています。結晶状態のほか、溶液で提供しているメーカーも存在します。分析試薬、金属表面処理剤、樹脂加工触媒、媒染剤をはじめとする多くの用途があるため、複数のメーカーから販売されている物質です。
解説
硝酸亜鉛 (英: Zinc nitrate) とは、の硝酸塩で、組成式Zn(NO3)2 で表される無機化合物です。
通常、無水物より六水和物Zn(NO3)2 ・6H2Oの状態で流通していることが多い物質です。また、四水和物Zn(NO3)2 ・4H2Oも存在します。
無水物のCAS登録番号は7779-88-6、四水和物のCAS登録番号は9154-63-3、六水和物のCAS登録番号は10196-18-6です。
用途
強力な酸化剤であり、可燃性物質や金属の硫化物、炭素、リン、硫黄、銅などの還元性物質と激しく反応する。炭酸ナトリウムとの反応により、炭酸亜鉛と硝酸ナトリウムが生成する。
合成
硝酸亜鉛の合成
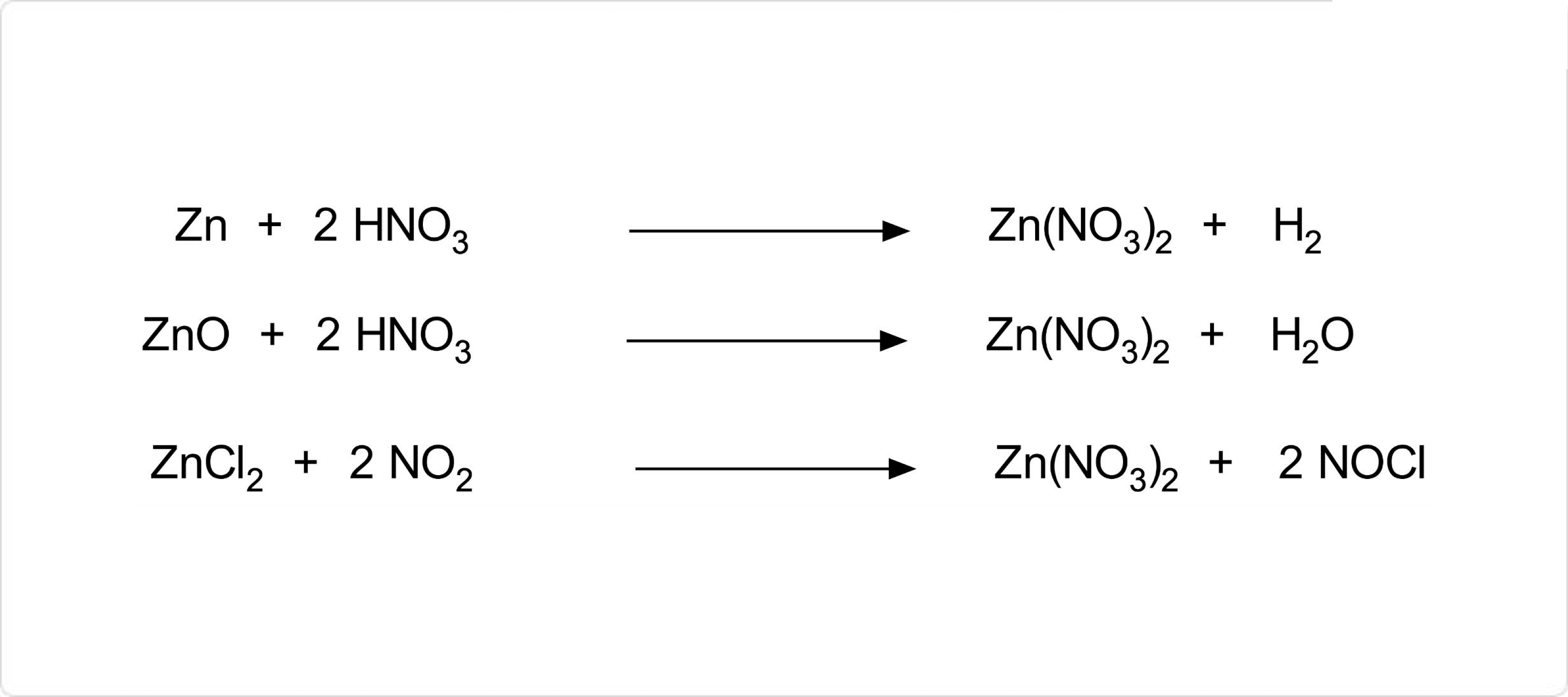
図3. 硝酸亜鉛の合成
硝酸亜鉛は、亜鉛の単体、若しくは酸化亜鉛に対して硝酸を加えることにより合成が可能です。また、硝酸亜鉛の無水物は、塩化亜鉛と二酸化窒素の反応によって得ることができます。
危険性
2. 硝酸亜鉛の危険性と法規制情報
硝酸亜鉛は、それ自体は不燃性の物質ですが、火災を助長するおそれがある酸化性物質です。加熱による危険有害な分解生成物としては、窒素酸化物や亜鉛酸化物が挙げられます。また、人体へも有害な物質であり、経口摂取によって胃痙攣やチアノーゼなどの症状が現れるとされています。
その他の有害性には、皮膚刺激や眼刺激、呼吸器への刺激のおそれなどがあります。上記の有害性から、硝酸亜鉛は、毒物および劇物取締法で劇物に指定されています。
労働安全衛生法では危険物・酸化性のものに指定されており、消防法では 第1類酸化性固体、硝酸塩類に該当する物質です。化学物質排出把握管理促進法 (PRTR法) では、第1種指定化学物質に指定されています。法令を遵守して正しく取り扱うことが必要です。
物理的性質
The hexahydrate, Zn(NO
3)
2?6H
2O, is a colorless and odorless crystalline solid; tetragonal structure; density 2.065 g/cm3 at 15°C; melts at 36.4°C; loses all its water of crystallization between 105 to 131°C; very soluble in water, about 184 g/100mL water at 20°C; the aqueous solution acidic, the pH of a 5% solution is about 5.1; also very soluble in alcohol
The trihydrate, Zn(NO
3)
2?3H
2O consists of colorless needles; melts at 45.5°C; very soluble in water, 327 g/100mL at 40°C.
一般的な説明
Zinc nitrate is a colorless crystalline solid. Noncombustible, but accelerates the burning of combustible materials. If large quantities are involved in a fire or the combustible material is finely divided, an explosion may result. Prolonged exposure to fire or heat may result in an explosion. Toxic oxides of nitrogen are produced in fires involving Zinc nitrate . Zinc nitrate is used as a catalyst in the manufacture of other chemicals, in medicine, and in dyes.
空気と水の反応
Water soluble.
反応プロフィール
Zinc nitrate is an oxidizing agent. Reacts violently with combustible and reducing materials. [Handling Chemicals Safely 1980. p. 967]; mixtures of Zinc nitrate s with alkyl esters may explode owing to the formation of alkyl nitrates; mixtures with phosphorus, tin (II) chloride, or other reducing agents may react explosively [Bretherick 1979. p. 108-109].
健康ハザード
Inhalation of dust may irritate nose and throat. Ingestion can cause irritation or corrosion of the alimentary tract. Contact with eyes causes irritation, which may be delayed. Contact with skin causes irritation.
使用用途
硝酸亜鉛の主な用途は、医薬品原料、媒染剤、樹脂加工触媒です。また、その他の用途には分析試薬、金属表面処理剤、二次電池などもあります。
硝酸亜鉛はそれ自体は不燃性の物質ですが、可燃物を燃え上がらせたり、人体への危険性が大きいので取り扱いには注意が必要です。
安全性プロファイル
A powerful oxidizer.
Can react violently with C, Cu, metal
sulfides, organic matter, P, S. When heated
to decomposition it emits toxic fumes of
NOx and ZnO. See also NITRATES and
ZINC COMPOUNDS.
二硝酸亜鉛 上流と下流の製品情報
原材料
準備製品