|
ChemicalBook Optimization Suppliers |
|
| 融点 | 88-91 °C(lit.) | | 沸点 | 256 °C(lit.) | | 比重(密度) | 1.01 g/mL at 20 °C | | 蒸気圧 | <1 mm Hg ( 20 °C) | | 屈折率 | 1.4801 | | 闪点 | 293 °F | | 貯蔵温度 | Store below +30°C. | | 溶解性 | H2O: 0.1 M at 20 °C, clear, colorless | | 外見 | crystalline | | 酸解離定数(Pka) | 6.953(at 25℃) | | 比重 | 1.03 | | 色 | white | | 臭い (Odor) | Amine like | | 酸塩基指示薬変色域(pH) | 9.5 - 11 | | PH | 9.5-11.0 (25℃, 50mg/mL in H2O) | | 水溶解度 | 633 g/L (20 ºC) | | Sensitive | Hygroscopic | | 極大吸収波長 (λmax) | λ: 260 nm Amax: 0.10
λ: 280 nm Amax: 0.10 | | Merck | 14,4912 | | BRN | 103853 | | Dielectric constant | 23.0(Ambient) | | 安定性: | Stable. Incompatible with acids, strong oxidizing agents. Protect from moisture. | | InChIKey | RAXXELZNTBOGNW-UHFFFAOYSA-N | | LogP | -0.02 at 25℃ | | CAS データベース | 288-32-4(CAS DataBase Reference) | | NISTの化学物質情報 | 1H-Imidazole(288-32-4) | | EPAの化学物質情報 | Imidazole (288-32-4) |
| | イミダゾール Usage And Synthesis |
| 外観 | 白色~わずかにうすい黄色, 結晶~結晶性粉末 | | 種類 | イミダゾール環に置換基が付いた、多種の誘導体があり、これらをイミダゾール類と呼びます。置換基が付く場所として、1位の窒素と2位、4位、5位の炭素があり、それぞれ異なる置換基を付けた誘導体の合成が可能です。また、3位の窒素も求核置換することで、カチオン化されますが、置換基をつけることが可能です。
イミダゾール類の代表的なものとして、2-メチルイミダゾール、2-エチル-4-メチルイミダゾール、2-フェニルイミダゾールなどがあり、接頭数字が環のどの部位に置換基が結合しているかを示しています。アシル化されたイミダゾールは求核反応に対して敏感であり、カルボン酸誘導体の合成に利用されます。
また、水酸基にシリルクロリドを作用させ、シリルエーテルとして保護する場合にも、イミダゾールを塩基兼触媒として使用することが一般的です。さらに、カルボニルジイミダゾール (CDI) はカルボニル化剤やアミドの縮合剤として有用です。
| | 性質 | イミダゾールは、分子式C3H4N2、分子子量68.08の白色から淡黄色のフレーク状の固体です。融点は88~92℃、沸点は256℃、引火点は145℃で昇華性があります。極性が高い溶媒にはよく溶け、水、メタノール、エタノールなどには易溶、ピリジン、クロロホルムに可溶、極性が低いエーテル、ベンゼンには難溶で、ヘキサンにはほぼ溶けません。
多くの遷移金属イオンと錯体を作り、優れた配位子として機能します。熱分解しにくく、酸化剤や還元剤に対しても比較的安定です。強い芳香族性を示し、水素原子の置換反応を受けやすいという特徴があります。
イミダゾールは、1位のプロトンが抜かれても、3位の窒素がプロトン化されても、共鳴構造を取って対称的な構造を保持します。このため、芳香族性を損なうことなく、電荷を分散させることができます。
| | 溶解性 | 水、エタノール及びアセトンに溶けやすい。 | | 解説 | イミダゾールは環内に窒素原子二つを含む複素環式化合物の一つ。1,3-ジアゾールの別名をもつ。グリオキサールにホルムアルデヒドとアンモニアを反応させると生成する。1858年にグリオキサールとアンモニアとの反応によって得られた。誘導体は1799年にすでに見いだされていた。誘導体には,ヒスタミン,ヒスチジン,ピロカルピンアルカロイドなどがある.
結晶性のよい固体で,融点91℃,沸点257℃。塩基性で,塩基解離指数pKb=7.05(25℃)で,異性体のピラゾールより強く,酸と結晶性の塩をつくる。水、エタノール(エチルアルコール)、エーテルによく溶けるほか、酸に溶けて塩を生成する。コバルト(Ⅱ)イオンと反応して青紫色の沈殿を生ずるので、コバルトの検出試薬となる。混酸(硝酸と硫酸の混合物)によりニトロ化すると4-ニトロイミダゾールを生成する。 | | 用途 | 有機合成原料。緩衝液調製。
イミダゾール化合物は、エポキシ樹脂の硬化剤、医農薬中間体、ウレタンの硬化触媒、銅の防錆剤、電解質などさまざまな工業分野に広く応用されています。最近ではイミダゾリウム塩が、グリーンソルベントとして注目されています。 | | 用途 | 医薬品?農薬の原料、エポキシ樹脂の硬化剤原料、防錆剤、電解めっき薬として使用 | | 説明 | Imidazole group denotes a heterocyclic organic compound whose molecule contains a five-membered hetero-aromatic ring of two non-adjacent nitrogen atoms, that a carbon atom is placed between two nitrogen atoms. Imidazole is the universally used trivial name for 1,3-azole. Earlier given names were glyoxaline and iminazole. The importance of this aromatic ring system is reflected by its presence in naturally occurring histidine, histamine and the purines, and in several classes of pharmaceuticals. Imidazole can act as a base and as a weak acid. It exists in two tautomeric forms with the hydrogen atom taking position between the two nitrogen atoms. | | 化学的特性 | Imidazole is a moderately strong base (pKb= 7.0), and a weak acid (pKa= 14.9). Imidazoles substituted with electron-withdrawing groups are stronger acids than imidazole itself; e.g., 4(5)-nitroimidazole has a pKa of 9.3. Imidazole is stable at 400°C, possesses considerable aromatic character, and undergoes the usual electrophilic aromatic substitution reactions. Nitration and sulfonation require, however, far more drastic conditions than the corresponding reactions with benzene. Other substitution reactions of imidazole include halogenation, hydroxymethylation, coupling with aromatic diazonium salts, and carboxylation. | | 来歴 | Imidazole[288-32-4] was first synthesized in 1858 by Debus from ammo�nia and glyoxal; it was originally named gly�oxalin. The name imidazole was introduced by Hantzsch. Industrial production of imidazole began in the 1950s; a wide range of derivatives is now available in industrial quantities. | | 使用 | Imidazole is used as a buffer in the range of pH 6.2-7.8. It is also an histamine antagonist. It acts as a chelator and forms complexes with various divalent cations. It is used as a corrosion inhibitor on certain transition metals such as copper. Its derivatives, like polybenzimidazole (PBI), act as fire retardants. It finds application in photography and electronics. Imidazole salts are used as ionic liquids and precursors to stable carbenes. Imidazole derivatives like ketoconazole, miconazole and clotrimazole are involved in the treatment of various systemic fungal infections. It is a part of the theophylline molecule, present in tea leaves and coffee beans, which stimulates the central nervous system. | | 定義 | ChEBI: Imidazole is an imidazole tautomer which has the migrating hydrogen at position 1. It is a conjugate base of an imidazolium cation. It is a conjugate acid of an imidazolide. It is a tautomer of a 4H-imidazole. It is an important pharmacophore in drug discovery. Imidazole is used as a Karl Fischer reagent in analytical chemistry and a reagent in synthetic organic chemistry. | | 主な応用 | Imidazole is a versatile heterocycle used in the preparation of various biologically active compounds such as the amino acid histidine and is present in many antifungal medication. It is also used ext ensively as a corrosion inhibitor on transition metals such as copper.It is used in organic synthesis and as an antiirradiationagent.
Imidazole has been used:
in the lysis, wash and elution buffer for the purification of histidine tagged Sonic Hedgehog(shh-N) protein.
in elution buffer in stepwise gradient for the purification of histidine tagged aldo keto reductases using nickel affinity chromatography.
as a component of homogenization buffer for the purification of phagosomal compartments from dendritic cell. | | 製造方法 | Imidazole is formed by reacting glyoxal with formaldehyde in the presence of ammonium acetate in acetic acid. The driving energy is microwave radiation. More generally, this reaction is used to produce substituted imidazoles.
Although there had been discoveries of various derivatives of imidazole in 1840, it was first reported in 1858. The synthesis process of imidazole follows the reaction between formaldehyde in ammonia and glyoxal. This process gives low yield of imidazole but it is still used to form imidazole with C-substitution (Wolkenberg et al., 2004). | | 一般的な説明 | Imidazole is a heterocyclic compound with a five-membered planar ring. It is amphoteric and highly polar. The pharmacophore of imidazole exists in bioactive compounds including amino acids, plant growth regulators and therapeutic agents. | | 健康ハザード | It is less toxic relative to pyrrole and otherfive-membered heterocyclic compounds ofnitrogen. Intraperitoneal administration ofimidazole caused somnolence, muscle contractions,and convulsions in mice. Theoral LD50 value in mice is in the range900 mg/kg. | | 火災危険 | Noncombustible solid. | | 使用用途 | イミダゾールは、工業的には化学品原料、農薬原料、医薬品などに幅広く利用されています。特に半導体封止剤やなど電子基板周辺の中でも、耐熱性が必要とされる箇所で優れた特性は発揮するため、利用される場合が多いです。
その他にも、エポキシ樹脂の硬化剤や、の発泡触媒、、ゴムの加硫促進剤、塗料、接着剤、建築材料やスポーツ用品などさまざまな工業分野で広く使われています。塩基触媒タイプの硬化剤または促進剤として、比較的少量の添加で硬化するなど、優れた保存安定性をもっているのが特徴です。
医薬品用途では、イミダゾールは抗真菌剤に、イミダゾール環に置換基が付いたイミダゾール類も抗潰瘍剤、抗高血圧剤、抗喘息剤など多くの医薬に使用されています。また、イミダゾールの窒素にアルキル付加させて4級アミンとしたイミダゾリウムカチオンを含むイミダゾリウム塩が、イオン液体という常温付近に融点を持つ中和塩となり、環境に優しい溶剤であるグリーンゾルベントとして注目されています。
| | Biochem/physiol Actions | Imidazole derivatives have antibacterial, antifungal and anticancer functionality. It interacts with DNA and also binds to protein and stops cell division. It also acts as a microtubule destabilizing agents and inhibits topoisomerase and Cytochrome P450 Family 26 Subfamily A Member 1 (CYP26A1) enzymes. Imidazole based anticancer drug find applications in cancer chemotherapy. It is used as buffer component for purification of the histidine tagged recombinant proteins in immobilized metal-affinity chromatography (IMAC). | | 作用機序 | N-substitution of imidazoles has created a family of drugs, called triazoles, that have the same mechanism of action as imidazoles, a similar or broader spectrum of activity, and less effect on human sterol synthesis. Both imidazoles and triazoles inhibit C-14α demethylation of lanosterol in fungi by binding to one of the cytochrome P-450 enzymes, which leads to the accumulation of C-14α methylsterols and reduced concentrations of ergosterol, a sterol essential for a normal fungal cytoplasmic membrane. Inhibition of cytochrome P-450 also decreases the synthesis of testosterone and glucocorticoids in mammals, an effect seen clinically with ketoconazole but not with later azoles[1]. | | 製造方法 | イミダゾール類の製造方法
イミダゾールの製造方法は、とアルデヒドとを反応させる方法、エチレンジアミンとニトリルから合成する方法があります。
1. グリオキサールから合成
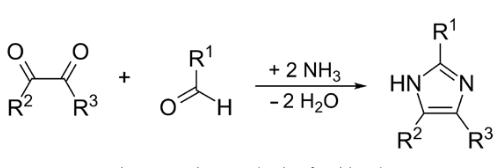
原料に使用するアルデヒド、アミンの種類により1位、2位の置換基が決まります。
OHC-CHO + R1-NH2 + R2CHO → R1R2C3H2N2 + 3H2O
2. エチレンジアミンから合成
ニトリルの置換基によって、1位、2位の置換基が決まります。
H2N-CH2CH2-NH2 + RCN → R2C3H4N2 + NH3→R2C3H2N2 + H2
参考文献
| | 純化方法 | Crystallise imidazole from *benzene, CCl4, CH2Cl2, EtOH, pet ether, acetone/pet ether and distilled de-ionized water. Dry it at 40o under vacuum over P2O5. Distil it at low pressure. It is also purified by sublimation or by zone melting. [Snyder et al. Org Synth Coll Vol III 471 1955, Bredereck et al. Chem Ber 97 827 1964, Caswell & Spiro J Am Chem Soc 108 6470 1986.] 15N-imidazole crystallises from *benzene [Scholes et al. J Am Chem Soc 108 1660 1986]. [Beilstein 23 II 34, 23 III/IV 564, 23/4 V 191.] | | 参考文献 | [1] Rex, J. and D. Stevens. “39 – Drugs Active against Fungi, Pneumocystis, and Microsporidia.” Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases 23 1 (2015): 479-494. |
|