氪、氙气体中异常杂质被确认后, 为了寻找其有效的净除方法, 从20 世纪90 年代以来, 做了如下探索试验。
2.1 .吸附法净除Kr中CF4
根据这两种气体的理化特性与分子直径的大小不同, 使用了几种不同的分子筛、在不同的温度条件下, 对Kr 中CF4 进行低温吸附。试验结果表明, 分子筛吸附剂对CF4 没有任何净除效果。
2.2 .精馏法净除Kr 中CF4
1992 年, 研制了一套小型低温填料精馏塔, 其结构、原理及操作方法与传统的Kr—Xe分离塔(三氪塔)相类似。经试验, 当Kr中CF4 含量φ(CF4)在(40~50) ×10-6之内的气体经过精馏后, 杂质净除率仅50%左右;由于塔釜的残液排放量较大, 加之塔器、管道的残留气损失, 气体损失率竟高达30%以上。由此可见, 因受当时技术等条件的限制, 这种一次精馏的方法还不能用于“黄金气体” 的纯化。
2.3 .金属吸气法净除惰性气体中的氟化物
由于碳氟间的强键结力, CF4 与C2F6 等氟化物性质特别稳定。据资料介绍:若采用热分解法,需要超过1000℃以上的高温才能让C2F6 分解;若要分解CF4 , 则要高达2000℃才可进行。而采用催化剂分解时, 其分解温度则大大降低[1]。然而, 针对需要解决的问题, 不仅要考虑将氟化物分解, 更要考虑分解后产生的新杂质气会发生二次污染。因此, 找到一种既不与惰性气体发生反应, 也不吸附或吸收惰性气体, 同时还可对氟化物的分解起催化作用, 又能及时吸附或吸收分解后的新杂质气的净化材料, 是解决该问题的关键所在。
经查阅有关资料[2] , Zr-Al16 有可能满足上述要求, 它是一种非常活泼的吸气剂, 在气体纯化领域已得到了广泛的应用。在相同的纯化温度下, 其吸气速率比纯Zr或纯Ti大几倍到几十倍, 它能吸收惰性气体中所有的活性杂质, 而惰性气体能自由通过[3] 。为了探索Zr-Al16 能否净除掉惰性气体中的氟化物,做了如下实验验证与机理分析。
2.3.1 .清除Ar 中CF4
由于氪、氙气体价格昂贵, 配制以氩气为平衡气, CF4 含量φ(CF4)为38.4 ×10-6 , 压力为13.6MPa 的钢瓶装混合气1 瓶;选用8~40目的Zr-Al16 吸气材料。还研制了一套净化实验装置,见图1 。

图1 实验装置示意图
1—样品气钢瓶 2—净化器 3—色谱仪
在不同的加热温度条件下, 将含有CF4 杂质气的钢瓶Ar气减压至0.2MPa后通入净化器, 其流量约50ml/min 。净化后的气体直接导入氦离子化色谱仪, 分析CF4 的含量。其净除效果见表1 。
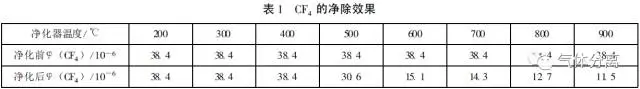
从表1 可以看出, Zr-Al16 对CF4 杂质有明显的净除效果, 工作温度在900℃时的杂质清除率可达到70%以上。但纯化后的气体中, CF4杂质气含量仍不能满足高纯气体用户的质量要求。
2.3.2 .Zr —Al16 清除CF4 的机理初探
虽然上述实验已经证明Zr-Al16对CF4 杂质有明显的清除效果, 但实验是在高温和小流量的条件下进行的, 其清除杂质的效果还不很理想, 若直接将实验装置模拟放大用于工业装置, 将不会有明显的效果。因此,有必要探讨最难分解的CF4杂质在Zr-Al16合金中被清除的机理, 进而寻求改进吸气材料的某些性能, 提高其清除杂质的能力。
武汉钢铁集团氧气公司利用图1 的实验装置, 在850℃的工作温度下, 连续向净化管内通入配制的φ(CF4) 为65.8×10-6的钢瓶氩气, 约120h,使CF4与锆铝合金充分接触。待净化管冷却至常温后, 将净化管刨开, 取出净化材料, 将未反应的净化材料和反应后的净化材料送北京某研究院分别进行X 光衍射分析与电镜扫描, 以测定合金的相组成和外表面的变化情况。反应前与反应后净化材料的测试结果如图2 、图3 所示, 反应前与反应后净化材料的电镜扫描照片如图4 、图5 所示。
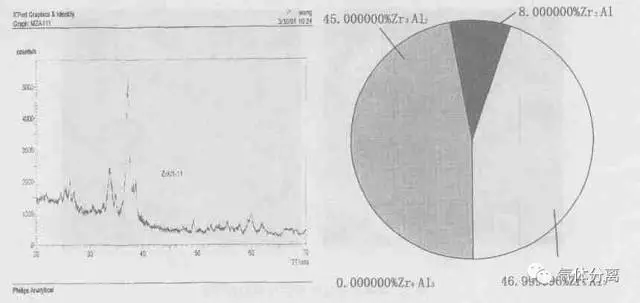
图2 反应前净化材料的X 光衍射曲线及成分含量图
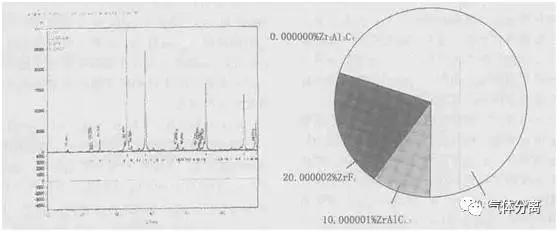
图3 反应后净化材料的X 光衍射曲线及成分含量图
从图2可看出:净除反应前, 金属化合物组成如下:ω (Zr2Al)≈8 %, ω (Zr3Al2)≈45%, ω(Zr5Al3)≈47%。
从图3可看出:净除反应后, 表面相组成为:ω(ZrAlC1.7)≈10 %, ω(ZrF4) ≈20 %, ω(ZrC)≈70 %。说明锆铝合金具有良好的吸气性能, 并生成了新的稳定的化合物。

图4 反应前净化材料的电镜扫描照片

图5 反应后净化材料的电镜扫描照片
从图4 的电镜扫描照片可看出:净除反应前,粉末颗粒状锆基合金外表面多角光亮, 从高倍放大照片上还能看到白色带状突起和暗色孔隙。这种不均匀凹凸分布的独特表面形貌不仅为金属的负载提供了大的可适用的比表面积, 而且也为催化剂活性中心的金属原子的多分散性提供了先决条件。
从图5 可看出, 净除反应后, 锆基合金粉末颗粒发生了明显变化, 高倍与低倍放大照片外表面发暗, 高倍放大照片上显示的白色带状物减少, 而出现更多不连续的多孔烧结物, 表面有新物质生成。
根据上述测试结果, 推断出如下净化机理:Ar 中的CF4 经过Zr-Al16合金粉末颗粒表面首先被吸附, 而后CF4 在合金粉末颗粒表面被催化分解;虽然CF4 的碳氟键键能很大(其热分解温度在2000℃以上), 但在Zr-Al16 吸气剂的催化作用下,它的碳氟键也会被打开, 分解为单质碳和氟原子。它们在高温作用下与活性金属锆铝发生化合反应,生成氟化锆、碳化锆和碳化锆铝等稳定的化合物。其化学反应式为:
CF4 +Zr5Al3 +Zr2Al +Zr3Al2 ※ZrF4 +ZrC +ZrAlC1.7
这种化学反应随着时间的延长, 逐步由粉末表面向内部扩散, 表面形状发生明显变化, 变成多孔状。从清除Ar 中的CF4 实验及后来的生产应用效果可以看出, 这种反应是不可逆的。由此,清除Kr或Xe中的CF4 、C2F6 和SF6等三种氟化物杂质的机理应与上述过程相同或相近。