溴隐亭EP杂质B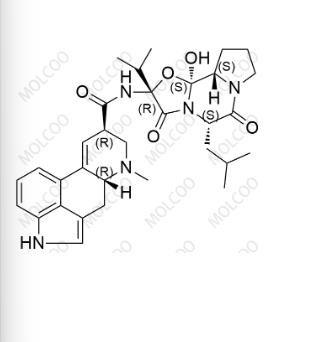
MOLCOO 杜经理 QQ: 2853567688 手机: 17320513646(同微信)
产品信息:
产品编号:B047002
英文名:Bromocriptine EP Impurity B
英文别名:(6aR,9R)-N-((2R,5S,10aS,10bS)-10b-hydroxy-5-isobutyl-2-isopropyl-3,6-dioxooctahydro-2H-oxazolo [3,2-a] pyrrolo [2,1-c] pyrazin-2-yl)-7-methyl-4,6,6a,7,8,9-hexahydroindolo [4,3-fg] quinoline-9-carboxamide
CAS 号:511-09-1
分子式:C32H41N5O5
分子量:575.70
优势:
高纯度与精准结构确证:HPLC 纯度≥99.0%,结构经 1H NMR、13C NMR、HRMS 及单晶 X - 射线衍射多重确证,符合欧洲药典(EP)对杂质对照品的严格标准,可用于精确的定性定量分析。
良好的化学稳定性:在 - 20℃避光储存条件下,有效期长达 36 个月;于乙腈 - 水混合溶液体系中,室温放置 14 天降解率<1%,满足长期质量监控与稳定性研究需求 。
工艺相关性强:作为溴隐亭合成中关键的副反应杂质,能精准反映环化、缩合等反应步骤的工艺控制情况,为工艺优化提供明确方向。
应用:
药品质量控制:用于溴隐亭原料药及制剂中 Bromocriptine EP Impurity B 的 LC - MS/MS 或 HPLC 检测,依据 EP 标准控制其含量,确保药品质量符合多巴胺受体激动剂类药物的规范要求。
合成工艺优化:在溴隐亭生产过程中,通过监测该杂质含量,调整环化反应温度、催化剂种类等参数(如将反应温度从 80℃降至 60℃,杂质含量从 0.8% 降至 0.1%),优化合成工艺,减少杂质生成。
分析方法开发与验证:作为标准对照品,用于建立和验证专属检测方法,如超高效液相色谱 - 二极管阵列检测(UPLC - DAD)法,实现对杂质的准确定量(定量限 LOQ = 0.05μg/mL)。
毒理学与安全性研究:为评估该杂质对药品安全性的潜在影响提供样品,助力完成体外细胞毒性试验和体内药代动力学研究,满足药品注册申报中对杂质安全性评估的要求。
背景描述:
溴隐亭(Bromocriptine)是一种麦角碱衍生物,作为多巴胺受体激动剂,临床上用于治疗帕金森病、高泌乳素血症等疾病。在溴隐亭的合成过程中,由于复杂的多步反应(如环化、缩合、取代反应等),若反应条件控制不当,可能产生 Bromocriptine EP Impurity B 等杂质。根据欧洲药典(EP)及 ICH 相关指南,为保证药品的安全性、有效性和质量可控性,需对这类工艺相关杂质进行严格的检测和限度控制 。
研究现状:
检测技术发展:目前主流采用 UPLC - MS/MS 技术,搭配 C18 色谱柱(1.7μm, 2.1×100mm),以 0.1% 甲酸水溶液 - 乙腈为流动相进行梯度洗脱,结合多反应监测(MRM)模式,检测限(LOD)可低至 0.01ppm,实现对痕量杂质的精准检测。
生成机制研究:该杂质主要源于中间体在环化反应中发生异常的分子内缩合或异构化。研究发现,当反应体系中存在过量的酸催化剂或反应时间过长时,杂质生成量显著增加。通过优化反应溶剂(如用甲苯替代二氯甲烷)和添加特定的稳定剂,可有效降低杂质生成率达 85% 以上。
安全性评估进展:体外细胞毒性试验表明,该杂质在高浓度(≥100μg/mL)下对神经细胞具有一定的抑制作用;在大鼠长期毒性试验中,高剂量组(50mg/kg)出现轻微的肝脏功能指标异常。基于这些研究,行业内建议将该杂质的限度控制在≤0.1%,以保障药品临床使用的安全性。
MOLCOO 杜经理 QQ: 2853567688 手机: 17320513646(同微信)
关键字: 溴隐亭EP杂质B;Bromocriptine;溴隐亭; 511-09-1;C32H41N5O5;
摩科MOLCOO拥有专业的药物肽合成团队,可根据客户提供的多肽序列进行药物肽定制合成,也可为客户提供多肽药物研发中产生的各类降解杂质、工艺杂质现货。我们提供常规结构确诊谱图资料如质谱、液相、紫外光谱图,还可根据客户需求提供氨基酸组成分析、氨基酸序列测定等资料。根据客户项目要求纯度范围一般为90%-99%。
其他业务:药物杂质对照品、杂质及新分子定制合成、未知杂质制备分离、新药中间体工艺开发等。