果糖
| 中文名称 | 果糖 |
|---|---|
| 中文同义词 | 果哌喃糖;果糖;左旋糖;果糖 HPLC;beta-D-果糖;FRUCTOSE 果糖;左旋糖(D-果糖);恩格列净杂质69 |
| 英文名称 | beta-D-Fructopyranose |
| 英文同义词 | beta-D-fructopyranose;FRUCTOSE HPLC;Fructosteril;Frutabs;Laevoral;Levungen;(2R,3S,4R,5R)-2-methyloltetrahydropyran-2,3,4,5-tetrol;FRUCTOPYRANOSE,BETA-D- |
| CAS号 | 7660-25-5 |
| 分子式 | C6H12O6 |
| 分子量 | 180.16 |
| EINECS号 | 200-333-3 |
| 相关类别 | 植提标准品;小分子抑制剂;对照品;食品添加剂;小分子抑制剂,天然产物;中药对照品;标准品;植物提取物;甜味剂;药用辅料;分析试剂标准品;化工产品-无机化工;杂质对照品;原料药API;标准品-中药标准品;chemical reagent;pharmaceutical intermediate;phytochemical;reference standards from Chinese medicinal herbs (TCM).;standardized herbal extract;Inhibitors;其他原料;标准品-对照品;化工材料;食品添加剂糖类;医药、农药及染料中间体;通用生化试剂-糖类;有机化工原料 |
| Mol文件 | 7660-25-5.mol |
| 结构式 | 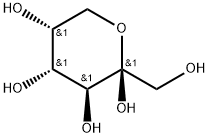 |
果糖 性质
| 熔点 | 103°C |
|---|---|
| 沸点 | 232.96°C (rough estimate) |
| 密度 | 1.6000 |
| 折射率 | 1.6170 (estimate) |
| 酸度系数(pKa) | 11.52±0.70(Predicted) |
| CAS 数据库 | 7660-25-5 |
| NIST化学物质信息 | Fructose(7660-25-5) |
美国从六十年代起研制生产果葡搪浆,并在其他一些国家得到很快发展。我 国于1976年开始生产。果糖为水果和蜂蜜中的主要糖分,是所有天然甜味剂中最甜的,并能与所有非营养型甜味剂协同增加甜味。广义果糖包括工业生产的三种液体产品:一代果糖(F-42)、二代果糖又称高果糖浆(F-55)、三代果糖又称高纯果糖(F-90)和结晶果糖。
果糖是自然界存在的最甜的单糖,其甜度大约为蔗糖的1.2~1.8倍,葡萄糖的3倍。在自然界,很多水果中都含有果糖,果糖不仅不掩盖其他风味,同时还具有增强其他风味的作用。由于果糖具有甜度高、营养价值好等功能特性,近年来在食品和医疗行业中得到了广泛的应用,是近几十年来世界上发展最快的甜味剂之一。果糖的生产和应用被认为是食品工业上的革命。食品中添加果糖能够减少所需的蔗糖、酸味剂和香精。这无疑是降低热量的经济方法。随着对其风味强化、甜味强化、高保湿性、低水活性、可强化焦化反应、高渗透压、降低凝冻温度、快速强化成胶等功能特性应用研究的不断深人,使其应用领域愈加宽广。
果糖是五羟基己酮糖,其游离状态常与果汁、蜂蜜或植物腺体花蜜中的葡萄糖和蔗糖共存。与葡萄糖是同分异构体,分子中的羰基是酮。在水溶液中加入溴水等弱氧化剂不能使它氧化。用强氧化剂(如硝酸)氧化则发生碳链断裂,得低级二元酸的混合物,据此证明羰基为酮。在不同条件下结晶可获得β-型结晶(熔点102~104℃,比旋光度-132.7°)和α-型结晶(比旋光度-63.6°)。它们的水溶液都会发生变旋现象,最终平衡时的比旋光度为 -92.2°。由此可推知,它在水溶液中链状结构和环状结构处于平衡状态。X-射线分析表明,其环状结构除六元环外还以五元环形式存在,并且两种环都存在有α-型和β-型结晶,在水溶液中处于动态平衡状态。果糖不能被溴水氧化,却能与多伦试剂和斐林试剂反应,和苯肼作用生成与葡萄糖相同的脎。因这些反应都在碱性水溶液中进行,发生酮式和烯醇式的互变异构,其中烯醇式结构比较活泼,具有还原性,能发生上述反应。工业上大规模生产果糖的最丰富原料是蔗糖。果糖比葡萄糖更易溶于水,味更甜。若以蔗糖的甜度为100,果糖的甜度是173.3,葡萄糖为74.3。
目前全世界产量已达数百万吨,成为制糖工业的重要产品。食品工业中大量采用果糖作为甜食品的调味剂。它也能为糖尿病患者及实质性肝病患者所用。医学上利用果糖在同等甜度下热量比蔗糖少,进入血液后不会导致血糖浓度迅速增加的特性,也可用于糖尿病人补充糖分。本品为无色结晶或白色结晶性粉末或颗粒性粉末,无臭,味极甜。易溶于水,溶于乙醇、甲醇,几乎不溶于氯仿和乙醚。水溶液近中性,5.50%水溶液为等渗液。
在果糖溶液中,果糖分子是以五元环状(呋喃式)或六元环状(吡喃式)半缩醛式和开链式的平衡混和物存在,如下图所示:
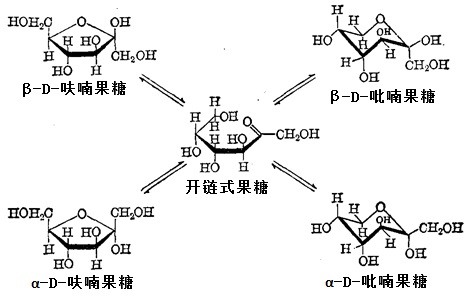
D-果糖分子中没有醛基,但酮羰基的邻位有羟基存在,这种α-羟基酮类化合物也具有较强的还原性,可以发生银镜反应,也能与斐林试剂、本尼地试剂反应产生红色沉淀。果糖在发生以上反应时,分子中的碳链发生断裂。
D-葡萄糖能被溴水或次溴酸钠氧化,而D-果糖则不反应。此性质可用于鉴别葡萄糖和果糖。果糖水溶液加间苯二酚的稀盐酸溶液显示红色,也可用于葡萄糖与果糖的鉴别。
D-果糖和苯肼反应形成脎,与D-葡萄糖、D-甘露糖形成的脎相同。
游离的D-果糖存在于水果与蜂蜜中。蔗糖、棉子糖等低聚糖中含有D-果糖。菊科植物根部含有一种叫菊粉的多糖,是D-果糖的高聚体。1.低热值特性 在天然食糖中,果糖是最甜的糖,具有清爽绵长的甜味,甜度为蔗糖的1. 2~ 1. 8倍。另外,在果糖的应用过程中,温度、pH和浓度都会影响果糖的甜度, 其中温度的影响最明显, 温度越低,甜度越高。因此,利用果糖的高甜度特性已经生产出多种低热值食品。
2.风味增强性和亲和性 果糖的甜味峰值出现在其他成分风味峰值之前,因而不会掩盖其他风味,而且还具有增强其他风味的作用。由于果糖大量存在于天然水果中,与果品中的其他成分具有很强的风味亲和性。在果汁饮料中使用果糖不但增加了果汁饮料的甜度,改善了风味,而且还具有抑制果汁香气的逸出,保持果汁固有香味的作用。因此,果糖已被使用在高档果汁饮料中。
3.焙烤和保水特性 在焙烤食品中,淀粉和甜味剂通常作为主要原料同时使用,而甜味剂的种类对于淀粉的糊化温度影响很大。研究发现甜味剂的碳链越长,糊化温度越高。果糖作为单糖,碳链短,糊化温度低。同时,在焙烤食品中,酵母利用果糖比蔗糖快,发酵性能好。所以,果糖被广泛用于焙烤食品中。在焙烤过程中果糖易发生焦糖化反应,生成的焦糖具有焙烤食品特有的风味。另外,由于果糖的水分活度相对于其他甜味剂要低,所以果糖是最有效的降低食品水分活度的甜味剂之一。利用果糖的保水性高的特点,加工的面包、蛋糕等焙烤食品久贮不干,数天后仍然质地松软。
4.抗冻性 由于果糖的冰点比其他甜味剂低,所以,在所有营养型甜味剂中,果糖的抗冻性比其他甜味剂要好。利用果糖的这种特性,在冰冻食品(如雪糕、冰淇淋)的制造过程中,添加果糖可较好的预防冰冻食品的结冰,使产品质地松软,组织细腻。
5.防腐特性 果糖的渗透压较高,能有效抑制细菌的生长繁殖,防腐性较好。因此,在糖果制造过程中使用果糖可较好的预防龋齿。1.以菊芋为原料,水解,可制得果糖。
2.用稀酸或转化酶水解蔗糖,加入氢氧化钙,与生成的果糖生成复合物沉淀,分离后,通入二氧化碳,生成碳酸钙沉淀,游离出果糖,过滤后,浓缩,可制得果糖结晶。
3.以葡萄糖为原料,以葡萄糖异构酶为催化剂,使葡萄糖异构化,生成转化糖,其中含42% 的果糖及58%的葡萄糖,仿照②法,使二者分离。
4.利用蔗糖发酵制葡聚糖剩下的废醪,经过滤后,经蒸馏回收乙醇,釜残液加入活性炭,过滤后,滤液经离子交换,可制得果糖。果糖为葡萄糖的左旋同分异构体,其作用基本上葡萄糖相似。具有直接供给能量、营养和补充体液作用。从血液中转移及转化成肝糖原等较葡萄糖快,并能在无胰岛素情况下合成糖原,故较易被利用。此外,果糖还可循酵解-氧化途径生成α-磷酸甘油和乙酰辅酶A,从而合成脂肪。果糖在体内的代谢强度仅受果糖浓度调节,故多食果糖(如含蔗糖的甜食,蔗糖为二糖,水解后得葡萄糖和果糖)容易合成较多的脂肪而发生高甘油三酯血症。果糖尚能使肝脏血流量增加30%,氧摄取量增加60%,因而可使乙醇的代谢灭活明显加快,血液廓清率成倍提高,而乳酸与丙酮酸的产生则减少60%。口服从胃肠道吸收较葡萄糖缓慢,但代谢却较快,主要在肝脏中代谢、转化为磷酸甘油和一部分葡萄糖,对血糖浓度影响很少。
果糖具有以下代谢特点:1)果糖主要在肝、肾和小肠中经果糖激酶催化生成 1-磷酸果糖;2)1-磷酸果糖在体内 1-磷酸果糖醛缩酶的催化下,生成磷酸二羟丙酮和甘油醛,甘油醛可通过甘油醛激酶的磷酸化而生成 3-磷酸甘油醛,该产物与磷酸二羟丙酮经糖酵解途径氧化分解或经糖元异生可转化为葡萄糖或合成糖元;而葡萄糖在肝脏内进入“Cori循环”(葡萄糖→肝糖元→血糖→肌糖元→血乳酸→肝糖元)。但葡萄糖和糖元不能逆向转化为果 糖;3)因果糖可绕过糖酵解中的限速酶(磷酸果糖激酶 ),在肝脏中果糖的分解速度快于葡萄糖;4)果糖代谢强度取决于果糖浓度,不受胰岛素的影响。
由于果糖的代谢特点,身体正常的人仅有极少量葡萄糖从肝脏释放出来,因此人体摄入果糖不会引起摄入葡萄糖和蔗糖容易引起的严重的饭后血糖高峰和低血糖等症状。不同温度(℃)时每100毫升水中的溶解克数:
375g/20℃;538g/40℃1. 循环和呼吸系统:过量输入可引起水肿,包括周围水肿和肺水肿。
2. 内分泌和代谢系统:滴速过快(每小时≥1g/kg)可引起乳酸性酸中毒、高尿酸血症以及脂代谢异常。
3. 电解质紊乱:稀释性低钾血症。
4. 胃肠道反应:偶有上腹部不适、疼痛或痉挛性疼痛。
5. 偶有发热、荨麻疹。
6. 局部不良反应包括注射部位感染、血栓性静脉炎等。。1. 肾功能不全、有酸中毒倾向以及高尿酸血症患者慎用。
2. 本品过量使用可引起严重的酸中毒,故不推荐肠外营养中替代葡萄糖。
3. 使用过程中应监测临床和实验室指标以评价体液平衡、电解质浓度和酸碱平衡。
4. 慎用于预防水过多和电解质紊乱。
5. 过量输注无钾果糖可引起低钾血症。本品不用于纠正高钾血症。
6. 本品能加剧甲醇氧化成甲醛,故本品不得用于甲醇中毒治疗。
7. 本品注射速度宜缓慢,以不超过每小时0.5g/kg为宜。
有关果糖的自然界存在的最甜的单糖、理化性质、制备方法、不良反应、禁忌、用途等是由Chemicalbook的旭艳编辑整理。(2016-04-20)遗传性果糖不耐受症、痛风和高尿酸血症患者禁用。1. 注射剂的稀释剂。
2. 用于烧创伤、术后及感染等胰岛素抵抗状态下或不适宜使用葡萄糖时需补充水分或能量的患者的补液治疗。
果糖是自然界存在的最甜的单糖,其甜度大约为蔗糖的1.2~1.8倍,葡萄糖的3倍。在自然界,很多水果中都含有果糖,果糖不仅不掩盖其他风味,同时还具有增强其他风味的作用。由于果糖具有甜度高、营养价值好等功能特性,近年来在食品和医疗行业中得到了广泛的应用,是近几十年来世界上发展最快的甜味剂之一。果糖的生产和应用被认为是食品工业上的革命。食品中添加果糖能够减少所需的蔗糖、酸味剂和香精。这无疑是降低热量的经济方法。随着对其风味强化、甜味强化、高保湿性、低水活性、可强化焦化反应、高渗透压、降低凝冻温度、快速强化成胶等功能特性应用研究的不断深人,使其应用领域愈加宽广。
果糖是五羟基己酮糖,其游离状态常与果汁、蜂蜜或植物腺体花蜜中的葡萄糖和蔗糖共存。与葡萄糖是同分异构体,分子中的羰基是酮。在水溶液中加入溴水等弱氧化剂不能使它氧化。用强氧化剂(如硝酸)氧化则发生碳链断裂,得低级二元酸的混合物,据此证明羰基为酮。在不同条件下结晶可获得β-型结晶(熔点102~104℃,比旋光度-132.7°)和α-型结晶(比旋光度-63.6°)。它们的水溶液都会发生变旋现象,最终平衡时的比旋光度为 -92.2°。由此可推知,它在水溶液中链状结构和环状结构处于平衡状态。X-射线分析表明,其环状结构除六元环外还以五元环形式存在,并且两种环都存在有α-型和β-型结晶,在水溶液中处于动态平衡状态。果糖不能被溴水氧化,却能与多伦试剂和斐林试剂反应,和苯肼作用生成与葡萄糖相同的脎。因这些反应都在碱性水溶液中进行,发生酮式和烯醇式的互变异构,其中烯醇式结构比较活泼,具有还原性,能发生上述反应。工业上大规模生产果糖的最丰富原料是蔗糖。果糖比葡萄糖更易溶于水,味更甜。若以蔗糖的甜度为100,果糖的甜度是173.3,葡萄糖为74.3。
目前全世界产量已达数百万吨,成为制糖工业的重要产品。食品工业中大量采用果糖作为甜食品的调味剂。它也能为糖尿病患者及实质性肝病患者所用。医学上利用果糖在同等甜度下热量比蔗糖少,进入血液后不会导致血糖浓度迅速增加的特性,也可用于糖尿病人补充糖分。本品为无色结晶或白色结晶性粉末或颗粒性粉末,无臭,味极甜。易溶于水,溶于乙醇、甲醇,几乎不溶于氯仿和乙醚。水溶液近中性,5.50%水溶液为等渗液。
在果糖溶液中,果糖分子是以五元环状(呋喃式)或六元环状(吡喃式)半缩醛式和开链式的平衡混和物存在,如下图所示:

D-果糖分子中没有醛基,但酮羰基的邻位有羟基存在,这种α-羟基酮类化合物也具有较强的还原性,可以发生银镜反应,也能与斐林试剂、本尼地试剂反应产生红色沉淀。果糖在发生以上反应时,分子中的碳链发生断裂。
D-葡萄糖能被溴水或次溴酸钠氧化,而D-果糖则不反应。此性质可用于鉴别葡萄糖和果糖。果糖水溶液加间苯二酚的稀盐酸溶液显示红色,也可用于葡萄糖与果糖的鉴别。
D-果糖和苯肼反应形成脎,与D-葡萄糖、D-甘露糖形成的脎相同。
游离的D-果糖存在于水果与蜂蜜中。蔗糖、棉子糖等低聚糖中含有D-果糖。菊科植物根部含有一种叫菊粉的多糖,是D-果糖的高聚体。1.低热值特性 在天然食糖中,果糖是最甜的糖,具有清爽绵长的甜味,甜度为蔗糖的1. 2~ 1. 8倍。另外,在果糖的应用过程中,温度、pH和浓度都会影响果糖的甜度, 其中温度的影响最明显, 温度越低,甜度越高。因此,利用果糖的高甜度特性已经生产出多种低热值食品。
2.风味增强性和亲和性 果糖的甜味峰值出现在其他成分风味峰值之前,因而不会掩盖其他风味,而且还具有增强其他风味的作用。由于果糖大量存在于天然水果中,与果品中的其他成分具有很强的风味亲和性。在果汁饮料中使用果糖不但增加了果汁饮料的甜度,改善了风味,而且还具有抑制果汁香气的逸出,保持果汁固有香味的作用。因此,果糖已被使用在高档果汁饮料中。
3.焙烤和保水特性 在焙烤食品中,淀粉和甜味剂通常作为主要原料同时使用,而甜味剂的种类对于淀粉的糊化温度影响很大。研究发现甜味剂的碳链越长,糊化温度越高。果糖作为单糖,碳链短,糊化温度低。同时,在焙烤食品中,酵母利用果糖比蔗糖快,发酵性能好。所以,果糖被广泛用于焙烤食品中。在焙烤过程中果糖易发生焦糖化反应,生成的焦糖具有焙烤食品特有的风味。另外,由于果糖的水分活度相对于其他甜味剂要低,所以果糖是最有效的降低食品水分活度的甜味剂之一。利用果糖的保水性高的特点,加工的面包、蛋糕等焙烤食品久贮不干,数天后仍然质地松软。
4.抗冻性 由于果糖的冰点比其他甜味剂低,所以,在所有营养型甜味剂中,果糖的抗冻性比其他甜味剂要好。利用果糖的这种特性,在冰冻食品(如雪糕、冰淇淋)的制造过程中,添加果糖可较好的预防冰冻食品的结冰,使产品质地松软,组织细腻。
5.防腐特性 果糖的渗透压较高,能有效抑制细菌的生长繁殖,防腐性较好。因此,在糖果制造过程中使用果糖可较好的预防龋齿。1.以菊芋为原料,水解,可制得果糖。
2.用稀酸或转化酶水解蔗糖,加入氢氧化钙,与生成的果糖生成复合物沉淀,分离后,通入二氧化碳,生成碳酸钙沉淀,游离出果糖,过滤后,浓缩,可制得果糖结晶。
3.以葡萄糖为原料,以葡萄糖异构酶为催化剂,使葡萄糖异构化,生成转化糖,其中含42% 的果糖及58%的葡萄糖,仿照②法,使二者分离。
4.利用蔗糖发酵制葡聚糖剩下的废醪,经过滤后,经蒸馏回收乙醇,釜残液加入活性炭,过滤后,滤液经离子交换,可制得果糖。果糖为葡萄糖的左旋同分异构体,其作用基本上葡萄糖相似。具有直接供给能量、营养和补充体液作用。从血液中转移及转化成肝糖原等较葡萄糖快,并能在无胰岛素情况下合成糖原,故较易被利用。此外,果糖还可循酵解-氧化途径生成α-磷酸甘油和乙酰辅酶A,从而合成脂肪。果糖在体内的代谢强度仅受果糖浓度调节,故多食果糖(如含蔗糖的甜食,蔗糖为二糖,水解后得葡萄糖和果糖)容易合成较多的脂肪而发生高甘油三酯血症。果糖尚能使肝脏血流量增加30%,氧摄取量增加60%,因而可使乙醇的代谢灭活明显加快,血液廓清率成倍提高,而乳酸与丙酮酸的产生则减少60%。口服从胃肠道吸收较葡萄糖缓慢,但代谢却较快,主要在肝脏中代谢、转化为磷酸甘油和一部分葡萄糖,对血糖浓度影响很少。
果糖具有以下代谢特点:1)果糖主要在肝、肾和小肠中经果糖激酶催化生成 1-磷酸果糖;2)1-磷酸果糖在体内 1-磷酸果糖醛缩酶的催化下,生成磷酸二羟丙酮和甘油醛,甘油醛可通过甘油醛激酶的磷酸化而生成 3-磷酸甘油醛,该产物与磷酸二羟丙酮经糖酵解途径氧化分解或经糖元异生可转化为葡萄糖或合成糖元;而葡萄糖在肝脏内进入“Cori循环”(葡萄糖→肝糖元→血糖→肌糖元→血乳酸→肝糖元)。但葡萄糖和糖元不能逆向转化为果 糖;3)因果糖可绕过糖酵解中的限速酶(磷酸果糖激酶 ),在肝脏中果糖的分解速度快于葡萄糖;4)果糖代谢强度取决于果糖浓度,不受胰岛素的影响。
由于果糖的代谢特点,身体正常的人仅有极少量葡萄糖从肝脏释放出来,因此人体摄入果糖不会引起摄入葡萄糖和蔗糖容易引起的严重的饭后血糖高峰和低血糖等症状。不同温度(℃)时每100毫升水中的溶解克数:
375g/20℃;538g/40℃1. 循环和呼吸系统:过量输入可引起水肿,包括周围水肿和肺水肿。
2. 内分泌和代谢系统:滴速过快(每小时≥1g/kg)可引起乳酸性酸中毒、高尿酸血症以及脂代谢异常。
3. 电解质紊乱:稀释性低钾血症。
4. 胃肠道反应:偶有上腹部不适、疼痛或痉挛性疼痛。
5. 偶有发热、荨麻疹。
6. 局部不良反应包括注射部位感染、血栓性静脉炎等。。1. 肾功能不全、有酸中毒倾向以及高尿酸血症患者慎用。
2. 本品过量使用可引起严重的酸中毒,故不推荐肠外营养中替代葡萄糖。
3. 使用过程中应监测临床和实验室指标以评价体液平衡、电解质浓度和酸碱平衡。
4. 慎用于预防水过多和电解质紊乱。
5. 过量输注无钾果糖可引起低钾血症。本品不用于纠正高钾血症。
6. 本品能加剧甲醇氧化成甲醛,故本品不得用于甲醇中毒治疗。
7. 本品注射速度宜缓慢,以不超过每小时0.5g/kg为宜。
有关果糖的自然界存在的最甜的单糖、理化性质、制备方法、不良反应、禁忌、用途等是由Chemicalbook的旭艳编辑整理。(2016-04-20)遗传性果糖不耐受症、痛风和高尿酸血症患者禁用。1. 注射剂的稀释剂。
2. 用于烧创伤、术后及感染等胰岛素抵抗状态下或不适宜使用葡萄糖时需补充水分或能量的患者的补液治疗。
安全信息
果糖 化学药品说明书
| 更新日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
|---|---|---|---|---|---|
| 2024/01/16 | XW766025501 | 果糖 | 7660-25-5 | 25G | 52元 |
