444731-52-6
中文名称
帕唑帕尼
英文名称
Pazopanib
CAS
444731-52-6
分子式
C21H23N7O2S
MDL 编号
MFCD11616589
分子量
437.52
MOL 文件
444731-52-6.mol
更新日期
2024/04/29 11:00:11
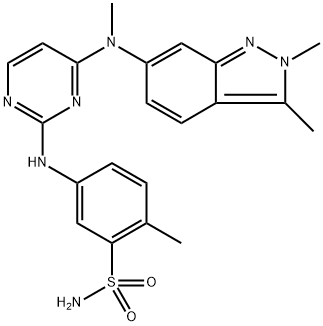 444731-52-6 结构式
444731-52-6 结构式
基本信息
中文别名
帕唑帕尼帕唑帕尼碱
帕唑帕尼游离碱
VEGFR抑制剂
帕唑帕尼 25MG
盐酸帕唑帕尼及中间体
GW786034
VOTRIENT
VOTRIENTPAZOPANIBGW786034 帕唑帕尼
5-[[4-[(2,3-二甲基-2H-吲唑-6-基)(甲基)氨基]嘧啶-2-基]氨基]-2-甲基苯磺酰胺
帕唑帕尼 [5-[[4-[(2,3-二甲基-2H-吲唑-6-基)(甲基)氨基]嘧啶-2-基]氨基]-2-甲基苯磺酰胺]
英文别名
VotrientPazopanib
Pazopanib base
Pazopanib, >=99%
Pazopanib(GW786034)
Votrient(pazopanib)
Pazopanib for research
5-[4-[(2,3-Dimethyl-2H-indazol-6-yl)-methyl-amino]-pyrimidin-2-ylamino]-2-methyl-benzenesulfon
5-[[4-[(2,3-DiMethyl-2H-indazol-6-yl)MethylaMino]-2-pyriMidinyl]aMino]-2-Methyl-benzenesulfonaMide
5-[[4-[(2,3-Dimethyl-2H-indazol-6-yl)(methyl)amino]pyrimidin-2-yl]amino]-2-methylbenzenesulfonamide
物理化学性质
熔点285-289°C (dec.)
沸点728.8±70.0 °C(Predicted)
密度1.40
闪点359℃
储存条件Refrigerator
溶解度可溶于酸水溶液(轻微)、DMSO(轻微、加热)、甲醇(轻微、加热)
酸度系数(pKa)10.19±0.60(Predicted)
形态黄色粉末
颜色白色至米色
常见问题列表
产品描述
帕唑帕尼是由葛兰素史克公司研发的一种可干扰顽固肿瘤存活和生长所需的新血管生成的新型口服血管生成抑制剂,靶向作用于血管内皮生长因子受体(VEGFR),通过抑制对肿瘤供血的新血管生成而起作用。适用于晚期肾细胞癌(一种在肾小管中发现癌细胞的肾癌类型)、软组织肉瘤(STS)、上皮性卵巢癌和非小细胞肺癌(NSCLC)的治疗。美国明尼苏达州罗彻斯特市梅奥临床研究中心临床研究显示帕唑帕尼(商品名Votrient)也能有效治甲状腺癌,能使一半患者的肿瘤体积缩小,较常用药物更能长时间稳定病情,可以维持相当长一段时间的治疗效果,是目前为止治疗甲状腺癌应答率最高的药物。

美国食品药品监督管理局(FDA)于2009年10月19日批准帕唑帕尼(商品名Votrient)上市,是自2005年以来第六个获批治疗肾癌的药物。2009年,大约有49,000名患者被诊断为肾细胞癌,有11,000名患者死于该病。
2010年6月15日,帕唑帕尼(商品名pazopanib)获得欧盟有条件批准用于晚期肾细胞癌的一线治疗及先前接受过细胞因子治疗的患者。一旦欧盟委员会给予此药最终上市授权,葛兰素史克公司便可拥有帕唑帕尼十年的独家销售权。
适应症
帕唑帕尼是一种口服的多靶点酪氨酸激酶抑制剂,能够阻断包括VEGFR1-3、PDGFR-α、PDGFR-β和c-KIT在内的多种受体,其作用机制与索拉非尼和舒尼替尼十分相似。2009年10月FDA正式批准帕唑帕尼用于晚期肾癌的一线治疗药物,随着诺华收购葛兰素史克抗肿瘤药物部门,现在由诺华负责上市销售。帕唑帕尼适应症:1.FDA批准用于晚期肾癌患者。
2.FDA批准用于之前接受化疗的晚期软组织肉瘤(STS)患者。
但对脂肪性STS或胃间质肿瘤疗效尚未确定。
治疗软组织肉瘤试验数据:在III期临床试验(EORTC62072),368例既往蒽环类为基础的化疗治疗失败的转移性的非脂肪性STS患者分别接受帕唑替尼或安慰剂治疗,PFS显著增高,4.6:1.6月。
治疗晚期肾透明细胞癌的疗效
为了探讨抑制血管生成的分子靶向药物酪氨酸激酶抑制剂帕唑帕尼治疗晚期肾透明细胞癌的疗效。解放军总院2006年6月至2007年5月参与的帕唑帕尼治疗晚期肾透明细胞癌随机临床药物试验的门诊病例14例,分为帕唑帕尼组(10例)和安慰剂组(4例),分别接受帕唑帕尼800mg/d和安慰剂,持续治疗12周后,根据服药前后的CT检查结果判定疗效。结果显示,帕唑帕尼组和安慰剂组患者可测量病灶的平均缩小比值分别为27.6%、-2.8%(P〈O.05);帕唑帕尼组和安慰剂组的疾病控制率分别为100%和25%。结论证实分子靶向血管生成抑制药酪氨酸激酶抑制剂帕唑帕尼能够在短期内对转移性肾透明细胞癌具有明显的治疗效果且安全性较高。
一项三期临床研究显示,与安慰剂相比,帕唑帕尼使肿瘤进展或死亡的风险降低54%。总的来看,本品组患者的疾病无进展生存期(PFS)存活时间平均为9.2个月,安慰剂组为4.2个月。在先前未接受过治疗的患者中,本品组存活时间平均为11.1个月,安慰剂组为2.8个月;在先前接受过细胞因子治疗的患者中,帕唑帕尼组存活时间平均为7.4个月,安慰剂组为4.2个月。
不良反应
腹泻、高血压、毛发颜色改变、恶心、食欲不振、呕吐、疲劳、虚弱、腹痛及头痛等。引起严重的肝脏问题,因此医护人员应在患者使用该药物治疗前和治疗期间对患者进行血液检验,监测患者肝功能
对胎儿有危害,妊娠期应禁用此药。
帕唑帕尼还可导致心律不齐,患者在用药期间应定期做心电图测量心率,并定期进行血液检验监测电解质水平,因为电解质失衡也会也起心律不齐。
生物活性
Pazopanib (GW786034) 是一种新型多靶点的VEGFR1,VEGFR2,VEGFR3,PDGFR,FGFR,c-Kit 和 c-Fms/CSF1R抑制剂,无细胞试验中IC50分别为10 nM,30 nM,47 nM,84 nM,74 nM,140 nM 和 146 nM。Pazopanib 可诱导 cathepsin B 的活化和自噬。靶点
| Target | Value |
|
VEGFR1
(Cell-free assay) | 10 nM |
|
VEGFR2
(Cell-free assay) | 30 nM |
|
VEGFR3
(Cell-free assay) | 47 nM |
|
c-Kit
(Cell-free assay) | 74 nM |
|
PDGFR
(Cell-free assay) | 84 nM |
体外研究
Pazopanib有效抑制VEGF诱导的HUVEC 细胞中VEGFR2磷酸化作用,IC50为8 nM。在所有滑膜肉瘤细胞系,包括SYO-1和HS-SY-II细胞中,Pazopanib表现出剂量依赖性生长抑制作用。SYO-1和HS-SY-II细胞的增殖在1微克/毫升的Pazopanib下被抑制,在5微克/毫升的Pazopanib下被完全废止。Pazopanib引起G1期阻滞,并且因此抑制滑膜肉瘤细胞的生长。与载体处理的细胞相比,Akts,GSK-3β,JNKs,p70 S6 激酶,和mTOR的磷酸化作用在Pazopanib处理的SYO-1细胞中被抑制。 Pazopanib在20毫克/毫升和22.5毫克/毫升之间表现出逐渐增加的RPE细胞活性降低。
体内研究
与用载体或10毫克/千克Pazopanib处理的小鼠相比,用30毫克/千克或100毫克/千克Pazopanib处理的小鼠,肿瘤负荷显著降低。Pazopanib治疗具有良好的耐受性,并且每组小鼠的体重差异没有明显不同。
