背景及概述[1][2]
阿必鲁肽,是一种由葛兰素史克(GSK)公司研制的一周注射一次的GLP-I受体激动剂。2014年4月15日,美国FDA批准阿必鲁肽皮下注射剂结合饮食与运动用于改善II型糖尿病成人患者的血糖控制。
阿必鲁肽(Albiglutide)的分子式为 C3232H5032N 8640979S41,相对分子质量为72970,由两个30个氨基酸序列组成的GLP.1类似物与重组人血清白蛋白融合形成融合体。通过替换完整的人GLP.1氨基酸序列的第八位氨基酸(丙氨酸替换谷氨酸)达到抵抗二肽基肽酶(DPP-4)的水解作用啊,并与形成的融合蛋白起到延长半衰期的作用。与正常人相比T2D患者往往GLP-1水平降低。 阿必鲁肽具有肠促降糖素降低葡萄糖的作用嗍,从而促进葡萄糖依赖的胰岛素分泌、抑制胰高血糖素分泌,减慢胃排空,促进饱腹感。阿必鲁肽作为一个长效GLP.1类似物,可降低空腹和餐后血糖水平。虽然形成的融合蛋白增加了药物的半衰期,但融合的大分子蛋白可能会影响药物与GLP.1受体的相互作用,通过对小鼠的研究表明,阿必鲁肽由于相对分子质量的改变导致对胃排空和饱腹感的影响可能会削弱。
药物学研究[1]
1 剂量研究
Matthews等领导一项有54名Ⅱ型糖尿病病人参与的随机双盲平行试验, 病人每周随机注射 9mg、16mg、32mg 的阿必鲁肽,结果显示空腹及餐后血糖水平与注射剂量有关。Seino 等的研究进一步证实了剂量与疗效的关系,在一项具有40名日本II型糖尿病病人参加的随机双盲平行对照试验中,其阿必鲁肽的剂量分别为 15 mg/周、30 mg/周、50 mg/两周、100 mg/四周或为安慰剂。治疗 29 天后,所有治疗组相对于安慰剂组的糖化血红蛋白基线值均明显改善 (-0.58%,0.57%,-0.63%,-0.5 1%;P <0.03);除 100 mg/四周组外其余治疗组与安慰剂相比明显改善了空腹血糖水平;50mg/两周、100 mg/四周治疗组相对其他组的血糖波动性较大;同时30 mg/周治疗组的不良反应最少。因而,TANZEUM说明书的推荐剂量是30 m g 每周一次(腹部、腿部、上臂皮下注射)。如若治疗6-8周后,降血糖效果不佳,剂量可增加至50 mg 每周1次。
2 药代动力学
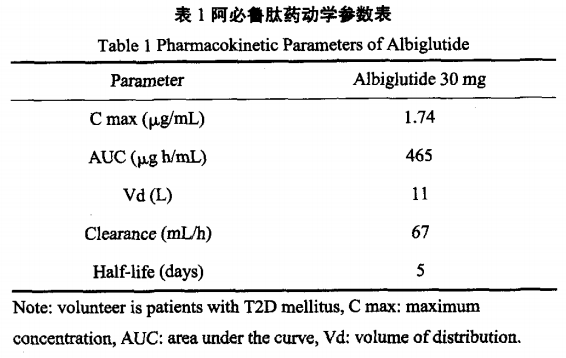
通过对39 名健康志愿者的临床试验发现,在第1、8天随机给予五种不同剂量的阿必鲁肽或安慰剂,(cohoat 1:0.25 +1 mg;cohort 2:3 + 6 mg;cohort3:16 + 24 m g;cohort4:4 8 + 6 0mg;cohort5:80 + 104 nag)。结果显示平均半衰期 (t1/2 ) 为 6.8天,血药浓度峰值(Tmax )出现在第 2.3-4 天,且血糖浓度与药物剂量有明显的联系。在针对Ⅱ型糖尿病病人的药代动力学研究中发现,单次注射30mg 的阿必鲁肽的血药峰浓度(Cmax) 为1.74g/m L,达峰时间为3-5日,曲线下面积(AUC)为465μg·h/mL;如若一周1次给药,4-5周后达稳态暴露量,估算其皮下注射的平均表观分布容积(Vd)为11L。阿必鲁肽作为一种与人血清白蛋白融合的药物,预估的代谢途径为由普遍存在的蛋白水解酶分解为小肽和单个氨基酸,其代谢途径可能与人类血清 白蛋 白代谢途径相似,即主要通过血管内皮分解。 研究发现本药平均表观清除率为 67 mL/h ,消除半衰期约为5天,故而本药合适每周一次给药。详细药代动力学参数见表 1。
3 药物相互作用
在药物相互作用研究中发现,阿必鲁肽与地高辛、口服避孕药以及华法林联合使用,对其药效或代谢率无明显影响。但当与辛伐他汀联合使用时,辛伐他汀及其活性代谢物的Cmax分别增长了18%和98%,辛伐他汀的曲线下面积( AUC )下降了40%,而其活性代谢物的AUC则增加了36%,这些药物相互作用的临床意义未知。
安全性研究[1]
1 生殖毒性研究
目前,没有暂无针对孕妇的药品安全性评价,小鼠动物模型显示当给予39 倍相当人类50mg剂量的阿必鲁肽时出现生殖毒性,但不致畸形,因而建议在计划妊娠前,需至少提前1 个月停止使用药物。由于阿必鲁肽是与血清白蛋白结合形成的融合蛋白,可能会存在于人类的乳汁中,故而建议停止哺乳或停止使用药物。
2 胰腺炎、甲状腺髓样肿瘤研究
包括阿必鲁肽在内的肠促胰素类药物均有导致胰腺炎的风险,在8项Ⅲ期临床试验中,出现的胰腺炎患者为阿必鲁肽组有6例 (6/2365,0.3%),安慰剂组0例(0/468,0%)以及阳性对比药物组 2 例(2/2065,0.1%)认定可能与药物治疗相关。在阿必鲁肽的说明书中,包含了黑框警告,提醒患者基于啮齿类动物与其他GLP -1类似物的研究发现,可能会导致使用者出现甲状腺髓样肿瘤。因而 FDA 要求阿必鲁肽上市后,要有至少15 年的甲状腺髓样肿瘤与药物的关系研究,以评价其安全性。
主要参考资料
[1] 张家行, 曹春来, 侯青宏,等. 阿必鲁肽:一种超长效Ⅱ型糖尿病治疗新药[J]. 现代生物医学进展, 2016, 16(2):353-357.
