323578-37-6
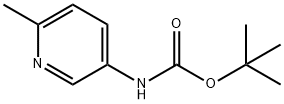 323578-37-6 结构式
323578-37-6 结构式
基本信息
N-BOC-6-甲基-3-氨基吡啶
(6-甲基吡啶-3-基)氨基甲酸叔丁酯
tert-Butyl (6-methylpyridin-3-yl)
tert-butyl 6-methylpyridin-3-ylcarbamate
Tert butyl 6- methyl pyridine -3- carbamate
tert-butyl N-(6-methylpyridin-3-yl)carbamate
Carbamic acid, (6-methyl-3-pyridinyl)-, 1,1-
(6-Methyl-pyridin-3-yl)-carbaMic acid tert-butyl ester
(6-Methyl-3-Pyridinyl)-Carbamic Acid 1,1-Dimethylethyl Ester
Carbamic acid, N-(6-methyl-3-pyridinyl)-, 1,1-dimethylethyl ester
Carbamic acid, (6-methyl-3-pyridinyl)-, 1,1-dimethylethyl ester (9CI)
物理化学性质
制备方法
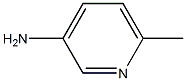
80287-53-2
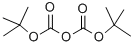
24424-99-5

323578-37-6
步骤1. 合成(6-甲基吡啶-3-基)氨基甲酸叔丁酯。在0℃下,向6-甲基吡啶-3-胺(25g,231mmol)的乙醇(100mL)溶液中缓慢滴加二碳酸二叔丁酯(55.5g,298mmol)。滴加完毕后,将反应混合物在室温下搅拌过夜。通过TLC(展开剂:石油醚/乙酸乙酯,2:1)监测反应进度,确认6-甲基吡啶-3-胺完全消耗。反应完成后,过滤反应混合物,滤饼用乙醇(30mL×3)洗涤。合并滤液,减压浓缩,得到黄色残余物。该残余物通过柱色谱法(洗脱剂:石油醚/乙酸乙酯,4:1至1:1)纯化,得到(6-甲基吡啶-3-基)氨基甲酸叔丁酯(32.5g,收率67.4%),为白色固体。1H NMR(400MHz,CDCl3)δ 8.30(d,J = 2.0Hz,1H),7.86(br s,1H),7.10(d,J = 8.5Hz,1H),6.57(br s,1H),2.49(s,3H),1.51(s,9H)。步骤2. 合成外消旋-顺式/反式-叔丁基(6-甲基哌啶-3-基)氨基甲酸酯。在氩气保护下,向干燥的氢化瓶中加入氧化铂(2.5g)。然后加入(6-甲基吡啶-3-基)氨基甲酸叔丁酯(33g,158.5mmol)的乙酸(300mL)溶液,将所得混合物在50℃、55psi氢气压力下氢化30小时。通过TLC(展开剂:石油醚/乙酸乙酯,2:1)监测反应进度,确认起始物料完全消耗。反应完成后,过滤反应混合物,滤饼用甲醇(50mL×2)洗涤。合并滤液,减压蒸发,得到(6-甲基哌啶-3-基)氨基甲酸叔丁酯(34g,收率100%),为黄色油状物(顺式/反式比例为2:1),该产物不经进一步纯化直接用于下一步反应。LC/MS(M + H)215.2。
参考文献:
[1] Patent: US2015/158864, 2015, A1. Location in patent: Paragraph 0270
[2] Journal of Medicinal Chemistry, 2017, vol. 60, # 5, p. 1971 - 1993
[3] Patent: WO2012/148775, 2012, A1. Location in patent: Page/Page column 113; 114
[4] Patent: WO2010/16005, 2010, A1. Location in patent: Page/Page column 135-136
[5] Bioorganic and Medicinal Chemistry Letters, 2016, vol. 26, # 22, p. 5580 - 5590