7440-38-2
 7440-38-2 结构式
7440-38-2 结构式
物理化学性质
安全数据
very toxic hazardous materials
Acute Tox. 3 Oral
Aquatic Acute 1
Aquatic Chronic 1
Carc. 1A
Repr. 1A
STOT RE 1 Oral
应用领域
制备方法
7440-38-2(安全特性,毒性,储运)
常见问题列表
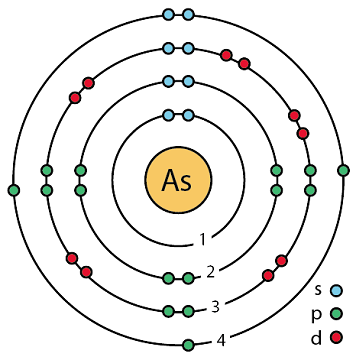
砷(Arsenic),化学元素符号为As,原子序数为33。砷分布在多种矿物中,通常与硫和其它金属元素共存,也有纯的元素晶体。艾尔伯图斯·麦格努斯在1250年首次对砷进行了记载。砷是一种非金属元素。单质以灰砷、黑砷和黄砷这三种同素异形体的形式存在,但只有灰砷在工业上具有重要的用途。
据传阿尔伯特·马格努斯(Albertus Magnus)在公元1250年获得了该元素。1649年,施罗德(Schroeder)发表了两种制备该元素的方法。在硫化物雄黄和果皮中发现它是天然的,如重金属的砷化物和硫代砷化物,氧化物和砷化物。
金属的硫砷化物、金属砷化物和雄黄以及自然界中的砷单质是商品化的砷产品的主要来源。环境中也有有机砷化合物存在。有机无机砷及其化合物,一旦进入食物链,通过甲基化过程逐步代谢为毒性较低的砷。
其他接触到自然界中的砷元素的途径包括火山灰、含砷矿物和矿石的风化和被地下水溶解。砷也能存在于食物、水体、土壤和空气中。砷能被所有的植物吸收,但更容易在叶用蔬菜、稻米、苹果和葡萄汁以及海产品中富集。
砷有广泛的用途:1.砷可用于合金的制造,比如生产铜的强化合金或是添加到制造车用铅酸蓄电池的合金中;
2.制造半导体电子器件时用砷作为掺杂剂合成n形半导体材料,掺杂了硅的光电子化合物砷化镓是在使用中最常见的半导体;
3.砷和它的化合物,特别是三氧化二砷(砒霜)用于合成农药(用于处理木材产品)、除草剂和杀虫剂。但这些方面的应用正在逐渐消失。
砷主要是从提炼铜产生的副产物中提取回收出来的。从铜,黄金,铅冶炼厂排出的粉尘就含有砷。
在空气中焙烧砷黄铁矿,砷元素以三氧化二砷的形式升华与氧化铁分离。而在无氧条件下焙烧则生成砷单质。通过在真空条件或氢气气氛中升华的方法可以将砷从硫或硫族元素中分离出来,也可以通过蒸馏熔融的铅砷混合物来分离砷。
砷以无机和有机形式存在。
无机砷化合物(比如水中所见者)含剧毒,而有机砷化合物(例如海产食品中所见者)对健康危害较小。 急性影响 急性砷中毒的早期症状包括呕吐、腹部疼痛和腹泄,随后是四肢麻痹和刺痛,肌肉痉挛,在极端情况下会发生死亡。 长期影响 长期接触高浓度无机砷(例如通过饮用水和食品)的先兆症状通常见之于皮肤,包括色素沉着变化、皮肤损伤以及手掌上的硬斑和双足上的肉垫(角化过度)。这些是最低限度大约五年砷接触后发生的,可能是皮肤癌的先兆。
除了皮肤癌外,长期接触砷还可能引起膀胱癌和肺癌。国际癌症研究机构将砷和砷化合物列为对人类致癌物,并称饮用水中的砷也是人类致癌因素。



