7647-17-8
 7647-17-8 结构式
7647-17-8 结构式
基本信息
氯化銫,光学级
氯化铯, 99.9% (METALS BASIS)
氯化铯, 超干, 99.9% (METALS BASIS)
氯化铯, 99.99% (METALS BASIS)
氯化铯, 99.999+% (METALS BASIS)
氯化铯, 99% (METALS BASIS)
氯化铯, 超干, 99.998% (METALS BASIS)
氯化铯, 超干, 99.99% (METALS BASIS)
CESIUM CHLORIDE
CESIUM CHLORIDE IN 0.1 N HCL
CSCL
Cesium chloride (CsCl)
Cesium monochloride
cesiumchloride(cscl)
cesiummonochloride
Dicesium dichloride
dicesiumdichloride
Tricesium trichloride
tricesiumtrichloride
Caesiumchlorid
Caesium chloride 99+ %
Cesium Chloride, MB Grade (1.01548)
Cesium chloride, Molecular Biology Grade
Cesium Chloride, ULTROL Grade
Cesium chloride,(99.9% Cs)
Cesium ion chromatography standard solution Fluka
Cesiumchlorid
物理化学性质
λ: 280 nm Amax: 0.02
| a/nm | b/nm | c/nm | α/o | β/o | γ/o | V/nm3 |
| 0.412 | 0.412 | 0.412 | 90 | 90 | 90 | 0.06994 |
安全数据
应用领域
制备方法
1.将碳酸铯溶解于少量水中。在不断搅拌下慢慢加入相对密度为1.18的盐酸,加热反应:

当pH=3时,煮沸半小时加入氢氧化铯使溶液pH值到中性。过滤,滤液蒸发浓缩至大量结晶析出,冷至室温,分离母液,洁净与100oC烘干,即为成品。
2.用碳酸铯溶于盐酸,再浓缩其溶液以制取氯化铯。通常可得到纯度为99.5%的氯化铯,可直接使用。对不够纯净的氯化铯,可采用下列方法精制。将15g的氯化铯,加热溶于100mL的水中。将化学计量24.2g氯化汞溶于25mL 4mol的盐酸中。趁热将此HgCl2HCl溶液加到上述溶液中,搅拌混合,冷却,即可析出CsHgCl3结晶。吸滤,收集结晶,弃去母液。将结晶溶于120mL的热水中,冷却后再次有结晶析出。为此反复进行2~3次重结晶,碱金属可降至0.01%以下,最后将结晶溶于热水,通入H2S气体使溶液达到饱和,就有HgS沉淀析出,滤去HgS,收集滤液,蒸发至干,即可得纯净的氯化铯。
3.通常可得到纯度为995%的氯化铯,可直接使用。对不够纯净的氯化铯,可采用下列方法精制。
精制方法1[166]将15g的氯化铯,加热溶于100mL的水中。将化学计量24.2g氯化汞溶于25mL 4mol的盐酸中。趁热将此HgCl2、HCl溶液加到上述溶液中,搅拌混合,冷却,即可析出CsHgCl3结晶。吸滤,收集结晶,弃去母液。将结晶溶于120mL的热水中,冷却后再次有结晶析出。为此反复进行2~3次重结晶,碱金属可降至0.01%以下,最后将结晶溶于热水,通入H2S气体使溶液达到饱和,就有HgS沉淀析出,滤去HgS,收集滤液,蒸发至干,即可得纯净的氯化铯。
7647-17-8(安全特性,毒性,储运)
常见问题列表
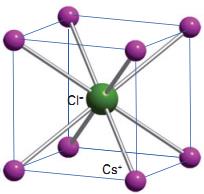
氯化铯晶体是简单立方晶体。采取这种晶体结构的化合物包括CsCl,CsBr,CsI,TlCl,TlBr和NH4Cl等。
146g/0℃;175g/10℃;187g/20℃;197g/30℃;208g/40℃
230g/60℃;250g/80℃;260g/90℃;271g/100℃
| 报价日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
| 2026/03/03 | 089188 | 氯化铯, 99.999+% (metals basis) Cesium chloride, 99.999+% (metals basis) | 7647-17-8 | 50g | 2204元 |
| 2026/03/03 | 087640 | 氯化铯, 99.99% (metals basis) Cesium chloride, 99.99% (metals basis), Thermo Scientific Chemicals | 7647-17-8 | 50g | 1746元 |
| 2026/03/03 | 043720 | 氯化铯, 超干, 99.99% (metals basis) Cesium chloride, ultra dry, 99.99% (metals basis), Thermo Scientific Chemicals | 7647-17-8 | 50g | 2682元 |
