背景[1-3]
通用基因组DNA提取试剂盒采用可以特意性结合DNA的离心吸附柱和独特的缓冲液系统,提取血液、唾液、口腔拭子、动物组织、粪便中的基因DNA、可限度的去除杂质蛋白及细胞中的其他化合物,提取的基因组DNA片段大,纯度高,质量稳定可靠。使用用本试剂盒提取的基因组DNA可适用于各种常规操作,包括酶切、PCR、测序、连接、转化和转染多种细胞等实验。
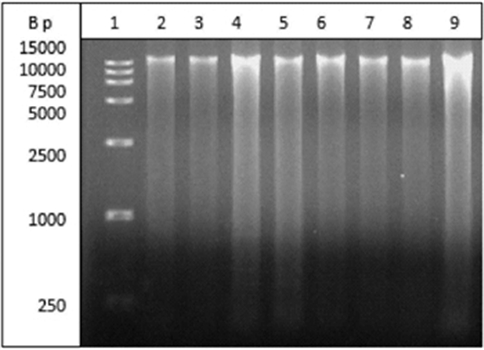
基因组DNA琼脂糖电泳图
适合处理以下几类来源的非液体类样品:
A.人和动物组织:1-25 mg动物组织或穿刺组织、福尔马林浸泡的组织、石蜡包埋切片、鼠尾、毛囊、指甲等
B.干燥的人和动物体液:滤纸、纸巾或样品采集卡上的干血点和唾液、香烟过滤嘴等
C.可离心收集的1×103~1×107动物细胞
D.可离心收集的1×107~2×109细菌
E.可离心收集的1×105~5×107酵母或真菌细胞
F.10-100 mg真菌菌块或菌丝
方法简便,具备以下特点:
处理人和动物组织无需研磨;
处理人和动物组织分散细胞和释放DNA为同一个步骤,无需使用两个温度分两个步骤操作;
处理离心收集的细菌和细胞在悬浮样品后直接进行裂解,无需再添加裂解试剂;
处理石蜡包埋切片无需脱蜡;
应用[4][5]
用于鹿血的PCR-RFLP鉴定方法研究
1. 建立鹿血PCR-RFLP(聚合酶链式反应--限制性片段长度多态性)种间及不同基原鉴定方法。2.寻找鹿血与非鹿血鉴别的限制性内切酶,并确定鹿血中掺入其他常见动物血的检出限度。3.寻找鉴别梅花鹿与马鹿血的限制性内切酶,并确定梅花鹿血中加入马鹿血的检出限度。
方法:1.用三种不同的试剂盒提取样品血液基因组DNA,测定浓度及纯度,选择适合提取本研究中动物血液基因组DNA的试剂盒。
2. 用动物DNA条形码通用引物COI和cytb(细胞色素b),扩增样品血液基因组DNA,以扩增效率高、扩增结果稳定为指标选取引物,并优化扩增条件。
3. 试剂盒法纯化PCR产物,T-A克隆(蓝白斑筛选及琼脂糖凝胶电泳确定阳性克隆),菌液进行基因序列测定。
4. 采用软件NEB Cutter2.0(http://nc2.neb.com/NEBcutter2/)对各样品血液的测序结果进行比对分析,确定试验中所购样品均为正品。根据各样品血液的cytb基因序列的差异,设计、选取可以区分鹿与非鹿、梅花鹿与马鹿的DNA限制性内切酶,并经实验验证。
5.将提取的各样品血液基因组DNA稀释至相似浓度,且A260在0.11.0范围内。在梅花鹿血基因组DNA中分别加入不同体积分数的非鹿类动物血基因组DNA,在梅花鹿血基因组DNA中加入不同体积分数的马鹿血基因组DNA,经PCR扩增后,产物用限制性内切酶进行切割,确定检出限度。
参考文献
[1]Molecular tracing of confiscated pangolin scales for conservation and illegal trade monitoring in Southeast Asia[J].Huarong Zhang,Mark P.Miller,Feng Yang,Hon Ki Chan,Philippe Gaubert,Gary Ades,Gunter A.Fischer.Global Ecology and Conservation.2015
[2]DNA Barcode-Based PCR-RFLP and Diagnostic PCR for Authentication of Jinqian Baihua She(Bungarus Parvus)[J].Xiaolei Li,Weiping Zeng,Jing Liao,Zhenbiao Liang,Shuhua Huang,Zhi Chao,Robert Henry.Evidence-Based Complementary and Alternative Medicine.2015
[3]Identification of Lonicera japonica and its Related Species Using the DNA Barcoding Method[J].Zhiying Sun,Ting Gao,Hui Yao,Linchun Shi,Yingjie Zhu,Shilin Chen.Planta Med.2011(03)
[4]DNA Barcoding of Panax Species[J].Yunjuan Zuo,Zhongjian Chen,Katsuhiko Kondo,Tsuneo Funamoto,Jun Wen,Shiliang Zhou.Planta Med.2011(02)
[5]王凤霞.鹿血的PCR-RFLP鉴定方法研究[D].承德医学院,2018.
