氘(deuterium,D或2H)是氢的稳定非放射性同位素,也称为重氢,氘原子核中有一个质子和一个中子,其相对原子量为普通氢的二倍。氢元素中有0.02%的氘,在大自然的含量约为一般氢的七千分之一。在生物医学相关领域,将药物分子中的部分位点的氢原子用其稳定同位素氘来替代,即对药物进行氘代标记,进而与液-质联用,能够快速获得数据并进行分析,这使得该技术广泛应用于对药物体内过程的吸收、分布、代谢和排泄过程的研究。如在药物代谢中,使用非标记和氘代标记的药物混合物,通过GC-MS或LC-MS对代谢产物进行分析检测,并确定代谢产物的结构。将药物进行氘标记除了可以方便地对生物体内的代谢产物进行定位分析,还有助于发现新的代谢产物以便开展代谢机理的研究等。使用氘标记药物进行临床代谢动力学研究主要有以下优点:测试的灵敏度和精度很高、测试快速便捷、数据可信度高等。
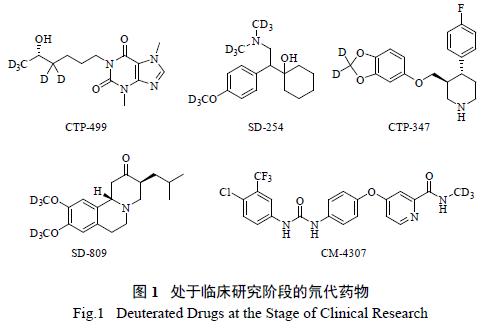
氘代药物作为一类新型药物已引起广泛关注。由于碳-氘键比碳-氢键更加稳定,将氢替换为氘后,可直接影响药物的吸收、分布、代谢和排泄等过程,一方面可提高药物的疗效,另一方面可以封闭代谢位点,延长药物半衰期。目前已有多家公司从事氘代药物的研究,如国外的Concert Pharmaceuticals和Auspex Pharmaceuticals,国内的苏州泽璟公司等。其中一些典型药物如CTP-499、氘代文拉法新(SD-254)、氘代帕罗西汀(CTP-347)、氘代丁苯那嗪(SD-809)以及氘代索拉非尼(CM-4307) 等,已进入Ⅰ期或Ⅱ期临床研究阶段(图1)。
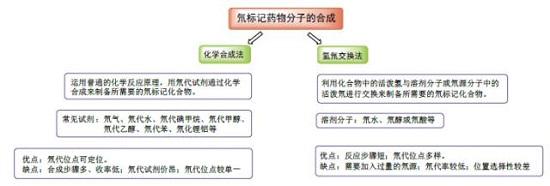
在这些领域的研究中,通常需要对相关药物分子的特定位点进行氘代标记,并且要求氘代位点有很高的氘代率。然而,由于氘元素的天然丰度太低,想要获得氘代率达到一定程度的药物,只能用含氘原料的合成反应来实现。氘代药物的合成方法主要有化学合成法和氢氘交换法。本文针对近年来氘标记药物分子的合成进行综述。
1、化学合成法
化学合成法是运用普通的化学反应原理,用含有氘元素的试剂,通过化学合成来制备所需要的氘标记化合物。常见的试剂有氘气、氘代水、氘代碘甲烷、氘代甲醇、氘代乙醇、氘代苯、氘化锂铝等,在目标分子的合成过程中,通常根据不同的氘代产物来选取不同的氘代试剂和反应方法。下面根据氘代试剂的不同进行一一阐述并举例说明。
1.1 氘代烷基化试剂
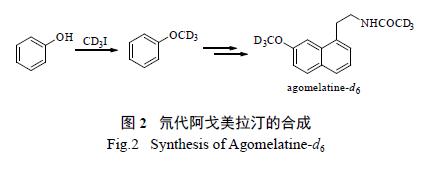
氘代药物中最常见的氘代基团是杂原子上连有氘代甲基(CD3)或氘代乙基(C2D5),对于这种结构,一般可采用氘代碘甲烷(CD3I)、氘代碘乙烷(C2D5I)等进行烷基化反应,从而生成相应的氘代产物。有时也可利用价格相对低廉的氘代甲醇或氘代乙醇作为烷基化试剂。如梁大伟等以苯酚为起始原料(图2),与氘代碘甲烷反应得氘代甲基标记的苯甲醚,再经傅- 克酰化、羟醛缩合、芳构化、还原及氘代乙酰化反应得目标药物分子氘代阿戈美拉汀(agomelatine-d6)。
1.2 氘代苯及其衍生物
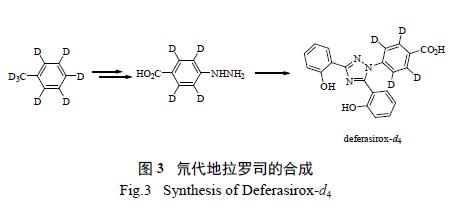
对于氘原子连接在苯环上的氘代药物分子,通常利用氘代苯或其衍生物,如氘代溴苯、氘代苯胺、氘代苯甲酸等作为底物,经过多步反应合成目标化合物。如文献报道用氘代甲苯为原料,经硝化、氧化、还原、重氮化等多步反应,首先合成氘代对肼基苯甲酸,再通过一步缩合反应来实现氘代地拉罗司(deferasirox-d4)的合成(图3)。
1.3 还原性氘试剂对不饱和键的还原反应
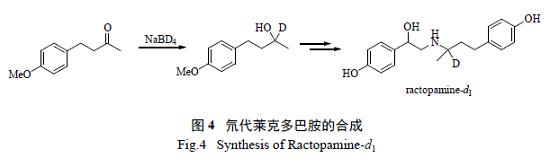
当药物的合成路线中含有还原反应,可使用还原性氘代试剂,如氘气、氘化锂铝、硼氘化钠等对不饱和键进行还原,从而得到氘原子加成到不饱和键上的产物,然后通过后续的转化反应生成目标氘代药物。如文献报道的氘代莱克多巴胺(ractopamine-d1) 的合成(图4)。
1.4 去官能化氘代反应
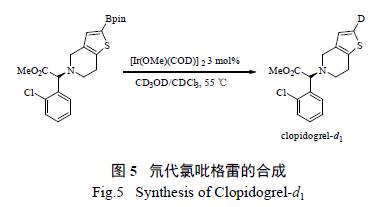
对于含有硼的化合物,其与氘离子进行氘解反应时,氘可以替代硼的位置,从而生成相应位点的氘代产物。利用这一原理,可以先合成目标氘代药物中想要氘代位点的硼化产物,然后进行氘解反应,生成相应的氘代药物。如将氯吡格雷中噻吩的邻位先进行硼化,然后再在铱催化下进行氘解,从而合成氘代氯吡格雷(clopidogrel-d1)(图5)。
此外,对含有碳- 卤键的化合物,在钯炭催化下可以发生还原脱卤反应,如果用氘气作为氘源,则得到卤素被氘取代的产物。如Allen等对氘代奈韦拉平(nevirapine-d1)的合成(图6)。

2、氢氘交换法
同位素交换是指两种不同分子之间同一元素的同位素相互替代的过程。对于氢氘交换,该方法是利用化合物中的活泼氢,与溶剂分子或氘源分子中的活泼氘进行交换。溶剂分子可选用价廉的氘代水、氘代醇或氘代酸等。在交换过程中,需要加入过量的氘源,才能得到理想氘代率的氘代目标化合物。如果氘代率不高,可通过多次交换来提高目标化合物的氘代率。
2.1 酸碱催化的氢氘交换反应
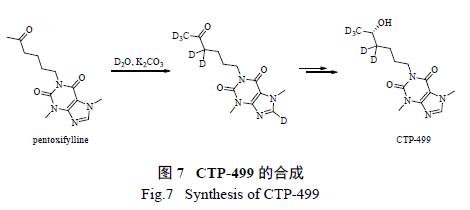
羰基邻位C-H键的酸性比较强,在碱的作用下可与氘代水发生氢氘交换反应。如用己酮可可碱为起始原料,在碳酸钾作用下与氘代水发生氢氘交换反应,经过后续的脱氘和还原反应,合成具有抗炎、抗氧化和抗纤维化等多种药理活性的糖尿病肾病治疗药CTP-499(图7)。
端炔烃的碳- 氢键也有一定的酸性,在碱或金属催化下也能与氘代溶剂发生氢氘交换反应。如文献报道用钌配合物作催化剂,成功实现了氘代优降宁(eudatin-d1)的合成(图8)。

2.2 金属催化的芳基氢氘交换反应
近年来,随着过渡金属催化不活泼碳- 氢键反应的不断深入研究,对于不活泼的碳-氢键化合物,也可在过渡金属的催化下进行氢氘交换反应,这些方法也逐渐应用于氘标记药物分子的合成。
2.2.1 铱催化的氢氘交换反应
2015年,Kerr等详细研究了磺酰胺作定位基团时,铱配合物可以催化磺酰胺邻位碳-氢键的选择性氘代反应,将该方法拓展到塞来昔布的氢氘交换反应上,磺酰胺邻位的氘代率可达97%,而间位只有11%,其他位置没有发生氘代反应,证明该反应具有非常好的位置选择性(图9)。

2.2.2 钌催化的芳基氢氘交换反应
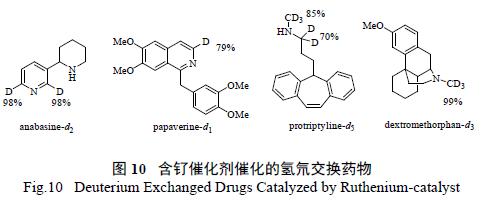
钌也广泛应用于催化碳- 氢键的活化。文献将纳米钌应用于氮杂芳环的氘代反应,以及氘代安纳巴松(anabasine-d2)、氘代罂粟碱(papaverine-d1)、氘代普罗替林(protriptyline-d5) 和氘代氢溴酸右美沙芬(dextromethorphan-d3)的合成中,结果表明目标药物分子都有非常高的氘代率和位置选择性(图10)。
2.2.3 铱催化的烷基氢氘交换反应
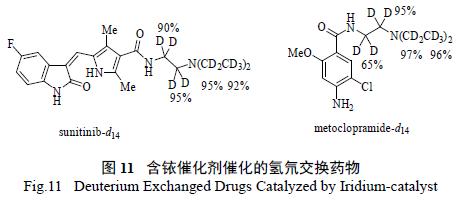
Neubert等研究了烷基胺的氢氘交换反应,在Shvo催化剂催化下,氮原子的α和β-位同时发生氘代反应, 并成功将其应用于氘代舒尼替尼(sunitinib-d14)和氘代甲氧氯普胺(metoclopramided14)等的合成(图11)。
2.2.4 铁催化的芳基氢氘交换反应
上面介绍的不活泼碳- 氢键的氢氘交换反应通常都需使用贵金属催化剂,最近Yu等在Nature报道了廉价金属铁催化的氢氘交换反应,反应具有非常好的普适性,并成功应用于多个药物分子的氢氘交换反应(图12)。
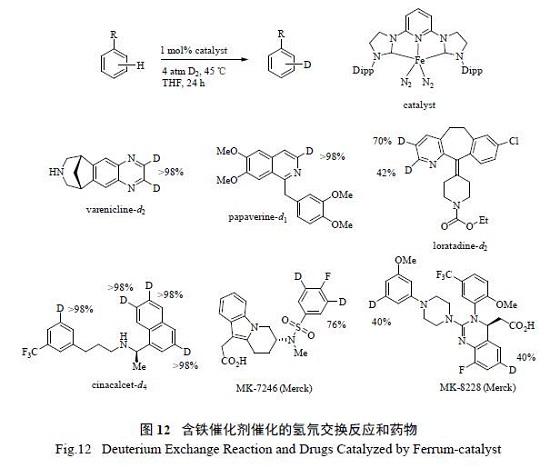
采用氢氘交换的方法可直接以目标药物分子或其前体为起始物,经一步或几步反应,快速构建氘标记的目标药物分子。反应过程中通常只需使用廉价的氘源,且氘代位点具有多样性。
3、结论和展望
氘标记的药物分子在生物学、药学、医学等领域发挥着重要作用,开发选择性合成特定位点的氘代标记化合物的方法,具有重要的学术意义和应用前景。对于化学合成法来说,发展新型的氘代试剂并商品化,可以更加有效地缩短反应步骤,优化反应路径,从而更高效地合成氘代目标药物分子。氢氘交换反应在氘代药物分子的合成中已受到越来越多的关注,发展新型的催化体系,使之具有更好的位置选择性、更高的氘代率、以及更好的底物适用性,将推动氘代药物产业的快速发展。
