背景及概述[1][2][3]
布格替尼是新一代酪氨酸激酶抑制药,对ALK+ 转移性NSCLC 有显著的疗效,2016年8月30日美国FDA授予布格替尼对代ALK+NSCLC 治疗药克唑替尼已进展或不能耐受的患者以突破性疗法和用于ALK+NSCLC 治疗罕用药地位,给予上市申请优先审评及允许申请资料滚动递交的待遇。FDA于2017年4月28日批准布格替尼上市,商品名为Alunbrigtm。
从2011年至今,美国国立综合癌症网络和欧洲肿瘤医学会历年发布的NSCLC 诊疗指导原则都推荐作为ALK+(阳性)NSCLC 的一线治疗首选治疗药物。2011年8月28日获美国食品药品管理局批准上市,2014年9月18日克唑替尼2 种规格的胶囊剂获得国家食品药品监督管理总局的进口注册证,用于治疗晚期或转移性ALK+NSCLC。
然而,尽管克唑替尼在ALK+患者获得良好中位无进展生存期和客观缓解率,但克唑替尼不能越过血-脑屏障,无法治疗中枢神经系统内ALK+肺癌,而且,NSCLC 不断产生新的基因亚型,最终难逃耐药性而治疗失败的命运。布格替尼其他译名为布吉替尼、布里替尼、布吉他滨等。布格替尼最初由美国Ariad制药公司研制,该公司后被日本武田制药株式会社收购,成为武田制药旗下的子公司,负责在美国上市和销售。
适应症[1]
布格替尼适用于ALK 阳性转移性NSCLC 患者,这些患者经克唑替尼治疗后不能耐受或疾病已进展,此适应证是根据肿瘤的缓解率和缓解的持续时间加速审批的,对适应证的后继批准可能取决于进一步临床试验的确证和对临床获益的描述。
规格[1]
薄膜包衣片,有2种规格,每片30和90mg。
用法用量[1]
1. 服药方法:是否与食物同服均可,药品应整片吞服,不可压碎或咀嚼。若缺失一次剂量或服药后发生呕吐,当日不另服附加剂量,应按服药时间表,服下一次剂量。
2. 正常剂量:在前7d的诱导期,口服90mg,每天1次,若患者能耐受,剂量增加至180mg,每天1次,,直至疾病进展或不能耐受药物的不良反应。
3. 调整剂量:对不良反应的剂量调整,若正在服90mg,每天1次。第1次可减为60mg,每天1次,再发生不良反应,就永久终止服药;若若正在服180mg,每天1次。第1次减量为120mg,每天1次,第2次减量为90mg,每天1次,第3次减量为60mg,每天1次。因不良反应减低剂量,随后不能随意增加剂量,如不能耐受60mg,每天1次的剂量应永久终止服药。
不良反应及注意事项[1]
1. ILD与肺炎:代号ALTA 的临床试验,曾出现服ALUnbrIg®后发生严重危及生命的ILD与肺炎不良反应。A 组有3.7%的患者,B 组为9.1%。最早发病时间在服药9 D内,发病中位时间为2 d,6.4%患者为不良反应3 或4 级,其中,2.7%是在监测新出现呼吸道症状或旧病复发中发现ILD与肺炎。开始治疗和治疗全过程,需密切监测患者的呼吸道症状。
2. 高血压:ALTA 试验,A 组报告高血压11%,B 组为21%。3 级高血压总病例数为5.9%。治疗前需严格控制血压,开始治疗后2 周和治疗期间都应监测血压。
3. 心动过缓:经ALUnbrIg® 治疗,可能发生心动过缓。ALTA 试验,A 组有5.7%患者心率<50 次/min,B组为7.6%。A 组1 例(0.9%)发生2 级心动过缓。治疗期间应监测心率和血压。如不能避免与可致心动过缓药物同服,应更频繁监测患者的心率和血压。
4. 视力障碍:ALTA 试验,观察到ALUnbrIg®可致视力障碍,包括视力模糊、复视和视力减退,A 组有7.3%,B 组为10%。两组各有1 例患者出现3 级视力障碍,分别为黄斑水肿和白内障。治疗期间建议患者报告任何视力症状。
5. CPK 升高:ALTA 试验,A 组发生CPK 升高27%,3 或4 级为2.8%,B 组48%,3 或4 级为12%。治疗期间应监测CPK 水平。建议患者报告任何不能解释的肌肉痛、压痛或软弱症状。
6. 胰酶升高:ALTA 试验,A 组有27%患者发生淀粉酶升高,3 或4 级为3.7%,B 组有39%,3 或4 级为2.7%。A 组有21%患者脂肪酶升高,3 或4 级为4.6%,B 组为45%,3 或4 级为5.5%。治疗期间应监测脂肪酶和淀粉酶。
7. 高血糖:ALTA 试验,接受ALUnbrIg® 治疗患者有43%出现新的高血糖症或原有病症恶化。据实验室检测,3.7%患者空腹血糖为3 级,10%(2/20)患者有糖尿病或基线葡萄糖不耐受,要求胰岛素治疗。开始治疗前应评估空腹血糖,其后需定期监测血糖。
8. 胚胎-胎儿毒性:根据作用机制和动物实验观察,孕妇服ALUnbrIg®可致胎儿危害。尚无妊娠妇女服ALUnbrIg®的临床数据。孕大鼠在器官形成期给予布格替尼12.5 mg/kg/d,按AUC 计算,相当于人用接触剂量(180 mg,qd)的0.7倍,可致剂量相关骨骼异常,剂量为25 mg/kg/d,相当于人接触剂量(180 mg,qd)≥1.26 倍,将增加植入后丢失、畸形和降低胎儿体质量。应忠告妊娠妇女对胎儿潜在风险。
建议有生殖潜能女性及其伴侣在治疗期间和末次剂量后至少4 个月使用有效的非激素避孕。
9. 哺乳期:尚无布格替尼进入人乳汁或对哺乳喂养婴儿及对乳汁产生影响的数据。哺乳喂养婴儿可能有潜在的不良反应,建议在治疗期间和末次剂量后一周不要哺乳喂养婴儿ꎮ
10. 老年患者:布格替尼的临床研究未包括足够数量的年龄≥65 岁患者,以确定老年患者的反应是否不同于较年轻患者。ALTA 试验,在222 例患者中,65~74岁患者占19.4%,≥75 岁占4.1%。患者≥65 岁和较年轻患者间未观察到全性或疗效有临床意义的差别。
制备[2]
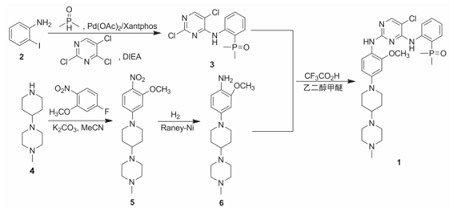
以2-碘苯胺为起始原料,经"一锅法"反应制得{2-[(2,5-二氯嘧啶-4-基)氨基]苯基}二甲基氧化膦(3); 1-甲基-4-(哌啶-4基)哌嗪(4)与5-氟-2-硝基苯甲醚反应后,经氢化还原得2-甲氧基-4-[4-(4-甲基哌嗪-1-基)哌啶-1-基]-苯胺(6); 3和6反应合成了布格替尼,总收率48. 5%,纯度99. 6%,其结构经1H NMR和MS(ESI)确证。
主要参考资料
[1] 陈本川. 治疗非小细胞肺癌新药——布格替尼 (brigatinib)[J]. 医药导报, 2017, 36(12): 1448-1456.
[2] 周海平, 倪迎港, 秦海芳, 等. 抗肿瘤药布格替尼的合成[J]. 合成化学, 26(9): 707-710.
[3] 杨雪, 倪倩, 裴艺芳, 等. 间变性淋巴瘤激酶酪氨酸激酶抑制剂布格替尼的药理作用与临床评价[J]. 临床药物治疗杂志, 16(6): 32-36.
