背景及概述
噻唑环是一类重要的含氮硫杂原子的五元芳杂环,有一个5元饱和环,1位有一个硫醚基,3位有一个胺基,其特殊的结构使得噻唑类化合物在化学、药学、生物学和材料科学等诸多领域具有广阔的应用前景,显示出巨大的开发价值,受到广泛关注。噻唑烷衍生物用途较多,具有广谱的生物活性。2-溴噻唑-5-甲酸甲酯是重要的有机合成中间体,可通过多种方式将噻唑基团引入其他分子中,产生新的具有生物活性的化合物,在药物合成中有着广泛的应用。2-溴噻唑-5-甲酸甲酯英文名称:Methyl 2-bromolhiazole-5-carboxylate,中文别名 :2-溴-噻唑-5-甲酸甲酯,CAS号:54045-74-8,分子式:C5H4BrNO2S,分子量:222.060。
制备
2-溴噻唑-5-甲酸甲酯的传统合成方法是先将α-卤代乙酸酯与甲酸乙酯反应得到α-甲酰基-α-卤代乙酸酯,再与硫脲进行环合,但原料具有较强的催泪性,且中间产物极不稳定,使得反应条件难以控制,总产率低;用β-乙氧基丙烯酸乙酯与N-溴代丁二酰亚胺(NBS)和水反应得到α-溴代β-羟基β-乙氧基丙酸乙酯,后者未经分离直接与硫脲环合制得2-氨基噻唑-5-甲酸乙酯,整个反应采用一锅法完成,条件温和,操作简便,产率高,但所用原料β-乙氧基丙烯酸乙酯价格昂贵。本文参考上述方法,以价格相对低廉的β-甲氧基丙烯酸甲酯为原料合成了2-氨基噻唑-5-甲酸甲酯;再通过重氮化-溴代反应将其转变为目标化合物2-溴噻唑-5-甲酸甲酯[1]。2-溴噻唑-5-甲酸甲酯的合成路线如下:
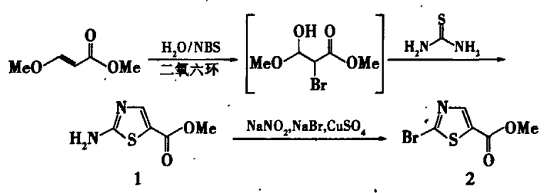
图1 2-溴噻唑-5-甲酸甲酯的合成路线图
实验操作:
2-氨基噻唑-5-甲酸甲酯(1)的合成
方法一、向一个干燥的 250mL 圆底烧瓶内依次加入 3.90g( 0.03 mol )β-甲氧基丙烯酸甲酯,4.56 g ( 0.06 mol ) 硫脲,7.62 g ( 0.03 mol ) 碘,搅拌使其混合均匀,在85℃ 下反应 15 h 。反应结束后,向烧瓶中加入大量水进行稀释,使固体大多溶解 (可微微加热),抽滤,取滤液。向滤液中加入浓氢氧化钠溶液,调节反应液使 pH 呈弱碱性,结晶抽滤,干燥得 2.76 g 白色粉状固体产物。
方法二、在100 mL三口烧瓶中加入25 mL水和25 mL二氧六环,冷却至-10℃后加入5.81 g(0.05 mol)β-甲氧基丙烯酸甲酯和9.78 g(0.055 mol)N-溴代丁二酰亚胺,室温下搅拌至完全溶解,然后加入3.80g(0.05 mol)硫脲,将混合液缓慢升温至80℃继续反应l h,冷却到室温,加入浓氨水10 mL,搅拌10 min,减压过滤,滤饼用水洗,真空干燥,得棕黄色固体5.60 g,产率71%。
2-溴噻唑-5-甲酸甲酯(2)的合成
方法一、在100 mL三口烧瓶中加入1.58 g(0.01 mol)化合物1,7.12 g(0.03 mol)五水硫酸铜,3.97 g(0.038 mol)溴化钠和20 mL 9 mol/L硫酸溶液,冰盐浴冷却至-5至-10℃,然后缓慢滴加已冷却至0℃的亚硝酸钠溶液(0.79 g亚硝酸钠溶于6.76 mL水中),滴加过程持续约40 min,滴加完毕后将反应液温度缓慢升至室温继续搅拌30 min,加20 mL水稀释反应液,用乙酸乙酯(20 mL×3)萃取,合并有机相,无水硫酸钠干燥,过滤,减压蒸去溶剂,粗产物经硅胶柱层析分离(乙酸乙酯:石油醚=1:15)得白色固体1.53 g,产率68%。
方法二、
250 mL 反应瓶中,加入 9.3 g ( 53.7 mmol )2-氨基噻唑-5-甲酸甲酯,加入 27.2 mL ( 0.4 mol ) 磷酸和 27.8 mL( 0.4 mol )硝酸,室温下磁力搅拌溶解,待溶清后将反应瓶移至带搅拌和滴液漏斗的反应釜中,控制温度在 0~5℃ 以内,滴加 4.6g ( 6.5mmol ,2.2mol/L )亚硝酸钠溶液;滴加完毕,继续搅拌 30 min 。滴加29.0 g ( 0.1 mol ,4.3 mol/L ) 溴化铜溶液,滴加完毕,在 0~5℃ 下继续反应 40 min ,再滴加 20.0 mL水,滴加完毕过滤,40℃ 下鼓风干燥 12 h 得橙红色粗品。用甲醇重结晶得 10.6g (理论量为 12.5g )白色晶体,收率 84.7% 。
结果与讨论
2-氨基噻唑-5-甲酸甲酯的合成以β-甲氧基丙烯酸甲酯为起始原料,避免了使用强催泪性的β-卤代乙酸酯;反应采用一锅法进行,可避免分离不稳定的中间产物,简化了操作,提高了产率;所得产物无需精制,可直接用于下一步反应。
文献报道将氨基噻唑衍生物转化为溴代噻唑衍生物一般采用亚硝酸异戊酯(叔丁酯).溴化、铜或亚硝酸钠-溴化钠-硫酸铜作为重氮化-溴代试剂。我们曾尝试用前一种方法合成2-溴噻唑-5-甲酸甲酯,但因反应产物被包裹在大量不溶于有机反应介质的溴化铜及溴化亚铜固体中,后处理复杂,产率低。后改用硫酸溶液作为溶剂,以亚硝酸钠-溴化钠-硫酸铜作为重氮化-溴代试剂,反应转化率高,后处理较为简单,且所用试剂价廉易得。为使重氮化反应进行完全并避免重氮盐分解,需在搅拌下缓慢滴加亚硝酸钠溶液,且滴加过程中反应液须用-5至-10℃冰盐浴冷却。
结论
通过对重氮化反应温度、重氮化反应时间、反应物料配比等工艺条件的研究,得到合成2-氨基噻唑-5-甲酸甲酯的优化工艺为:重氮化反应温度为 0~5℃ ,重氮化反应时间为 40 min ,物料配比为 n (2-氨基噻唑-5-甲酸甲酯) ∶n ( 85.0%磷酸) ∶n ( 65.0%硝酸) ∶n (亚硝酸钠) ∶n (溴化铜) =1.0∶8.0∶8.0∶1.3∶2.5 ; 在此工艺条件下可合成得产品纯度为 99.5% ,收率达 84.7% ,产品结构经熔点、1 HNMR 等方法确证。此合成路线原料廉价易得,收率高,具有工业化应用前景。
参考文献
[1] 王莹 , 匡永清 , 罗成礼 , 等 . 2- 氨基噻唑 -5- 甲酸甲酯和 2- 溴噻唑 -5- 甲酸甲酯的简便合成 [J]. 化学试剂 , 2008, 30 (5) : 385-386.
