JNJ-79635322/JNJ-5322(BCMA
× GPRC5D ×
CD3)在I期试验(NCT05652335)中,对重度预处理后的RRMM患者(中位既往4线治疗)显示出86%的总缓解率(ORR),在推荐II期剂量(RP2D)下达到100%,其中89%患者达到≥VGPR。在未接受过BCMA和GPRC5D治疗的患者中,ORR为100%。细胞因子释放综合征(CRS)多为1级(无≥3级事件),支持每4周一次皮下给药,其安全性优于部分双特异性抗体。
IBI3003(GPRC5D × BCMA × CD3)已获得FDA快速通道资格。SIM0500、PIT565等其他候选药物也在推进中,显示出克服双特异性抗体耐药的潜力。
 研究中的关键靶点组合
研究中的关键靶点组合
CD19 × CD3(blinatumomab)
作为BiTE平台的基础产品,主要用于复发/难治性B细胞急性淋巴细胞白血病(R/R B-ALL)。其机制是通过低亲和力CD3结合重定向T细胞,形成免疫突触并诱导肿瘤细胞凋亡。这一组合奠定了BiTE平台的临床基础,是多特异性抗体从概念走向实践的里程碑。
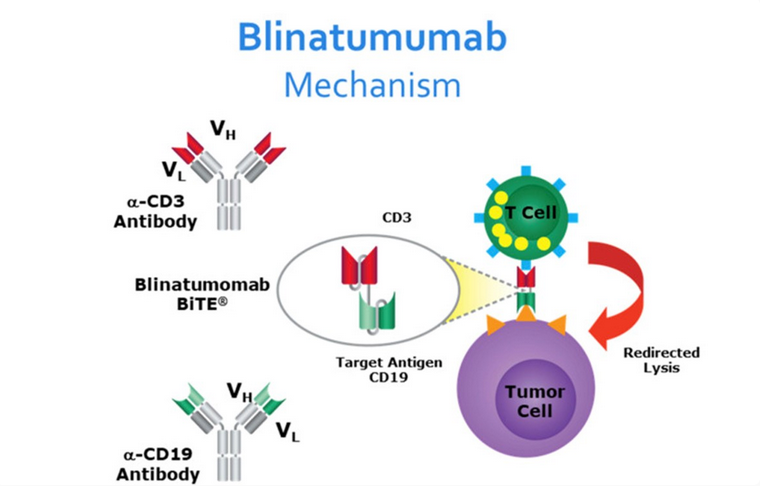 图3. blinatumomab的作用机制
图3. blinatumomab的作用机制BCMA × CD3(teclistamab、elranatamab、linvoseltamab)
BCMA是多发性骨髓瘤(MM)浆细胞表面高表达的核心靶点。这些双特异性抗体通过T细胞重定向实现高效肿瘤杀伤,在三线或后线暴露的RRMM中显示出强劲疗效。该靶点类药物有效应对BCMA表达的异质性,成为RRMM标准治疗的重要补充。
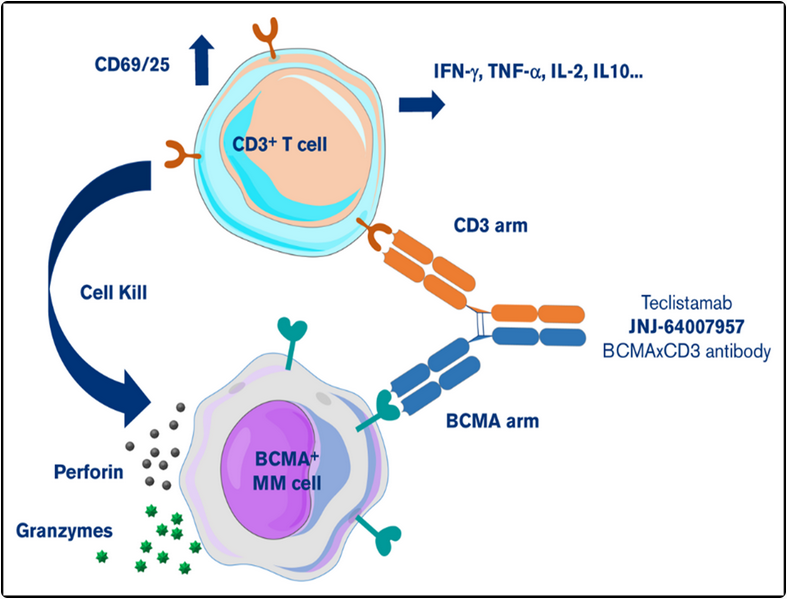 图4. teclistamab的作用机制
图4. teclistamab的作用机制CD20 × CD3(glofitamab、epcoritamab)
针对B细胞淋巴瘤(尤其是DLBCL和FL),采用2:1不对称结构(一个CD20臂、两个CD3臂),以增强对低密度CD20抗原的亲和力,同时保留Fc介导的效应功能。该组合通过双靶点桥接有效克服CD20表达下调导致的逃逸,已成为二线治疗后B细胞恶性肿瘤的重要选择。
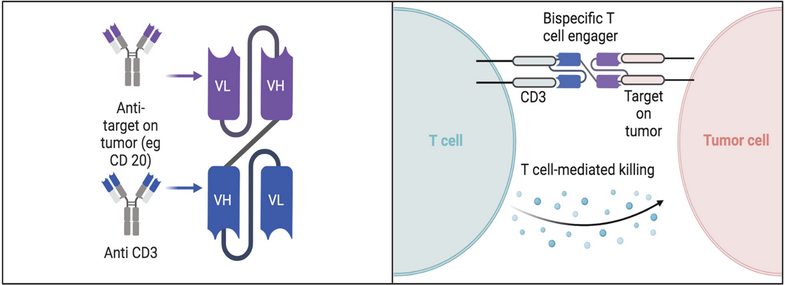 图5. 双特异性抗体的作用机制
图5. 双特异性抗体的作用机制GPRC5D × CD3(talquetamab)
GPRC5D是MM的一种新型表面标志物,在BCMA耐药或低表达患者中表达尤为显著,可有效应对抗原丢失。Monumental-1试验确认,talquetamab在三线或后线RRMM患者中取得显著疗效,尤其适用于既往BCMA靶向治疗失败的患者。该靶点与BCMA互补,形成“双保险”策略,进一步拓展了MM的治疗格局。
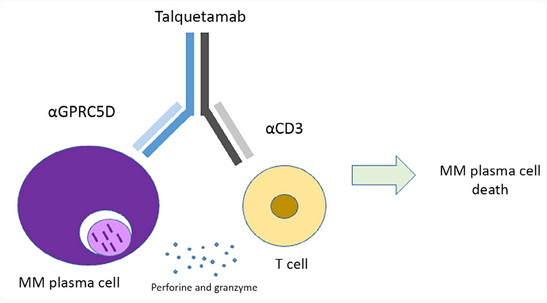 图6. Talquetamab通过同时结合T细胞CD3和浆细胞GPRC5D,介导T细胞活化并杀伤多发性骨髓瘤细胞
图6. Talquetamab通过同时结合T细胞CD3和浆细胞GPRC5D,介导T细胞活化并杀伤多发性骨髓瘤细胞 典型三特异性示例:BCMA × GPRC5D × CD3(JNJ-79635322/JNJ-5322,又称ramantamig)
双TAA+CD3设计同时靶向BCMA和GPRC5D,显著提升肿瘤覆盖范围并降低抗原逃逸风险,同时采用低亲和力CD3结构域优化安全性。在一项针对RRMM患者(中位既往4线治疗)的I期试验中,RP2D(100
mg Q4W)达到86%的ORR(75% ≥VGPR)。在未接受过BCMA和GPRC5D治疗的亚组中,ORR达100%(89%
≥VGPR),所有患者均维持缓解(中位随访8.5个月)。CRS以1级为主(无≥3级事件),支持每月一次皮下给药,其安全性优于多数双特异性抗体。该设计代表了多特异性抗体的下一代范式,有望以“现成”形式实现类似CAR-T的疗效,并适合门诊治疗。
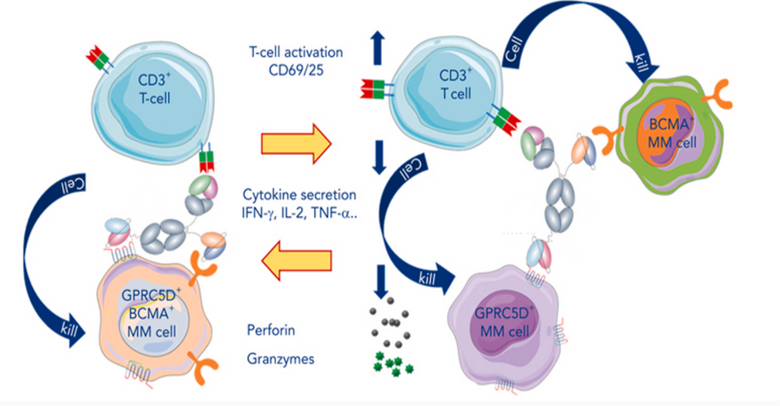 图7. 三特异性抗体募集T细胞至肿瘤细胞
图7. 三特异性抗体募集T细胞至肿瘤细胞 安全性、耐药挑战及优化策略
安全性、耐药挑战及优化策略
在双特异性和三特异性抗体的临床转化过程中,安全性和药物耐药仍是需要重点优化的领域。常见的免疫相关不良反应包括细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)以及骨髓抑制导致的血细胞减少。
通过阶梯式给药、Fc沉默设计、可被蛋白酶激活的掩蔽肽以及低亲和力CD3结合结构域等先进工程策略,这些毒性已得到显著缓解,大多数患者能够良好耐受治疗。
耐药的主要驱动因素是肿瘤细胞靶抗原丢失和效应T细胞耗竭。未来应对策略包括BsAbs/TsAbs与CELMoD(cereblon E3连接酶调节剂)药物联合、与PD-1免疫检查点抑制剂协同,或进一步开发四特异性抗体平台,以实现多维度免疫激活和肿瘤微环境重塑。
 未来展望
未来展望
三特异性抗体及下一代多特异性抗体正从血液肿瘤快速扩展至实体瘤。固定疗程治疗、便捷的皮下注射方案,以及与抗体-药物偶联物(ADC)和个性化肿瘤疫苗的联合疗法,有望成为主流方向。未来预计将有更多TsAbs获得FDA等监管机构的完全批准,全面开启精准癌症免疫治疗的“多靶点协同”时代,为癌症患者提供更持久、更有效的治疗选择。

参考文献:
1.
Chennapragada SS, Ramadas P. Bispecific Antibody Toxicity. [Updated
2024 Apr 20]. In: StatPearls [Internet]. Treasure Island (FL):
StatPearls Publishing; 2026 Jan-.
2.
Abou Dalle, I., Dulery, R., Moukalled, N. et al. Bi- and Tri-specific
antibodies in non-Hodgkin lymphoma: current data and perspectives. Blood
Cancer J. 14, 23 (2024).
3.
Wen J, Cui W, Yin X, Chen Y, Liu A, Wang Q, Meng X. Application and
future prospects of bispecific antibodies in the treatment of non-small
cell lung cancer. Cancer Biol Med. 2025 Apr 7;22(4):348–75. doi:
10.20892/j.issn.2095-3941.2024.0470 . PMID: 40192238; PMCID:
PMC12032835.
4.
Verma V, Sharma G. Bispecific antibodies in clinical practice:
Understanding recent advances and current place in cancer treatment
landscape. Clin Exp Med. 2024 Nov 28;25(1):11. doi:
10.1007/s10238-024-01520-y . PMID: 39607562; PMCID: PMC11604778.
5.
Wei J, Yang Y, Wang G and Liu M (2022) Current landscape and future
directions of bispecific antibodies in cancer immunotherapy. Front.
Immunol. 13:1035276. doi: 10.3389/fimmu.2022.1035276
6.
Amoozgar B, Bangolo A, Habibi M, Cho C, Goy A. From Molecular Precision
to Clinical Practice: A Comprehensive Review of Bispecific and
Trispecific Antibodies in Hematologic Malignancies. Int J Mol Sci. 2025
Jun 1;26(11):5319. doi: 10.3390/ijms26115319 . PMID: 40508128; PMCID:
PMC12154751.
7.
Runcie K, Budman DR, John V, Seetharamu N. Bi-specific and tri-specific
antibodies- the next big thing in solid tumor therapeutics. Mol Med.
2018 Sep 24;24(1):50. doi: 10.1186/s10020-018-0051-4 . PMID: 30249178;
PMCID: PMC6154901.
8.
Chao Z, Mei Q, Yang C, Luo J, Liu P, Peng H, Guo X, Yin Z, Li L, Wang
Z. Immunological synapse: structures, molecular mechanisms and
therapeutic implications in disease. Signal Transduct Target Ther. 2025
Aug 11;10(1):254. doi: 10.1038/s41392-025-02332-6 . PMID: 40784895;
PMCID: PMC12336355.