103616-89-3
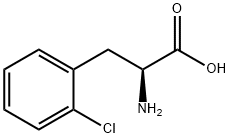 103616-89-3 结构式
103616-89-3 结构式
基本信息
(S)-2-氨基-3-(2-氯苯基)丙酸
2-氯-L-苯丙氨酸
2-氯-L-苯基丙氨酸, 98+%
2-Chloro-L-Phenylalanine HCl
(S)-2-amino-3-(2-chlorophenyl)propanoic acid
2-Chloro-L-phenylalaninehydrocloride
(2R)-2-amino-3-(2-chlorophenyl)propanoic acid
2-CHLORO-L-PHENYLALANINE HYDROCHLORIDE
L-H-Phe(2-Cl)-OH
3-(2-Chlorophenyl)-L-alanine
2-CHLORO-PHE-OHHCL 98%MIN
2-Chloro-L-phenylalanine
2-Chloro-L-phenylalanine, 98+%
H-Phe(2-Cl)-OH L-2-Chlorophe
L-2-Chloro-phe-OH
物理化学性质
制备方法
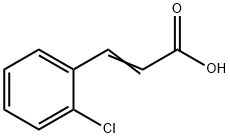
3752-25-8

103616-89-3
以2-氯肉桂酸为原料合成L-2-氯苯丙氨酸的一般步骤如下:首先,根据Rhodosporidium toruloides ATCC 10788的苯丙氨酸氨基裂解酶(PAL)蛋白质序列(NCBI蛋白质数据库编号CAA31209),由Genscript Corporation合成R. glutinis的PAL基因,并进行密码子优化以适应大肠杆菌表达。合成的PAL基因通过Genscript连接到pUC57载体的SmaI位点,构建成pUC57_PAL质粒。将5μg冻干的pUC57_PAL质粒溶解于50μl MilliQ水中,取1μl溶液转化大肠杆菌DH5α化学感受态细胞,按照供应商的协议进行操作。转化后的细胞在含有100μg/ml羧苄青霉素的LB固体培养基上于37℃过夜培养。挑选单一菌落接种于20ml含100μg/ml羧苄青霉素的LB液体培养基中,制备8%甘油的菌液并保存于-80℃。将含有pUC57_PAL的DH5α菌株接种于1000ml含100μg/ml羧苄青霉素的LB培养基中,28℃过夜培养。随后,将培养物接种于10升TB培养基(含0.1g/l羧苄青霉素和1mM IPTG)中,37℃搅拌发酵9.5小时,转速500至1500rpm。通过离心收集细胞,获得230g湿细胞,分装成10g等分试样储存于-20℃。反应前,将适量细胞解冻并重悬于冷水中。将1.8g(10mmol)3-(2-氯苯基)-丙烯酸溶于0.5L 13vol%氨水溶液中,用25w/w% H2SO4调节pH至11。将130g湿细胞重悬于0.2L pH11的13vol%氨水溶液中,与底物溶液混合,总体积调节至1L。反应在30℃、200rpm的密闭容器中进行。初始1小时内,每5分钟加入0.91g(5.0mmol)3-(2-氯苯基)-丙烯酸,随后7小时内每25分钟加入相同量。8.5小时后,离心去除细胞,HPLC测定反应产率约91%,得到约18.1g(91mmol)2-氯苯丙氨酸。上清液(850mL,pH10.8)减压浓缩(150至10mbar,60℃),去除约65%水后形成沉淀(pH7.5)。过滤沉淀,水洗去除无机盐,干燥得14.9g产物,其中含57w/w% N-氨基-3-(2-氯苯基)-丙酸(8.5g,47%产率),24w/w%水和1.7w/w% 3-(2-氯苯基)-丙烯酸。(S)-2-氨基-3-(2-氯苯基)-丙酸的对映体过量(e.e.)为99%。母液中剩余9.5g (S)-2-氨基-3-(2-氯苯基)-丙酸。
参考文献:
[1] Patent: EP1676838, 2006, A1. Location in patent: Page/Page column 17-18
[2] Patent: WO2006/69799, 2006, A1. Location in patent: Page/Page column 30-31
[3] Journal of the American Chemical Society, 2015, vol. 137, # 40, p. 12977 - 12983
[4] Catalysis Science and Technology, 2016, vol. 6, # 12, p. 4086 - 4089
