142356-33-0
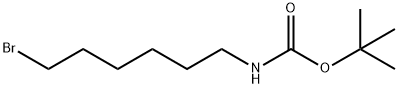 142356-33-0 结构式
142356-33-0 结构式
基本信息
N-BOC-6-溴代己胺
6-(BOC-氨基)己基溴
6-(BOC-氨基)溴己烷
6-(叔丁氧羰基氨基)溴己烷
N-叔丁氧羰基-6-溴己基胺
N-BOC-6-溴代己胺 1G
(6-溴己基)氨基甲酸 叔丁酯
N-(6-溴己基)氨基甲酸叔丁酯
N-BOC-6-溴代己胺TERT-BUTYL (6-BROMOHEXYL)CARBAMATE
N-Boc-6-BroMohexylaMin
N-BOC-6-BROMO-HEXYLAMINE
ert-Butyl(6-bromohexyl)carbamate
tert-butyl 6-broMohexylcarbaMate
N-Boc-6-Bromohexylamine≥ 95% (NMR)
6-(Boc-amino)hexyl bromide >=97.0% (GC)
N-(tert-Butoxycarbonyl)-6-broMohexylaMine
(6-Bromo-hexyl)-carbamic acid tert-butyl ester
N-(6-BroMohexyl)carbaMic Acid 1,1-DiMethylethyl Ester
物理化学性质
制备方法
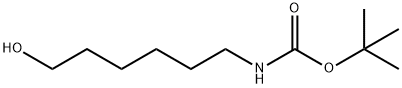
75937-12-1

142356-33-0
6-(BOC-氨基)-1-己醇 为原料合成 N-BOC-6-溴代己胺一般步骤:向溶解在1:1二恶烷/水混合物(12 mL)中的6-(BOC-氨基)-1-己醇(0.500 g,2.82 mmol,1当量)中加入K2CO3(1.870 g,13.56 mmol,4当量),并在室温下搅拌10分钟。随后,向混合物中加入二碳酸二叔丁酯(0.7 mL,3.39 mmol,1.2当量),并继续搅拌过夜。反应完成后,用EtOAc(12 mL)稀释反应混合物,分离有机层。有机层依次用10% HCl(2×10 mL)洗涤,用MgSO4干燥,然后真空浓缩。得到产物0.570 g(2.62 mmol,收率93%),无需进一步纯化即可用于下一步。薄层色谱(TLC)显示Rf值为0.50(硅胶,60% EtOAc/Hex)。1H NMR(400 MHz,CDCl3)δ: 4.51(br s,1H),3.61(t,J = 6.5 Hz,2H),3.09(t,J = 6.7 Hz,2H),1.42(s,9H),1.55-1.30(m,8H)ppm。13C NMR(100 MHz,CDCl3)δ: 156.1,79.0,62.7,40.4,32.6,30.1,28.4,26.4,25.3 ppm。NMR谱图与文献报道一致[41]。 接下来,向溶解在无水二氯甲烷(14 mL)中的6-(叔丁氧基羰基氨基)己-1-醇(0.600 g,2.76 mmol,1当量)中加入CBr4(0.920 g,2.76 mmol,1当量)和PPh3(0.720 g,2.76 mmol,1当量),在0℃下反应。反应混合物在2小时内缓慢升温至室温。反应完成后,将混合物真空浓缩,并通过柱色谱法纯化,得到产物0.696 g(2.48 mmol,收率90%)。薄层色谱(TLC)显示Rf值为0.57(硅胶,20% EtOAc/Hex)。1H NMR(400 MHz,CDCl3)δ: 4.48(br s,1H),3.66(t,J = 6.8 Hz,2H),3.09(t,J = 6.5 Hz,2H),1.88-1.82(m,2H),1.47(s,9H),1.54-1.18(m,6H)ppm。13C NMR(100 MHz,CDCl3)δ: 156.1,62.9,51.1,32.8,28.5,26.4,25.4 ppm。NMR谱图与文献报道一致[42]。
参考文献:
[1] Helvetica Chimica Acta, 1993, vol. 76, # 2, p. 884 - 892
[2] Biochimica et Biophysica Acta - General Subjects, 2016, vol. 1860, # 3, p. 486 - 497
[3] ACS Medicinal Chemistry Letters, 2017, vol. 8, # 5, p. 510 - 515
[4] Bioorganic and Medicinal Chemistry Letters, 2005, vol. 15, # 18, p. 4033 - 4036
[5] Patent: WO2015/77503, 2015, A1. Location in patent: Paragraph 00400
