211915-06-9
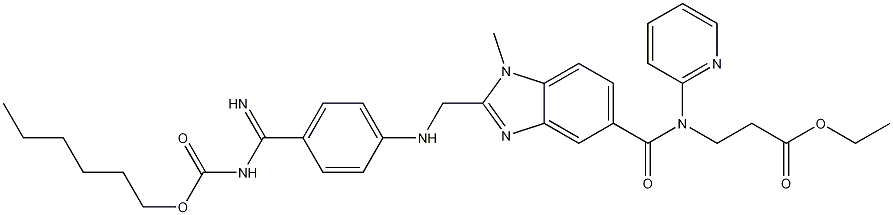 211915-06-9 结构式
211915-06-9 结构式
基本信息
达比加群酯
达比加群酯 1G
达比加群酯自由碱
达比加群酯杂质(全套)
甲磺酸达比加群-中间体3
ETEXILATE达比加群
原研代码CDBA510BS
N-[2-[4-[N-(己氧基羰基)氨基]苯氨基甲基]-1-甲基-1H-苯并咪唑-5-基羰基]-N-(2-吡啶)-BETA-丙氨酸乙酯
3-[[[2-[[[4-[[[( 己氧基) 羰基] 氨基] 亚氨甲基] 苯基] 氨基] 甲基]-1- 甲基-1H- 苯并咪唑-5-基] 羰基]( 吡啶-2- 基) 氨基] 丙酸乙酯
BIBR-1048
BIBR 1048
BIBR-1048, >=99%
Dabigatran etexilate
Pradaxa (dabigatran)
BIBR-1048(Dabigatran etexilate)
Dabigatran Etexilate (free base)
Ethyl 3-(2-((4-(N-(hexyloxycarbonyl)carbamimidoyl)phenylamino)methyl)-1-methyl-N-(pyridin-2-yl
N-[2-[4-[N-(Hexyloxycarbonyl)aMidino]phenylaMinoMethyl]-1-Methyl-1H-benziMidazol-5-ylcarbonyl]-N-(2-
物理化学性质
安全数据
应用领域
制备方法
![N-[[2-[[[4-(氨基亚氨基甲基)苯基]氨基]甲基]-1-甲基-1H-苯并咪唑-5-基]羰基]-N-2-吡啶基-BETA-丙氨酸乙酯 4-甲基苯磺酸盐](/CAS/GIF/872728-85-3.gif)
872728-85-3
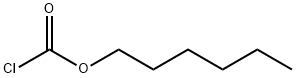
6092-54-2

211915-06-9
以N-[[2-[[[4-(氨基亚氨基甲基)苯基]氨基]甲基]-1-甲基-1H-苯并咪唑-5-基]羰基]-N-2-吡啶基-β-丙氨酸乙酯 4-甲基苯磺酸盐和氯甲酸正己酯为原料,合成3-(2-(((4-(N-((己基氧基)羰基)氨基甲酰基)苯基)氨基)甲基)-1-甲基-N-(吡啶-2-基)-1H-苯并[d]咪唑-5-甲酰胺基)丙酸乙酯的一般步骤如下:参照实施例-2中达比加群酯游离碱的制备方法,将1-甲基-2-[N-(4-脒基苯基)-氨基甲基]-苯并咪唑-5-基-羧酸-N-苯基-N-(2-乙氧基羰基乙基)-酰胺的p-TSA盐(20g)悬浮于乙腈(80mL)中,于27℃下搅拌。向此悬浮液中加入碳酸钾(24.7g)的DM水(50mL)溶液,继续搅拌30分钟。随后将反应混合物冷却至12-15℃,加入氯甲酸正己酯(4.9g),搅拌30分钟。将反应温度升至17℃,再搅拌30分钟。加入第二批氯甲酸正己酯(1.49g),通过HPLC监测反应进度,待反应完成后,于16-20℃下继续搅拌1小时。加入DM水(50mL),于30℃下保持15分钟。过滤收集沉淀,用水洗涤,50℃真空干燥,得到达比加群酯,为灰白色固体(16.4g,HPLC纯度>96%)。
参考文献:
[1] Patent: EP1609784, 2005, A1. Location in patent: Page/Page column 10
[2] Patent: WO2015/33353, 2015, A2. Location in patent: Page/Page column 13; 14
常见问题列表
达比加群酯是继华法林之后美国食品与药品管理局批准的又一种新型口服抗凝血药物,属非肽类的凝血酶抑制剂,通过特异性和选择性地阻断凝血酶(游离型或结合型)的活性而发挥抗凝效果。具有可以口服、强效、无需特殊用药监测、药物相互作用少等特点,是抗凝血治疗领域和潜在致死性血栓预防领域的一项重大进展,具有里程碑意义。口服经胃肠吸收后,在体内转化为具有直接抗凝血活性的达比加群,通过结合于凝血酶的纤维蛋白特异结合位点,阻止纤维蛋白原裂解为纤维蛋白,从而阻断了凝血瀑布网络的最后步骤及血栓形成。达比加群还可以从纤维蛋白一凝血酶结合体上解离,发挥可逆的抗凝作用。
在2009年欧洲心脏病学会年会上,德国勃林格殷格翰公司首次公布迄今为止最大型的房颤转归临床试验-RE-LY(新型凝血酶直接抑制剂达比加群酯长期抗凝治疗的随机评价)研究数据。结果显示:与良好对照的华法林治疗组相比,达比加群酯可显著降低卒中和栓塞性疾病(包括出血性卒中)的风险,显著降低出血(包括致命性出血和颅内出血)的发生,显著降低血管死亡率。研究结果还表明,达比加群酯提供了有效、稳定的抗凝效果,无需常规监测凝血功能和调整用药剂量。
ChemicalBook MaggieQ 编辑
2008年4月达比加群酯首先在德国和英国上市,随后在40多个国家获准上市并广泛应用于择期全髋/膝关节置换术后患者深静脉血栓的一级预防。
2010年10月,美国食品与药品管理局FDA正式批准达比加群酯上市销售,适应症为心房颤动(AF)引发的中风预防。
AF是最常见的心律失常之一,在所有年龄人群中发病率达1%,在80岁以上人群中发病率达10%。它几乎见于所有的器质性心脏病,在非器质性心脏病也可发生。医学界普遍认为,由房颤(AF)导致中风的预防用药有很大的市场机会,前景广阔。
2012年11月2日,FDA发布信息指出已经对使用抗凝剂(血液稀释剂)达比加群酯(Pradaxa)和华法林可能存在严重出血风险的新信息进行了评估。这项风险评估采用的是FDA哨点行动(Sentinel Initiative) Mini-Sentinel监测系统的医疗保险补偿和管理数据。此次评估结果显示,与新使用达比加群酯相关的出血率并未高于与新使用华法林相关的出血率,这与批准达比加群酯时依据的大规模临床试验(RE-LY试验)观察结果相吻合。FDA关于这个问题的安全调查仍在进行当中,正在继续评估多方来源的数据。
2013年3月,美国食品和药品管理局(FDA)在《新英格兰医学杂志》上发表的最新述评指出,2012年11月所开展的小规模前哨评估之后,FDA作为药监部门并未改变其针对泰毕全®(达比加群酯)所作出的推荐。FDA指出,并未观察到与新近使用泰毕全®相关的出血事件发生率高于与新近使用华法林相关的出血发生率,这与核心研究RE-LY®中所观察到的结果保持一致。
2013年5月,德国勃林格殷格翰公司生产的新型口服抗凝药泰毕全®已获我国国家食品药品监督管理局颁发的进口药品注册证,即将在国内上市。
直接凝血酶抑制剂通过特异性阻滞凝血酶(游离型和结合型)活性而发挥强大抗凝疗效,凝血酶是血栓形成过程中的具有核心作用的酶。与作用于不同凝血因子的维生素K拮抗剂不同,达比加群酯可提供有效的、可预测的、稳定的抗凝效果,同时较少发生药物相互作用,无药物食物相互作用,无需常规进行凝血功能监测或剂量调整。
达比加群酯的临床使用经验已经超过了所有其他新型口服抗凝药物,该药在全球80多个国家中各种注册适应症的用药已经超过了一百四十万患者年。
达比加群酯出血风险和肾功能评估:依据达比加群酯上市后严重出血事件的报告,以及老年患者和出血高危患者或肾功能损害患者的使用情况,对产品专论的内容做了更新。目前更新后的内容包括,建议对考虑使用或已经使用达比加群酯治疗的患者要进行肾功能评估,具体内容如下:
开始用达比加群酯治疗前,所有患者都要通过计算肌酐清除率(CrCl)评估肾功能,以排除重度肾功能损害(即CrCl<30毫升/分钟);达比加群酯治疗期间,如果临床上有怀疑肾功能快速减退或迅速恶化的情况(如血容量不足、脱水以及同时使用某些药物),要复查肾功能。
这些临床情况可能导致达比加群酯的暴露量增加;老年(>75岁)患者或中度肾功能损害(CrCl30~50毫升/分钟)的患者,要通过计算肌酐清除率评估肾功能,每年至少1次。
给医疗专业人员的建议:
达比加群酯禁用于重度肾功能损害(CrCl<30毫升/分钟)的患者;
出血高危患者也不要使用达比加群酯;
要对患者进行临床监测,注意有无出血或贫血的表现;
如果发生严重出血,应停用达比加群酯,并查明出血部位。
对心脏瓣膜疾病患者的建议:
达比加群酯的安全性和有效性尚未在血流动力学上有明显风湿性心脏瓣膜病表现(特别是二尖瓣狭窄)的患者或有人工心脏瓣膜的患者中进行研究。没有数据支持达比加群酯在安装人工心脏瓣膜的患者(无论是否有心房纤颤)中具有充分的抗凝效果,因此,达比加群酯不宜用于血流动力学上有明显风湿性心脏瓣膜病表现的患者或有人工心脏瓣膜的患者。
| Target | Value |
| Thrombin |
Dabigatran选择性的,可逆的抑制人凝血酶(Ki: 4.5 nM)和凝血酶诱导的血小板聚集(IC50: 10 nM),对其它血小板刺激试剂没有抑制效果。Dabigatran抑制匮乏血小板的血浆中(PPP)凝血酶的产生,通过內源凝血酶指数(ETP)测定的IC50 是0.56 μM。在体外实验中,Dabigatran对各种物种具有浓度依赖性抗凝血作用。在人类PPP中,在浓度分别是0.23,0.83 和0.18 μM时,加倍活化部分凝血活酶时间(aPTT),前凝血酶时间(PT) 和Ecarin 凝固时间(ECT)。。
