46258-62-2
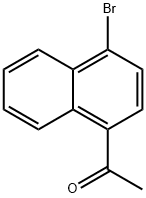 46258-62-2 结构式
46258-62-2 结构式
基本信息
1-(4-溴萘-1-基)乙酮
1-(4-溴-1-萘基)乙酮
1-(4-溴萘-1-基)乙-1-酮
4-Bromo-1-acetonaphthone
4'-Bromo-1'-acetonaphthone
4-broMo-1-acetylnaphthalene
1-Acetyl-4-bromonaphthalene
1-(4-Bromo-1-naphthyl)ethanone
1-(1-BROMONAPHTHALEN-4-YL)ETHANONE
1-(4-Bromonaphthalen-1-yl)ethanone
1-(4-bromononaphthalen-4-yl)ethanone
1-(4-Bromonaphthalen-1-yl)ethan-1-one
物理化学性质
制备方法
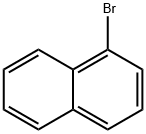
90-11-9
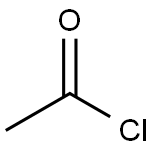
75-36-5

46258-62-2
1. 在0℃下,将1-溴代萘(10g,48.3mmol)和乙酰氯(4.2ml,58mmol)溶于1,2-二氯乙烷(100ml)中,分批加入氯化铝(14.4g,108mmol)。 2. 将反应混合物在室温下搅拌24小时。 3. 将反应混合物倒入冰水(100ml)中,分离有机层和水层。 4. 水层用乙醚(3×150ml)萃取,合并有机层并用硫酸镁干燥。 5. 过滤后,减压除去溶剂,得到橙色油状物。 6. 通过快速色谱法(环己烷/乙酸乙酯:95/5)纯化,得到1-(4-溴-1-萘基)乙酮,为黄色油状物(收率91%)。 7. 按照类似化合物22的制备方法,将1-(4-溴-1-萘基)乙酮转化为其肟衍生物,得到白色粉末(收率98%)。 8. 将活化的锌粉(24.7g,379mmol)分批加入到肟(10.0g,37.9mmol)的乙酸(40ml)悬浮液中,室温搅拌2小时。 9. 过滤去除锌粉,减压除去乙酸。 10. 加入水(100ml),用1N NaOH调节pH至13。 11. 水层用EtOAc(3×100ml)萃取,合并有机层并用MgSO4干燥。 12. 过滤后,减压除去溶剂,得到黄色油状物(收率70%)。 13. 将Boc2O(7.1g,31.8mmol)加入到胺(6.6g,26.5mmol)的1,4-二恶烷(50ml)溶液中,室温搅拌2小时。 14. 减压除去溶剂,通过快速色谱法(环己烷/EtOAc:95/5)纯化,得到黄色粉末(收率75%)。 15. 将溴化物(350mg,1mmol)溶于THF(13ml)/水(2ml)中,加入乙酸钾(100mg,1mmol)、1,3-双(二苯基膦基)丙烷(9.0mg,0.02mmol)和钯(II)乙酸酯(9.0mg,0.04mmol)。 16. 在50atm CO压力和150℃下搅拌3小时。 17. 过滤反应混合物,滤液用MgSO4干燥,减压除去溶剂,得到黄绿色油状物(300mg)。 18. 通过快速色谱(DCM/MeOH:90/10)纯化,得到4-(1-叔丁氧基羰基氨基乙基)-萘-1-羧酸,为白色粉末(收率14%)。 19. 按照化合物31的程序,从4-(1-叔丁氧基羰基氨基乙基)-萘-1-羧酸(44mg)和4-氨基吡啶出发,制备标题产物(收率67%)。 NMR数据(300MHz,DMSO-d6):δ 1.64(d,3H,J=6.6Hz);5.3(q,1H,J=6.5Hz);7.71(m,1H);8.00(d,1H,J=7.7Hz);8.32(m,1H);8.35(d,1H,J=7.3Hz);8.81(d,2H,J=7.2Hz);12.2(s,1H)。
参考文献:
[1] Patent: WO2005/82367, 2005, A1. Location in patent: Page/Page column 64-65
[2] Patent: US2011/152246, 2011, A1. Location in patent: Page/Page column 110; 111
[3] Canadian Journal of Chemistry, 1981, vol. 59, p. 2629 - 2641
[4] Canadian Journal of Chemistry, 1995, vol. 73, # 6, p. 885 - 895
[5] Bioorganic and Medicinal Chemistry, 2012, vol. 20, # 6, p. 2067 - 2081
