7782-49-2
 7782-49-2 结构式
7782-49-2 结构式
物理化学性质
安全数据
toxic compounds or compounds which causing chronic effects
Acute Tox. 3 Oral
Aquatic Chronic 4
STOT RE 2
应用领域
制备方法
二氧化硫还原法在搅拌下,向浓度为170g/L的二氧化硒水溶液(亚硒酸溶液,Se为130 g/L),通入经水和稀硫酸洗涤的二氧化硫气体,在75℃充分搅拌下进行还原反应,可得到200目以上六方结晶黑色微细硒粉末。
氨气还原法 将二氧化硒的蒸气用氨气在450~500℃进行还原反应,制得硒粉末。其
3SeO2+4NH3→3Se+6H2O+2N2
将原料纯度为99.9%的硒粉,通过熔盐法提纯,可提高到99.99%。亦可用真空蒸馏法提纯。
7782-49-2(安全特性,毒性,储运)
常见问题列表
硒是一种非金属(或半金属)元素(也称为准金属)。 它属于元素周期表的第16组(VIA组),位于硫和碲之间。硒有多种同素异形体形式,包括灰色,红色和黑色硒。它主要存在于其他金属的硫化矿石中,并作为副产物获得(例如从电解精炼中的阳极污泥中获得)。
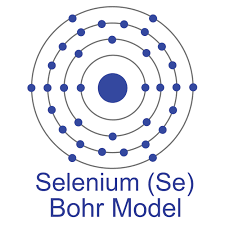
硒是Berzelius和Gahn在1817年研究铅制硫酸法的过程中发现的。他们最初认为,铅室底部产生令人讨厌的气味的原因是碲的存在,碲是35年前发现的硫族元素。进一步的研究表明了一种新元素,其化学性质与碲非常相似。这个新元素被命名为硒,源于希腊词selene,意为月亮。该名称沿用tellus,碲在化学上类似于新元素的拉丁词,代表碲。威洛比·史密斯(Willoughby Smith)在1873年发现了这种金属的光阻性,即随着金属上的曝光强度增加,其电流电阻降低。
硒是地壳中第67个最丰富的元素。它广泛分布在地球上,但并不大量存在。硒共有35个同位素。 其中五个是稳定的,第六个同位素的半衰期很长,因此也被认为是稳定的:Se-82 = 0.83×10 + 20年。 第六种同位素构成了地壳中硒丰度的8.73%,其他五个稳定同位素构成了地球上硒丰度的其余部分。作为一种游离元素,通常会与元素硫一起发现。 仅有一种含硒的矿物矿石:辉石(CuAgSe)。尽管硒含量丰富,但太稀少了,无法用于商业用途。几乎所有的硒都从铜的加工过程中以及作为硫酸的生产回收的剩余污泥副产品。这使硒的回收有利可图。 硒存在于墨西哥,波斯尼亚,日本和加拿大。在许多国家的某些土壤中,其可回收量中都可以找到它。

硒具有许多工业用途,尤其是电子和固态应用,近年来,这种用途已显着增加。这归因于其独特的特性:(1)将光直接转换为电(光伏作用); (2)其电阻随着照明度(光电导率)的增加而降低; (3)能够将交流电转换成直流电。
硒用于光电电池,太阳能电池,并用作收音机和电视机的整流器。从历史上看,它也用于摄影的曝光计中,并用作调色浴的成分。用于复印文档。在玻璃工业中,它被掺入颜料中使粉红色,橙色和红宝石色玻璃着色。其他应用还可以用作制备电弧光电极的金属基底。作为不锈钢的添加剂;在镀铬槽中诱导微裂纹以控制腐蚀;橡胶硫化;作为催化剂;以及用作配电盘电缆的阻燃剂。 尽管是有毒金属,但微量的硒是营养元素。添加到牛粮中的微量元素可有效抵抗绵羊和牛的肌肉营养不良。
在电解精炼铜时,会从阳极泥或煤泥中回收硒。阳极泥用硫酸处理并烘烤。硒转化为二氧化硫,然后蒸发并收集在湿式洗涤器系统中。 或者,用热稀硫酸给未加工的阳极泥充气,以去除铜。然后将粘液与碳酸钠充分混合,并在足够的空气中烘烤。将形成的硒酸钠用水浸出。将盐酸添加到该硒酸盐溶液中。用二氧化硫处理会沉淀出元素硒。或者,将硒酸盐溶液蒸发至干。通过在高温下与碳加热将硒酸钠还原为硒化钠。硒酸钠用水浸出。空气吹过溶液。硒被氧化成元素硒,然后沉淀。
应使患者离开污染区,安置休息并保暖。眼睛受刺激用水冲洗,并就医诊治。皮肤接触先用水冲洗,再用肥皂彻底洗涤,如灼伤须就医诊治。误服立即漱口,急送医院救治。
| 报价日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
| 2026/03/03 | A12592 | 硒粉 Seleniumpowder | 7782-49-2 | 1000g | 4751元 |
| 2026/03/03 | 045115 | 硒 锭/块, ≈38mm (1.5in) 直径 Selenium ingot/button,≈38mm (1.5 in.) dia., Thermo Scientific Chemicals | 7782-49-2 | 1pc | 906元 |
| 2026/03/03 | 036208 | 硒粉, -200 目, 99.999% (metals basis) Selenium powder, -200 mesh, 99.999% (metals basis), Thermo Scientific Chemicals | 7782-49-2 | 50g | 4374元 |

