【背景及概述】[1][2][3]
半导体是一种导电能力介于绝缘体和金属的材料,可分为两种:一种是元素半导体(Ⅵ族元素),另一种是化合物半导体(Ⅱ族和Ⅵ族化合物或者Ⅲ族和Ⅴ族元素化合而成)。基于半导体材料特殊的载流子输运机制及其光电特性,使其在发光二极管(LED)、激光二极管(LD)、紫外探测器(UV-photodetector)、场效应晶体管(FET)、金属-绝缘体-半导体场效应晶体管(MISFET))和单片微波集成电路(MMIC)等半导体器件领域得到广泛应用。近年来,一些铜系化合物材料(如CuO、Cu2O、CuSCN、CuI等)由于具有简单的制备技术和特殊的半导体物理性能,开始受到人们的广泛关注。由于晶体内部存在点缺陷(铜空位),这些材料表现出优异的p型导电特性。其中,CuI是直接宽禁带半导体材料,禁带宽度3.1e V,具有很高的激子束缚能(62me V);同时,CuI具有较小的空穴有效质量,因此CuI具有较高的空穴迁移率。此外,CuI还具有透明度高(可见光区)、无毒、储量丰富、成本低廉的优点。
【结构】[2]
CuI 的晶体结构与温度和压强有关。CuI 在温度低于 643K 呈闪锌矿结构(γ-CuI),在温度介于 643K 和 673K 之间时呈纤锌矿结构(β-CuI),在温度高于673K 时呈面心立方结构(α-CuI)。CuI 各晶体结构之间的熵变为ΔSγ→=1100k Jmol-1K-1,ΔSβ→α=473k Jmol-1K-1。而且,可以通过 X-射线衍射来确定 CuI 闪锌矿结构的极性特点。在 643K 以下,压强在0GPa~1.4GPa 之间,CuI 呈闪锌矿结构;压强在 1.4GPa~4GPa,CuI 呈菱形结构;压强在4GPa~8GPaCuI 呈四方晶系结构:
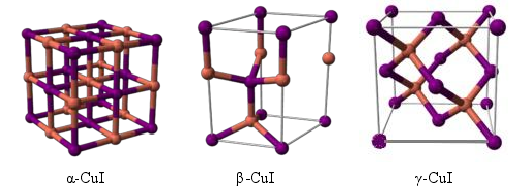
CuI 禁带中也会存在各种本征缺陷能级。例如:铜空位缺陷(VCu),碘空位缺陷(VI),碘间隙缺陷(Ii)和铜间隙缺陷(Cui),OI是氧替换碘缺陷,SI是硫替换碘缺陷。通过利用 LDA-GGA 方法可计算CuI 晶体中不同缺陷的生成焓(ΔHƒ)和单粒子跃迁能级(ε)的数值。
【合成】[1]
碘化亚铜的制备方法较多,如:铜与碘共热;将铜溶解在热浓氢碘酸中;用氢碘酸处理氰化亚铜;将铜与碘仿共热反应;将碘化钾和硫代硫酸钠的混合溶液加到硫酸铜溶液中去等等。虽然碘化亚铜的制备方法较多,但真正在合成上有价值的却不多#在实验室里一般是利用如下反应:

即在水溶液里二价铜离子与碘离子的化合作用最初生成的碘化铜几乎立即被一个氧化还原反应所分解,生成碘化亚铜和游离碘#该反应应该说没有造成环境污染的可能,不过要想将碘完全从产物中除掉是极困难的,一般是用一种还原剂将碘还原掉。如果用一般的除碘方法如萃取法(用四氯化碳)或升华法都是不甚可行的。如当用硫酸铜和碘化钾溶液反应生成碘化亚铜和游离碘后加入四氯化碳萃取,静置后溶液分层,上层为清亮的淡黄色的反应液,下层为紫色的碘的四氯化碳溶液,而白色的极细小的碘化亚铜沉淀则分布在两液相界面和下层萃取液中,其过滤操作复杂,回收率低,而且由于碘没有完全利用,不符合绿色化学中原子经济的要求,所以不可取。
实验室里主要有以下三种方法:
1)用二氧化硫还原
总反应方程式: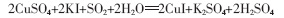

制备:向13.2g无水硫酸铜(纯级)溶于30毫升水的溶液中通入(在通风处)二氧化硫气体使之达饱和,同时在搅拌下分次少量加入由8.7g碘化钾(纯级)所配成的50%碘化钾溶液。起初溶液和所析出的沉淀均呈棕色。但随着二氧化硫的通入,溶液逐渐褪色而沉淀变成白色。用布氏漏斗吸滤出CuI沉淀,并进行洗涤,直到去尽硫酸根离子为止(在洗涤水试样中加入盐酸和氯化钡时,试样不应变浑)。将洗涤过的沉淀置于盛有灼烧过的氯化钙的干燥器中进行干燥,或置于瓷皿中在不超过50℃的温度和搅拌下进行干燥,产量20g(98%)。这种方法利用了二氧化硫的还原性,表面上看是将二价铜盐还原为碘化亚铜,实际上还是生成了碘化亚铜和游离碘,二氧化硫还原的是碘。由于碘化亚铜能溶于碘化钾溶液,故应分次少量地加入碘化钾溶液,使加入的碘化钾溶液都能快速完全地反应掉。由于通入二氧化硫使之饱和,其参与反应时该是过量的,有利于反应向正方向进行,且气体通入时也能起到搅拌作用,增大了反应接触面,具有反应迅速、效果明显的优点。这种制备方法的优点还在于它充分利用了碘,使反应物中的碘全部转化为产物中的碘,符合原子经济概念的要求。
2)用硫代硫酸钠还原
总反应方程式: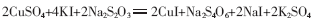
制备:将25g无水硫酸铜放在一只400毫升烧杯中并溶解在150毫升水中,制成溶液,将16.6g碘化钾和25g五水合硫代硫酸钠溶解在100毫升水中来配置第二溶液,将第二溶液在不断搅拌下分次少量地加入溶液。陈化,收集,洗涤,干燥后制得成品。由于过量的碘化物可能溶解产物生成可溶的铜7碘络合物,过量的硫代硫酸钠可能会和铜盐生成铜7硫代硫酸钠络合物,因此将碘化钾7硫代硫酸钠第二溶液加到硫酸铜溶液中去,该法操作简单,没有任何有毒物质参与反应或产生,没有辅助性物质和衍生过程。但是,由于没有充分利用碘,而且除了生成碘化亚铜沉淀,还生成了硫代硫酸钠、电话那和硫酸钾的混合溶液,无法回收利用,因而不符合绿色化学中原子经济的要求。因此从绿色化学的角度看,用硫代硫酸钠还原制备碘化亚铜不是方法。但如果将硫代硫酸钠改为亚硫酸钠,其反应方程式为:
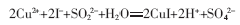
该反应既充分利用碘,还可通过使碘化物与亚硫酸盐的阳离子一致来回收副产物硫酸盐,从而充分利用反应物原子,符合原子经济的要求。
3)用硫酸铜、单质碘与亚硫酸钠反应
总反应方程式: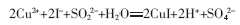
制备:将一定量的碘加到1.3倍计算量的亚硫酸钠溶液中,充分搅拌后加入1.01倍计算量的硫酸铜,不断搅拌下使之迅速反应,然后加热升温至60℃,维持15min,室温静置陈化1h(正交实验得出的反应配比和反应条件)。分离出沉淀,经洗涤,干燥,粉碎,制得产品碘化亚铜。这种方法也可用同样具有还原性的硫代硫酸钠来代替原来的亚硫酸钠进行反应。但实验结果表明,在同样的条件下,硫代硫酸钠的分解严重,产品质量差,这种制备方法反应物及产物无毒无害,制备操作简单,较为合理,由于发生了反应:


生成的碘离子和铜离子反应生成碘化亚铜和游离碘,再由亚硫酸钠还原生成碘,该反应路线循环使用了反应物与生成物;没有碘化钾溶液的滞留从而避免了碘化亚铜沉淀溶解的可能;可以通过调节酸度,回收生成另一产物硫酸钠,得到副产品芒硝,因此反应物原子全部得到利用并且没产生任何废弃物,符合原子经济的要求;没有使用辅助性物质,未产生衍生过程,虽然亚硫酸钠在酸性条件或者是高温时也可能分解释放出二氧化硫有毒气体,但只要操作恰当,反应条件控制适当,是可以避免亚硫酸钠的分解。因此,该方法是较为合理的制备碘化亚铜的方法。
【应用】[1][2]
CuI 作为一种宽禁带直带隙 p 型半导体材料,带隙宽度为 3.1e V,在可见光范围(400nm-760nm)内具有很高的透过率,具有很高的载流子浓度和空穴迁移率,而且制备方法简单易行,耗材损耗少,制备效率高,制备过程无毒无污染,因此在半导体光电器件领域具有广泛的应用前景。
1)CuI 薄膜作为空穴注入层,用于发光二极管(LED)、场效应晶体管。
利用 CuI/Al 复合层可作为有机半导体场效应晶体管的栅电极。CuI作为空穴注入层,可直接与有机半导体层接触。与单层金属(金或铝)作源漏极来比,CuI 降低金属与有机半导体之间的接触势垒,可以提高空穴迁移率,提高载流子的注入和输运效率,提高电流的开关比,还可以急剧降低阈值电压,减少能量损耗。构造有机发光二极管(OLED),以 CuI 掺杂的 NPB(烷类化合物)作空穴注入层,在外加偏压的作用下,提高了空穴的输运效率,增加了电子复合发光几率,使 OLED 的电流效率增加到 69cd/A。
2)CuI 作为空穴传输层用于染料敏化太阳能电池(SSDC)。常用的空穴层传输材料主要有三类:有机聚合物类电解质,液态电解液以及机 p 型半导体材料。无机 p 型半导体材料性能稳定,可以解决聚合物容易降解老化、液态物质容易挥发分解这两个问题,提高 SSDC 的稳定性和使用寿命。CuI以空穴传输层介于透明电极和染料之间,提高电子的势垒(阻挡电子向阳极输运),降低空穴的势垒。当太阳光辐射染料分子产生电子空穴对时,CuI 增加了空穴收集率,减少电子空穴的复合率,提高了内量子效率,从而达到提高光转换效率的目的。n-二氧化钛(TiO2)∣有机物∣p-CuI 固态染料敏化太阳能电池,首次利用 p-CuI 作空穴传输层,光电转换效率为 0.8%; n-ZnO∣D-358 染料∣p-CuI 固态染料敏化太阳能电池,光电转换效率高达 3.2%。聚合太阳能电池(PSCs),以 CuI 作为缓冲层,光电转换效率达到 3.84%。
【主要参考资料】
[1] 过静雯, 胡琦艳. CuI 制备方法的绿色研究[J]. 井冈山师范学院学报, 2005 (2005 年 03): 30-32.
[2] 碘化亚铜(CuI)材料的制备及光电性能的研究. 鲁东大学硕士学位论文
[3] 钟国清, 曾仁权. 饲料添加剂碘化亚铜的制备与测定[J]. 饲料工业, 1998, 19(11): 45-46.
