过氧化镍为黑色含水粉末,几乎不溶于任何溶剂。商品化试剂为水合过氧化镍 NiO2-xH2O,其中 Ni 含量高于 25 % , 活性氧含量高于30 %。也可以通过碱性硫酸镍与次氯酸钠反应来制备。
注意事项
镍试剂具有毒性和致癌性,使用时要小心谨慎。
过氧化镍可用于醇、酚和胺的氧化反应,并常用于杂环化合物的脱氢反应[1]。
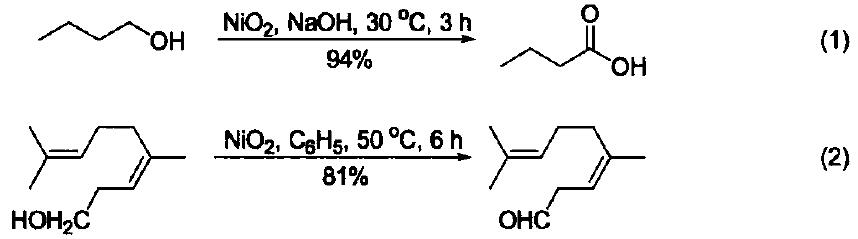
过氧化镍是一种温和的氧化剂。在碱性水溶液中可以选择性实现伯醇的氧化,得到相应的羧酸衍生物(式1)[2]。当反应在石油醚或苯等有机溶剂中进行时,可以将伯醇氧化为相应的羰基化合物(式2)。
在过氧化镍作用下,简单的苯酚会发生聚合反应。只有立体位阻较大的酚类化合物才能在过氧化镍氧化下实现二聚和低聚反应,或者得到醌类化合物。例如:2,6-二叔丁基苯酚被氧化为二聚4,4'-二苯醌的反应(式3)。使用对位有大位阻的苯酚底物时,则得到相应的 3,5- 二取代对苯亚甲基环戊二烯酮(式4)[3]。

在苯溶剂中,丙二烯伯醇在过氧化镍作用下能高产率地被氧化为相应的醛(式 5)[4]。当反应在氨介质中进行时 , 伯丙二烯醇则能被氧化为相应的酰胺(式6)。

在过氧化镍氧化下,脂肪族伯胺和苄胺能够被转变成为相应的腈化合物(式7)[5]。在同样条件下,芳香族伯胺生成对称的偶氮化合物,芳香族仲胺则生成对称联胺(式8)[6]。

过氧化镍还能实现脱氢反应。在过氧化镍作用下,邻氨基苯酚与苯甲醛生成的席夫碱化合物能发生分子内氧化脱氢成环反应(式9)。

参考文献
1. George, M.V.; Balachandran, K.S.Chem. Rev. 1975, 75,491.
2. Nakagawa, K.; Kotiaka, R.; Nakata, T.J. Org. Chem. 1962,27,1597.
3. Becher, H.D.J.Org. Chem. 1967,32,2943.
4. Bertrand, M.; Gil, G. ;Viala, J.Tetrahedron Lett. 1979,1595.
5. Nakagawa, K.; Tsuji, T.Chem. Pharm. Bull 1963,11,296.
6. Nakagawa, K.; Onoue, H.; Sugita, J.Chem. Pharm. Bull. 1964,12,1135.
