背景[1-3]
人巨细胞病毒抗体是一类可以特异性结合人巨细胞病毒的多克隆抗体,主要用于体外检测人巨细胞病毒的免疫学实验。
人巨细胞病毒(human cytomegalovirus,HCMV)是疱疹病毒家族中基因组的成员,可编码200多种蛋白质。HCMV感染宿主范围较窄,以人类为宿主,尚无感染动物模型。HCMV裂解复制增殖较缓慢,周期较长,除形成核内包涵体,HCMV具有能引发核周和细胞质包涵体产生和细胞肿胀(巨细胞)的特性,并因而得名。根据基因组和表型异质性的不同,HCMV可分为多种毒株,虽然病毒株之间存在一定的抗原变异,但并不具有临床重要意义。
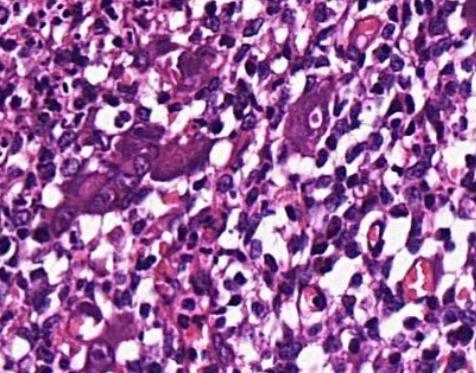
人巨细胞病毒抗体免疫组化
巨细胞病毒(cytomegalovirus,CMV)可以引起先天性感染。妊娠期有原发性感染或复发性感染,CMV可通过胎盘感染胎儿。临床表现为巨细胞包涵体病,病儿有肝脾肿大、黄疸、血小板减少性紫癜及溶血性贫血,少数呈先天性畸形,智力低下、神经肌肉运动障碍、耳聋、脉络视网膜炎等,重者流产或死胎。围生期感染症状较轻。儿童或成人感染是通过密切接触和性接触传播。输血感染可引起异嗜性和EB病毒抗体阴性的传染性单核细胞增多症及肝炎等。免疫力低下者,如肿瘤、器官移植、艾滋病等,可以引起潜伏的CMV激活,导致全身严重的CMV感染,表现为间质性肺炎、肝炎,并可导致死亡。此外,CMV还可能有致癌作用。其实验室检查有病毒分离、PCR和血清学试验。
应用[4][5]
用于人巨细胞病毒gH和PP65蛋白多肽疫苗的免疫原性研究
利用生物信息学技术对人巨细胞病毒(Human cytomegalovirus,HCMV)的包膜糖蛋白g H和磷酸化蛋白65(PP65)进行综合预测分析得到两个蛋白的线性B细胞优势抗原表位、CD8+T细胞优势抗原表位以及CD4+T细胞优势抗原表位。将抗原表位合成多肽分别在细胞和动物水平对合成的多肽进行免疫原性验证,从而为HCMV亚单位疫苗的研究提供有一定理论依据的抗原表位。
方法1、使用Prot Param、Prot Scale、SOPMA等共11个生物信息学软件,对HCMV g H和PP65蛋白的理化性质、结构功能、线性B细胞抗原表位、CD8+T细胞抗原表位和CD4+T细胞抗原表位进行预测,得到抗原表位后通过生物合成技术合成多肽共13条,根据生物学特性用合适的溶剂将其溶解。分别通过体外和体内实验检测合成多肽的免疫激活效果。
2、体外实验将人单核细胞系U937通过佛波酯(Phorbol myristate acetate,PMA)诱导为巨噬细胞,用于评价合成多肽对抗原提呈细胞的激活作用。用不同浓度的PMA及不同处理时间诱导U937细胞,通过镜下观察细胞形态变化以及利用流式细胞分析技术检测巨噬细胞表面激活标志物CD11b的表达情况,从而确定的诱导条件。通过细胞毒性(CCK-8)试验检测不同诱导条件对U937细胞的细胞毒性。在巨噬细胞中加入浓度为50μg/ml的多肽,无多肽组为阴性对照组,培养24h后,以流式细胞术检测M1型巨噬细胞表面激活标志物CD86的表达,探究每条多肽对巨噬细胞的免疫激活效果。
3、体内实验将鸡卵清白蛋白(ovalbumin,OVA)与弗氏佐剂混合制备的疫苗设为阳性组,g H蛋白多肽、PP65蛋白多肽、g H蛋白多肽+PP65蛋白多肽以及灭活的HCMV与弗氏佐剂混合制备的疫苗设为实验组,生理盐水组设为阴性组,生理盐水与佐剂混合组设为佐剂对照组,用肌肉注射的方式对小鼠进行三次免疫,次免疫所用佐剂为弗氏完全佐剂(Freund’s Adjuvant Complete,FCA),第二次和第三次免疫用弗氏不完全佐剂(Freund’s Adjuvant Incomplete,FICA),分别于第1、3、5周进行免疫。末次免疫1周后取小鼠脾脏,处理得到脾细胞悬液后,通过流式细胞分析技术对T细胞表达干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)和白细胞介素-4(IL-4)的情况进行检测。
结果通过生物信息学软件预测,g H蛋白和PP65蛋白优势抗原表位的氨基酸位点如下:g H蛋白线性B细胞优势抗原表位氨基酸位点179-194、383-398和526-541,PP65蛋白线性B细胞优势抗原表位氨基酸位点382-397和463-478;g H蛋白CD8+T细胞优势抗原表位氨基酸位点719-727,PP65蛋白CD8+T细胞优势抗原表位氨基酸位点495-503;g H蛋白CD4+T细胞优势抗原表位氨基酸位点236-250、340-354和707-721,PP65蛋白CD4+T细胞优势抗原表位氨基酸位点45-59、110-124和287-301。细胞诱导实验的结果表明,PMA在浓度为100ng/ml、处理48h时诱导U937细胞成为巨噬细胞的效果较好,CCK-8实验结果显示此诱导条件下没有细胞毒性。
参考文献
[1]Where do we Stand after Decades of Studying Human Cytomegalovirus?[J].Francesca Gugliesi,Alessandra Coscia,Gloria Griffante,Ganna Galitska,Selina Pasquero,Camilla Albano,Matteo Biolatti.Microorganisms.2020(5)
[2]HCMV glycoprotein B nucleoside-modified mRNA vaccine elicits antibody responses with greater durability and breadth than MF59-adjuvanted gB protein immunization[J].Cody S.Nelson,Jennifer A.Jenks,Norbert Pardi,Matthew Goodwin,Hunter Roark,Whitney Edwards,Jason S.McLellan,Justin Pollara,Drew Weissman,Sallie R.Permar.Journal of Virology.2020(prep)
[3]Congenital Cytomegalovirus—History,Current Practice,and Future Opportunities[J].Thigpen J..Neonatal Network.2020(5)
[4]Battle between Host Immune Cellular Responses and HCMV Immune Evasion[J].Trishna Manandhar,Gia-Gia T.Hò,Wiebke C.Pump,Rainer Blasczyk,Christina Bade-Doeding.International Journal of Molecular Sciences.2019(15)
[5]张倩文.人巨细胞病毒gH和PP65蛋白多肽疫苗的免疫原性研究[D].青岛大学,2021.
