简介
(2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐被用作靶向泛素化的调节剂,特别是多种多肽和其他蛋白质的抑制剂/或以其他方式被双功能化合物抑制。其一端包含一个von Hippel与泛素连接酶结合的Lindau(VHL)配体,另一端是与靶蛋白结合的部分,使得靶蛋白被放置在泛素连连酶附近以实现降解[1]。
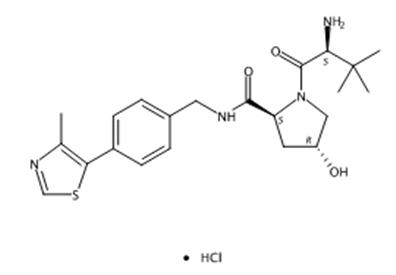
图1 (2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐的结构式。
合成
![图2 (2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐的合成路线[1]。 图2 (2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐的合成路线[1]。](/NewsImg/2022-12-24/6380750345236328703099075.jpg)
图2 (2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐的合成路线[1]。
步骤1:将4-溴苯甲腈(5.1克,28毫摩尔,1当量)、4-甲基噻唑(5.56克,56毫摩尔,2当量)乙酸钾(5.5克,56毫摩尔,2 eq)、乙酸钯(II)(63毫克,0.28毫摩尔,1%工具)溶解在二甲基乙酰胺中并在氩气下搅拌。(CITE JOC,2009,74,1179)将混合物加热至150°C并搅拌19小时,然后用500 mL EtOAc稀释,并用300 mL水洗涤4次。然后用300mL EtOAc反萃取次洗涤液,然后用100mL水洗涤4次。合并的有机层用硫酸钠干燥,过滤并在真空下浓缩,得到与报道的光谱数据相符的产物。然后将固体溶解在MeOH(280 mL)中并冷却至4℃。加入氯化钴(9.9克,41.6毫摩尔,1.5当量),然后缓慢分批加入硼氢化钠(5.2克,139毫摩尔,5当量),伴随剧烈起泡。90分钟后,加入水和氢氧化铵使反应停止。混合物用氯仿萃取4次,并通过柱色谱(10-30%0.5M NH3(MeOH)/DCM)纯化。较深的油,产率4.12克,20.2毫摩尔,73%。
步骤2:将(2S,4R)-1-(叔丁氧基羰基)-4-羟基吡咯烷-2-羧酸(366 mg,1.58 mmol,1当量)溶解在15 mL DMF中,并加入EDC(380 mg,2.0mmol,1.3当量),搅拌5分钟后加入HOBt(310 mg,2.0 mmol,1.5当量)(4-(4-甲基噻嗪-5-基)苯基)甲胺(325 mg,1.58mmol,1当量。搅拌15小时后,用25mL EtOAc稀释反应物,并用25mL盐水(2X)洗涤,然后用25mL饱和NaHCO3(2X)洗涤。将有机层浓缩,得到产物。黄色油,产率650 mg,98%。1H NMR(400 MHz,CDCl3)δ8.67(s,1H),7.43-7.29(m,4H),4.49(d,J=16.7 Hz,4H),3.51(dd,J=11.0,4.7 Hz,2H),2.61-2.45(m,4 H),2.03(d,J=7.4 Hz,2H),1.42(s,9H)。TLC:(9:1 DCM:MeOH(0.5 N NH3))Rf=0.20;毫秒(ESI)41715(M+H)+。
步骤3:将(2S,4R)-叔丁基4-羟基-2-((4-(4-甲基噻唑-5-基)苄基)氨基甲酰基)吡咯烷-1-甲酸酯(8g,19mmol)在甲醇(30mL)和二氯甲烷(20mL)的混合物中的溶液用4M盐酸在1,4-二恶烷(8mL,32mmol)中的溶液处理。将混合物在环境温度下搅拌2小时。将溶剂蒸发至干,残余物在二氯甲烷中研制,过滤并在真空下干燥,得到标题化合物。6.7克,99%。LCMS RT=0.51分钟,ES+ve m/z 318[m+H]+。
步骤4:将(2S,4R)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基苄基)吡咯烷-2-甲酰胺盐酸盐(70mg,0.20mmol)和(S)-2-((叔丁氧基羰基)氨基)-3,3-二甲基丁酸(可从例如Fluka购得)(50mg,0.22mmol)在DMF(1mL)的DMF(1 mL)中的搅拌混合物用DIPEA(0.14mL,0.79mmol)处理,然后用HATU(90mg,0.0.22mmol)处理,-并在环境温度下搅拌30分钟。通过质量导向自动制备HPLC(甲酸改性剂)纯化产物,得到中间体boc保护产物。然后将中间体溶解在二氯甲烷(0.5mL)和甲醇(0.1mL)的混合物中,并用4M盐酸在1,4-二恶烷(0.25mL,1.0mmol)中处理。在环境温度下搅拌1小时后,将反应混合物蒸发至干,残余物用二氯甲烷研成固体,并在真空下干燥,得到标题化合物(2S,4R)-1-((S)-2-氨基-3,3-二甲基丁酰基)-4-羟基-N-(4-(4-甲基噻唑-5-基)苄基)吡咯烷-2-甲酰胺盐酸盐。76 mg,82%。
参考文献
[1] C.M. Crews, D. Buckley, A. Ciulli, W. Jorgensen, P.C. Gareiss, I. Van Molle, J. Gustafson, H.-S. Tae, J. Michel, D.W. Hoyer, A.G. Roth, J.D. Harling, I.E.D. Smith, A.H. Miah, S.A. Campos, J. Le, Compounds and methods for the enhanced degradation of targeted proteins and other polypeptides by an E3 ubiquitin ligase, particularly targeting the von Hippel-Lindau E3 ubiquitin ligase using hydroxyproline analogs to disrupt the VHL/HIF-1α interaction, Yale University, USA; GlaxoSmithKline Intellectual Property Development Limited; Cambridge Enterprise Limited University of Cambridge . 2013, p. 509pp.
