人参皂苷 CK(20-O-B-D-glucopyranosyl-20-(S)-protopanaxadiol,C-K)属二醇型皂苷,它在自然界中是不存在的,是人参皂苷Rbl等人参二醇类皂苷口服后,被肠道菌所分解生成、吸收、进入血液的主要成分。在1972年,Yasioka等在用土壤细菌降解二醇型人参皂苷Rbl,Rb2和Rc的混合物来鉴定真性苷元结构时首次发现了人参皂苷 CK。人参皂苷 CK无论在体内,还是体外均具有良好的抑制癌细胞生长作用和抗癌细胞转移作用,因此,人参皂苷 CK是一种很好的潜在抗癌药物。近年来诸多研究表明,人参的许多生物学活性都是由该化合物引起的,特别是在抗肿瘤、抗衰老、改善记忆、抗炎及保肝等方面都体现了良好的药效。

结构
人参皂苷由疏水性糖苷配位基团与1~4个亲水性糖苷基团结合而成,人参皂苷 CK为四环达玛烷型三萜皂苷,在C-20上只有一个糖苷键,因此更利于被人体吸收利用。人参皂苷 CK的分子质量为622.88,分子式为C36H62O8。与其他皂苷相比,人参皂苷 CK分子质量较低,有较高的渗透性,在人体内的生物利用度更高。
制备方法[1]
一、化学法
化学法主要利用酸水解糖苷键、氧化加成和乙酰化等反应改变取代基,可能导致C-20位置的糖苷键发生非特异性裂解,引发一系列副反应,如差向异构、水合和羟基化等。许凌巧等利用醋酸水解人参茎叶总皂苷提取物制备人参皂苷CK,在底物加人量为0.5g、酸体积分数0.8%、温度110℃的条件下,人参皂苷 CK的含量从0.4%提高到6.09%,该方法简便且快速。但总的来说,化学水解会产生物质残留、环境污染、条件复杂、副反应产物多、对人身体健康产生威胁等问题,不适宜在食品行业的应用,因此用化学法大规模制备人参皂苷 CK较为困难。
二、生物转化法
1、肠道菌群转化
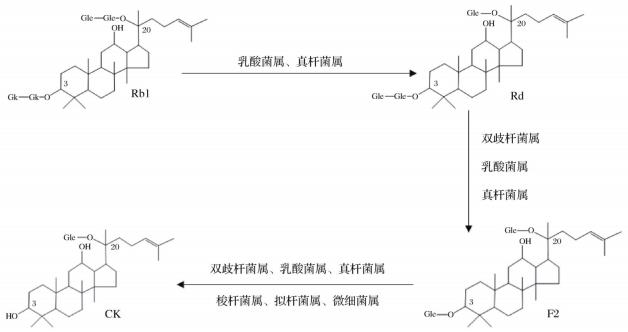
BAU等研究发现肠道内的乳酸菌可将人参皂苷转化为人参皂苷 CK,并成功分离该菌种。乳酸菌参与人参皂苷在肠道内的代谢途径如图所示,其中清酒乳杆菌、植物乳杆菌和长双歧杆菌参与Rb1-Rd代谢,短乳杆菌参与Rd-F2-CK代谢。因此可表明原人参皂苷能通过肠道内的菌群进行分解代谢,转化为生物活性更高的人参皂苷 CK。但由于个体不同,肠道内微生物具有明显的差异性,转化效率也各不相同,因此在体外对原人参皂苷脱糖基可实现其药理作用的高效发挥以及人参皂苷 CK的批量制备。
2、微生物发酵
微生物发酵是指用微生物产生的酶水解人参皂苷的糖苷键,进而转化为更易被人体吸收、生物活性更高的稀有人参皂苷 CK。周伟利用拟青霉(Paecilomyces Bainier sp.229)对人参皂苷进行转化,10L、50L的中试放大实验CK转化率最高达到75.47%和83.22%,经过纯化工艺后纯化度可达92%以上,因此拟青霉是具有大规模发酵制备CK潜质的菌种。
3、酶转化法
与微生物转化相比,酶转化法用特定的酶水解糖苷键,因此特异性更强,可以定向生成目标产物,且反应周期短、污染小、产物纯度高、可控性强。目前大多数研究都是以蜗牛酶和β-葡萄糖苷酶进行固定化,固定方式各有不同,研究一种成本更低、转化效率更高的重组酶作为底物进行固定并改善固定方式有利于人参皂苷 CK制备的进一步发展。除此之外,可以考虑和纳米技术结合,将纳米颗粒作为载体提高人参皂苷 CK的生物利用度和酶的活性,也是更高效规模化制备人参皂苷 CK的一个研究方向。通过特定且能循环利用的酶转化为特定的稀有人参皂苷则可以提高转化效率,减少分离混合产物过程中的损失,节约资源,并且循环使用酶可利于大规模生产特定人参皂苷 CK。
参考文献
[1]金香梅. 微生物转化人参主皂苷为稀有皂苷C-K的研究[D]. 吉林:延边大学,2010. DOI:10.7666/d.D01177858.
