3,5-二氯-4-羟基苯甲酸是一种苯甲酸衍生物,常温常压下为白色结晶固体,具有显著的酸性和优异的化学稳定性,它不溶于水但是在碱性水溶液中有一定的溶解性。3,5-二氯-4-羟基苯甲酸可由其苯甲酸酯的前体物质通过水解反应制备得到,也可通过对羟基苯甲酸的氯化反应制备得到,该物质主要用作有机合成中间体,有文献报道它可用于尿酸盐转运蛋白抑制剂的合成。
制备方法
方法一
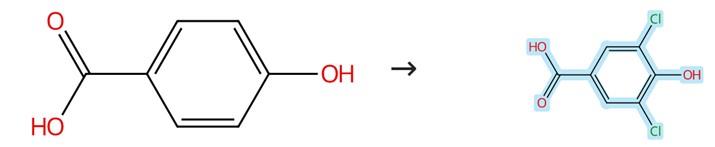
图1 3,5-二氯-4-羟基苯甲酸的制备方法
向3.5 g(0.025 mol)4-羟基苯甲酸溶于10 mL盐酸和20 mL水形成的悬浮液中加入10 mL 33%过氧化氢,反应后过滤生成的白色沉淀,用热水洗涤该沉淀,最后通过乙醇重结晶得到目标产物分子3,5-二氯-4-羟基苯甲酸。[1]
方法二
将3,5-二氯-4-羟基苯甲酸丁酯(200 mg, 0.76 mmol)和氢氧化钠(120 mg, 3.04 mmol, 4 eq)加入甲醇/水(2/8)混合溶剂中,室温搅拌反应18小时;随后加入乙酸乙酯(20 mL)和盐酸进行酸化,有机相经水(20 mL)洗涤、干燥并减压浓缩,最后通过硅胶柱色谱纯化,洗脱体系为二氯甲烷至二氯甲烷/甲醇即可得到目标产物3,5-二氯-4-羟基苯甲酸。[2]
苄基化反应
3,5-二氯-4-羟基苯甲酸结构中的羧基单元和酚羟基基团都具有显著的酸性,可在常见的碱性物质作用下发生去质子化反应得到相应的氧负离子,后者具有显著的亲核性可进行酯化和醚化反应。
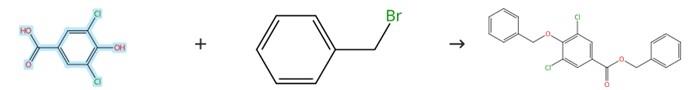
图2 3,5-二氯-4-羟基苯甲酸的苄基化反应
将3,5-二氯-4-羟基苯甲酸(5.00 g, 24.15 mmol)和碳酸钾(6.68 g, 48.3 mmol)加入200 mL烧瓶,注入DMF(30 mL)后于室温搅拌30分钟,再加入溴化苄(48.31 mmol)并于80°C下搅拌反应3小时;待原料完全消耗后加水(100 mL)淬灭,用乙酸乙酯(200 mL × 3)萃取合并有机相,经饱和食盐水洗涤后通过旋转蒸发仪在水浴中浓缩,最后经硅胶柱色谱纯化得到4-苄氧基-3,5-二氯苯甲酸苄酯。[3]
参考文献
[1] Derkach, L. G.; et al, Banana-shaped liquid crystals based on 2,7-dihydroxynaphthalene derivatives, Russian Journal of General Chemistry 2015, 85, 577-583.
[2] Albouy, Marion; et al, Characterization of pregnant women exposure to halogenated parabens and bisphenols through water consumption, Journal of Hazardous Materials 2023, 448, 130945.
[3] Zhao, Zean; et al, Discovery of novel benzbromarone analogs with improved pharmacokinetics and benign toxicity profiles as antihyperuricemic agents, European Journal of Medicinal Chemistry 2022, 242, 114682.
