背景及概述[1]
卡利拉嗪为非典型抗精神病药物,属于多巴胺D2、D3受体部分激动剂,主要用于治疗成人精神分裂症及双相躁狂症。目前已有森林实验室的盐酸卡利拉嗪胶囊上市。盐酸卡利拉嗪胶囊于2015年9月获FDA批准上市,原研药生产商为吉瑞大药厂,由森林实验室开发推广,用于治疗精神分裂和显性双相障碍的躁狂和混合症状。
卡利拉嗪 (cariprazine)是一种D3/D2受体部分激动剂,优先结合D3受体,与传统精神类药物(单纯作 用于D2)相比有优势(锥体外反应副作用发生率低、阴性症状的治疗)。在人体内被P450酶系代谢为活性代谢产物DCAR和DDCAR。稳定状态下70%为DDCAR,半衰期长达2-3周,也就是20 天左右。

制剂[1] [3-4]
一、盐酸卡利拉嗪冻干粉针剂
制备过程:
(1)称取处方量一水磷酸二氢钠、吐温80于约60%配制总量的注射用水中,搅拌溶解;
(2)加入处方量的羧甲基纤维素钠至上述溶液中,搅拌至完全溶解;
(3)加入盐酸卡利拉嗪,搅拌至完全分散,用氢氧化钠调节pH值为6.0至7.0,定容,得初始混悬液;
(4)将上述所得混悬水溶液,采用球磨机进行研磨分散。
(5)采用Malvern Mastersizer 2000粒度测定仪测定研磨后混悬水溶液粒度分 布,HPLC检测含量和有关物质,结果见表5-2,表5-3;
(6)将研磨后的混悬水溶液灌装于7mL西林瓶中,灌装量为2mL,进行冷冻干燥,测定冻干后粒径、含量、有关物质,放置加速条件,考察稳定性。
二、卡利拉嗪口腔崩解片的制备(规格1.5mg,以卡利拉嗪计)
卡利拉嗪口腔崩解片制备方法如下:
(1)按表1的配方,将盐酸卡利拉嗪、稀释剂、矫味剂、内加崩解剂(即内加部分的崩 解剂)混合均匀,然后用多功能流化床顶喷的方式进行一步制粒,在一步制粒过程中加入粘 合剂水溶液,制粒后得颗粒;其中,粘合剂在粘合剂溶液中的质量百分比为2.5%;
(2)对所得颗粒进行整粒,过80目筛后,加入外加崩解剂(即外加部分的崩解剂)和润滑剂,用三维混合机混合,然后用多功能旋转压片机进行压片,即得。
三、CN201510638151.4公开了一种盐酸卡利拉嗪药物组合物,由0.3wt%-10wt%的盐酸卡利拉嗪、82wt%-99.7wt%填充剂、0wt%-5wt%崩解剂和0wt%-3wt%润滑剂组成,其中,所述填充剂为乳糖或乳糖与其他填充剂的混合物,所述崩解剂选自低取代羟丙基纤维素或交联聚维酮中的一种或几种,所述润滑剂选自氢化蓖麻油、山嵛酸甘油酯、聚乙二醇或双硬脂酸甘油酯中的一种或几种。
本发明公开的盐酸卡利拉嗪药物组合物在水和酸性介质中均溶出完全,且稳定性良好,从而能保证用于人体时,在各种体内环境中均有一定的溶出或释放,即对于任何体质的患者均有一定的疗效。
晶型[2]
将卡利拉嗪盐酸盐样品5g加入冰醋酸10ml使之完全溶解;向上述溶液中迅速倾入 800ml四氢呋喃,白色固体析出形成悬浊液;静置悬浊液,减压抽滤,丙酮洗涤。 60℃烘干。得到产物4g。该产物经X-射线粉末衍射证明为卡利拉嗪盐酸盐的晶型 Ⅳ。
合成[5]
4-硝基环己基乙酸在水溶液中采用 10%Pd/C 催化氢化,室温反应 3 d 至原料反应完全,处理后得白色固体,然后将其加入 1 mol/L 盐酸乙醚溶液,浓缩析晶得到反式异构体的盐酸盐 2 的结晶,过滤干燥得白色固体,将化合物 2 用二氯甲烷溶解,加入三乙胺碱化,然后室温条件下与二碳酸二叔丁酯反应 24 h 得到化合物 3。
以甲苯为溶剂,氮气保护条件下,将二异丁基氢化铝慢慢滴加到用干冰冷却至−78℃的化合物 3 的溶液中,滴加完毕继续保温反应至不再冒泡,甲醇淬灭,后处理得到化合物 4。以 1,2-二氯乙烷为溶剂,将化合物 4 与 5 在三乙酰氧基硼烷存在下反应 24 h,制备得到化合物 6。以二氯甲烷为溶剂,室温条件下化合物 6 与三氟乙酸反应 16 h 后,再用羟基铵溶液调至 pH 10,然后以三乙胺为碱在氮气保护条件下与二甲基胺甲酰氯反应得到化合物 1(cariprazine),见图 2。
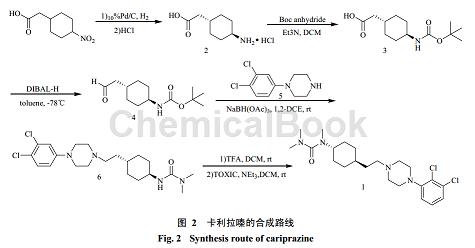
药代动力学[5]
卡利拉嗪具有较高的口服生物利用度,为脂溶性药物,因此在人体中较易穿过血脑屏障。其大鼠的口服生物利用度为 52%(剂量为 1 mg/kg)。卡利拉嗪的活性是其自身以及它的两个主要的活性代谢产物——去甲基卡利拉嗪(DCAR)和二去甲基卡利拉嗪(DDCAR)所产生,两种代谢产物与卡利拉嗪药理等效。
在一项为期 12 周的Vraylar 多剂量给药实验中,卡利拉嗪和 DCAR 的平均浓度在第 1 周到第 2 周达到平稳状态,DDCAR的平均浓度在第 4 周到第 8 周才接近稳定状态。若以达到稳定状态的时间为依据,根据平均浓度时间曲线估算半衰期,卡利拉嗪为 2~4 d, DDCAR 的为 1~3 周。主要活性代谢物 DDCAR 达到稳定状态的时间是根据患者的情况改变的,一些患者在 12周的治疗结束时仍不能达到稳定状态,在 12 周治疗结束时,DCAR 和 DDCAR 的平均浓度分别约为卡利拉嗪的 30%和 400%。
Vraylar 停药后,卡利拉嗪、 DCAR 和 DDCAR血浆浓度均已多指数的方式下降。从最后 1 个剂量开始, DDCAR 的平均血浆浓度在 1 周内下降到大约 50%, 卡利拉嗪和 DCAR 的平均浓度下降到该数值仅用了约 1 d 时间, 进而于 1 周后下降到约 10%;而 DDACR 的血浆浓度则用了约 4 周时间下降到10%。在卡利拉嗪 1 mg 单一剂量的实验中,停药 8周后仍可检测到微量的 DDCAR。多剂量给药 Vraylar 后,卡利拉嗪、 DCAR 和DDCAR 的血浆暴露按比例增加,这一数值超出了治疗剂量范围。
主要参考资料
[1] CN201711469664.2 一种盐酸卡利拉嗪注射制剂及其制备方法和用途
[2] CN201510609586.6 一种盐酸卡利拉嗪晶型Ⅳ及其制备方法
[3] CN201610936894.4 卡利拉嗪口腔崩解片及其制备方法
[4] CN201510638151.4盐酸卡利拉嗪药物组合物及其制备方法
[5]张海枝,陈会慧,刘长鹰,刘宁宁,张彦巧.卡利拉嗪:抗精神分裂症新药、多巴胺D3/D2受体部分激动剂[J].药物评价研究,2016,39(01):152-157.
