Anti-TGF-β/PD-L1 bispecific antibody promotes T cell infiltration and exhibits enhanced antitumor activity in triple-negative breast cancer
三阴性乳腺癌(TNBC)作为乳腺癌的一种亚型,以其侵袭性强、复发转移率高和预后差的特点,一直是乳腺癌治疗领域的难点。尽管近年来免疫治疗,特别是PD-1/PD-L1抑制剂的应用,为TNBC的治疗带来了新的希望,但临床响应率依然不高,且存在免疫抑制因素如TGF-β的干扰。为此,华中科技大学同济医学院附属同济医院肿瘤科吴孔明教授团队、浙江大学医学院附属第一医院乳腺外科代志军教授团队与武汉友芝友生物制药股份有限公司(以下简称友芝友生物)周鹏飞博士团队共同合作,研发出了一种靶向TGF-β和PD-L1的双特异性抗体(BiTP),并在《Journal for immunotherapy of cancer》期刊上发表了题为《Anti-TGF-β/PD-L1 bispecific antibody promotes T cell infiltration and exhibits enhanced antitumor activity in triple-negative breast cancer》的研究论文。该研究揭示了BiTP在TNBC治疗中的潜力,为TNBC的治疗提供了新的解决方案。

TNBC的治疗挑战与免疫治疗进展
TNBC约占所有乳腺癌病例的20%,其特点在于雌激素受体(ER)、孕激素受体(PR)和人类表皮生长因子受体2(HER2)均为阴性,这使得传统的内分泌治疗和抗HER2治疗对其无效。TNBC的预后极差,患者确诊后的生存期通常不超过20个月,5年生存率不足15%。因此,寻找新的治疗方法,特别是免疫治疗策略,对于TNBC患者来说至关重要。
从免疫学角度来看,乳腺癌被视为一种“冷”肿瘤,即肿瘤微环境中免疫细胞浸润较少,免疫反应较弱。然而,TNBC由于其肿瘤浸润淋巴细胞数量较多、PD-L1表达较高和肿瘤突变负荷较高,已成为免疫治疗策略的首选亚型。目前,已有多个PD-1/PD-L1抑制剂获批用于治疗TNBC,但这些治疗的临床响应率依然不高,不超过20%。此外,PD-L1单抗联合化疗也未能改善TNBC患者的总生存期(OS),这主要归因于肿瘤中存在的免疫抑制因素,如TGF-β等。

TGF-β/PD-L1双特异性抗体的研发背景与机制
鉴于PD-1/PD-L1抑制剂在TNBC治疗中面临的挑战,研究人员开始探索其他免疫调节靶点,以寻找新的治疗策略。其中,TGF-β作为一种重要的免疫抑制因子,在TNBC中发挥着关键作用。TGF-β能够抑制T细胞的增殖和分化,降低其抗肿瘤活性,从而促进肿瘤的生长和转移。因此,靶向TGF-β的免疫治疗策略成为研究热点。
友芝友生物基于其Check-BODY平台,成功开发出了一种四价对称的靶向TGF-β和人PD-L1的双特异性抗体(BiTP)。该抗体对两个靶点均表现出高结合亲和力,能够同时阻断TGF-β-Smad和PD-L1-PD-1-NFAT信号传导。这一特性使得BiTP具有双重免疫调节作用,既能抑制TGF-β的免疫抑制作用,又能增强PD-1/PD-L1通路介导的抗肿瘤免疫反应。

实验设计与结果解析
为了验证BiTP在TNBC治疗中的疗效和机制,研究人员构建了两种将鼠PD-L1替换为人PD-L1的小鼠TNBC肿瘤细胞株(EMT-6-hPDL1和4T1-hPDL1),并建立了乳腺原位荷瘤小鼠模型。通过这两种动物模型的药效实验,研究人员发现BiTP相对于抗PD-L1和抗TGF-β单药治疗具有优越的抗肿瘤活性。
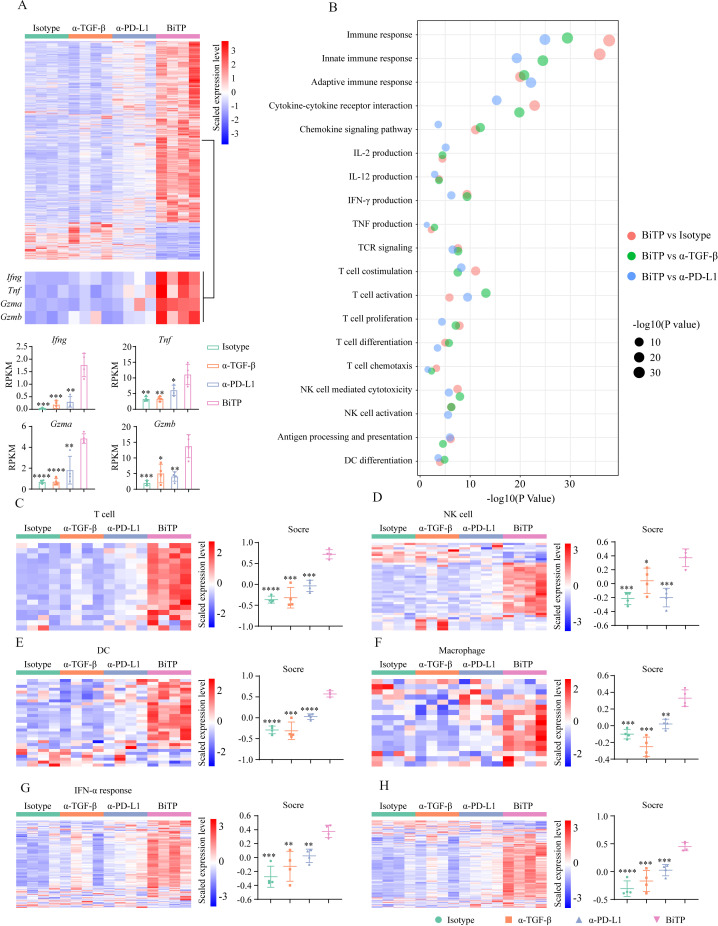
在机制上,BiTP减少了肿瘤微环境中的胶原蛋白沉积,改善了肿瘤微环境,从而增强了CD8+ T细胞的穿透力和肿瘤浸润淋巴细胞的数量。这一发现揭示了BiTP改善肿瘤微环境、提升抗肿瘤活性的重要作用机制。此外,BiTP还表现出优于单抗的抗肿瘤活性,表明其对于TNBC治疗具有潜在的临床价值。
药效与安全性评估
在研究过程中,研究人员对BiTP的药效和安全性进行了全面评估。药效实验结果显示,BiTP在EMT-6-hPDL1和4T1-hPDL1肿瘤模型中均表现出显著的抑瘤效果,且显著延长了小鼠的存活时间。同时,BiTP并未增加毒性反应,表现出良好的安全性。这一结果进一步支持了BiTP在TNBC治疗中的潜在应用前景。
研究的临床意义与转化价值
此项研究不仅证实了TGF-β/PD-L1双特异性抗体对TNBC的抑制效果,还拓宽了其抗肿瘤谱。基于该双特异性抗体的免疫疗法有望成为治疗TNBC的全新解决方案,具有很大的临床意义和转化价值。
首先,BiTP的研发为TNBC患者提供了新的治疗选择。由于TNBC对传统治疗方法的响应率较低,且预后较差,因此寻找新的有效治疗方法对于提高患者生存率具有重要意义。BiTP作为一种新型的双特异性抗体,能够同时靶向TGF-β和PD-L1两个免疫调节靶点,具有显著的抗肿瘤活性,有望为TNBC患者带来新的治疗希望。
其次,BiTP的研发也推动了免疫治疗策略的发展。传统的免疫治疗策略主要依赖于单一的免疫调节靶点,如PD-1/PD-L1等。然而,由于肿瘤微环境的复杂性和多样性,单一靶点的免疫治疗往往难以取得理想的疗效。BiTP的研发为免疫治疗策略提供了新的思路,即通过同时靶向多个免疫调节靶点来增强抗肿瘤免疫反应,从而提高疗效。
最后,BiTP的研发还促进了双特异性抗体技术的发展。双特异性抗体作为一种新型的药物形式,具有同时靶向多个靶点的优势。然而,双特异性抗体的研发也面临着技术挑战和专利壁垒。友芝友生物通过其Check-BODY平台成功开发出BiTP,不仅验证了双特异性抗体在TNBC治疗中的潜力,还为其他双特异性抗体的研发提供了有益的借鉴和参考。
友芝友生物在双特异性抗体领域的贡献与未来展望
迄今为止,友芝友生物已发表多篇关于TGF-β/PD-L1双特异性抗体的文章,从多个角度深入研究了其作用机制和联合治疗策略。这些研究不仅揭示了BiTP抑制TGF-β和PD-L1的双通路协同机制,还展示了其联合治疗对抑瘤效果的显著增强作用。此外,友芝友生物还从针对人的双特异性抗体BiTP角度研究了治疗TNBC的可能性,为TGF-β/PD-L1双特异性抗体临床方案的设计提供了坚实的理论基础。
未来,友芝友生物将继续致力于双特异性抗体技术的研发和创新,推动其在肿瘤免疫治疗领域的应用和发展。一方面,友芝友生物将继续优化和完善其Check-BODY平台,提高双特异性抗体的研发效率和成功率;另一方面,友芝友生物将加强与国内外科研机构和制药企业的合作与交流,共同推动双特异性抗体技术的创新和发展。此外,友芝友生物还将积极探索BiTP在其他肿瘤类型中的应用前景,为更多患者提供有效的治疗选择。
综上所述,TGF-β/PD-L1双特异性抗体BiTP在TNBC治疗中展现出了显著的疗效和潜力。该研究的发表不仅为TNBC患者提供了新的治疗希望,还推动了免疫治疗策略和双特异性抗体技术的发展。未来,随着研究的深入和技术的创新,BiTP有望成为治疗TNBC的重要药物之一,为更多患者带来福音。
PCNA (D3H8P) XP ® Rabbit mAb
100ul
PCNA (D3H8P) XP ® Rabbit mAb
20ul
N-Cadherin (D4R1H) XP ® Rabbit mAb
20ul
beta-Actin (D6A8) Rabbit mAb
100ul