抗体偶联物纯化:非亲和层析技术全攻略
发布日期:2026/2/25 17:21:34发布人:上海优宁维生物科技股份有限公司阅读量:39
抗体偶联物是免疫检测、诊断试剂与蛋白研究的核心试剂,常见类型包括酶标抗体、荧光标记抗体、生物素 / 亲和素标记抗体。抗体与小分子偶联后,会出现电荷、疏水性、分子量不均一的问题,单纯依靠亲和层析难以实现高质量分离。
本文围绕离子交换层析、疏水层析、凝胶过滤层析三类非亲和纯化方式,结合实际图谱案例,讲解不同抗体偶联物的纯化思路,在去除未反应原料的同时,最大程度保护复合物活性与稳定性。
一、抗体偶联物纯化要点
不同偶联目标对标记比例要求不同:
酶标抗体:低偶联比例更利于保留抗体结合力与酶活性
荧光抗体:适当提高偶联比例可增强信号,但过度修饰易导致聚集、荧光淬灭
生物素 / 毒素类偶联物:高比例可提升结合能力,但需避免改变蛋白特性
因此,根据分子量、电荷、疏水性差异选择层析策略,是纯化成功的关键。
二、酶标抗体的纯化方案
1. HRP 标记抗体纯化
HRP(辣根过氧化物酶)分子量约 44 kDa,游离酶易去除,但 1:1 偶联物与游离抗体较难分离,通常采用足量酶进行反应。
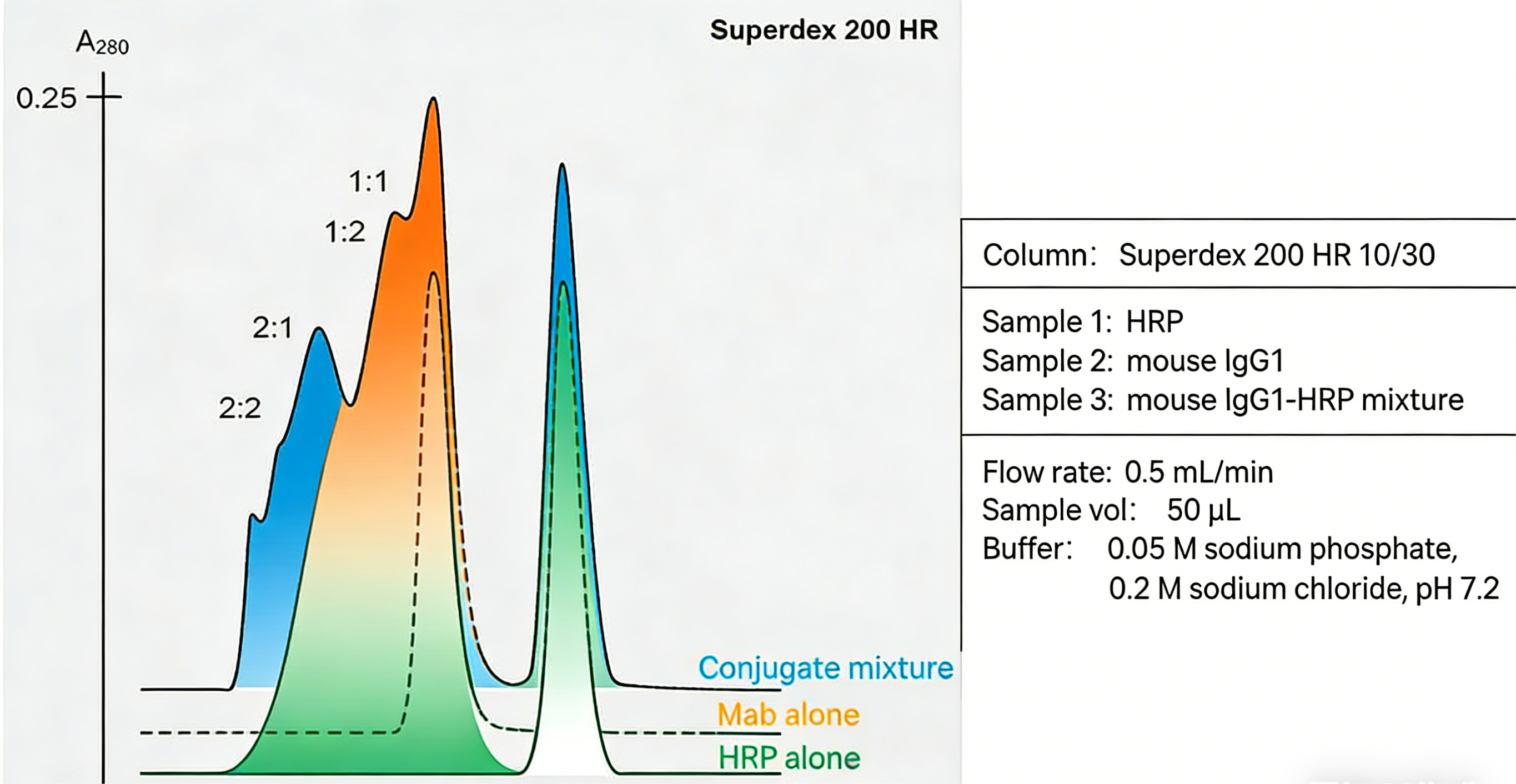
图 1 凝胶过滤层析分离 HRP - 抗体偶联物
(采用 Superdex 200 填料,依据分子量差异分离游离抗体、HRP - 抗体复合物及游离酶)
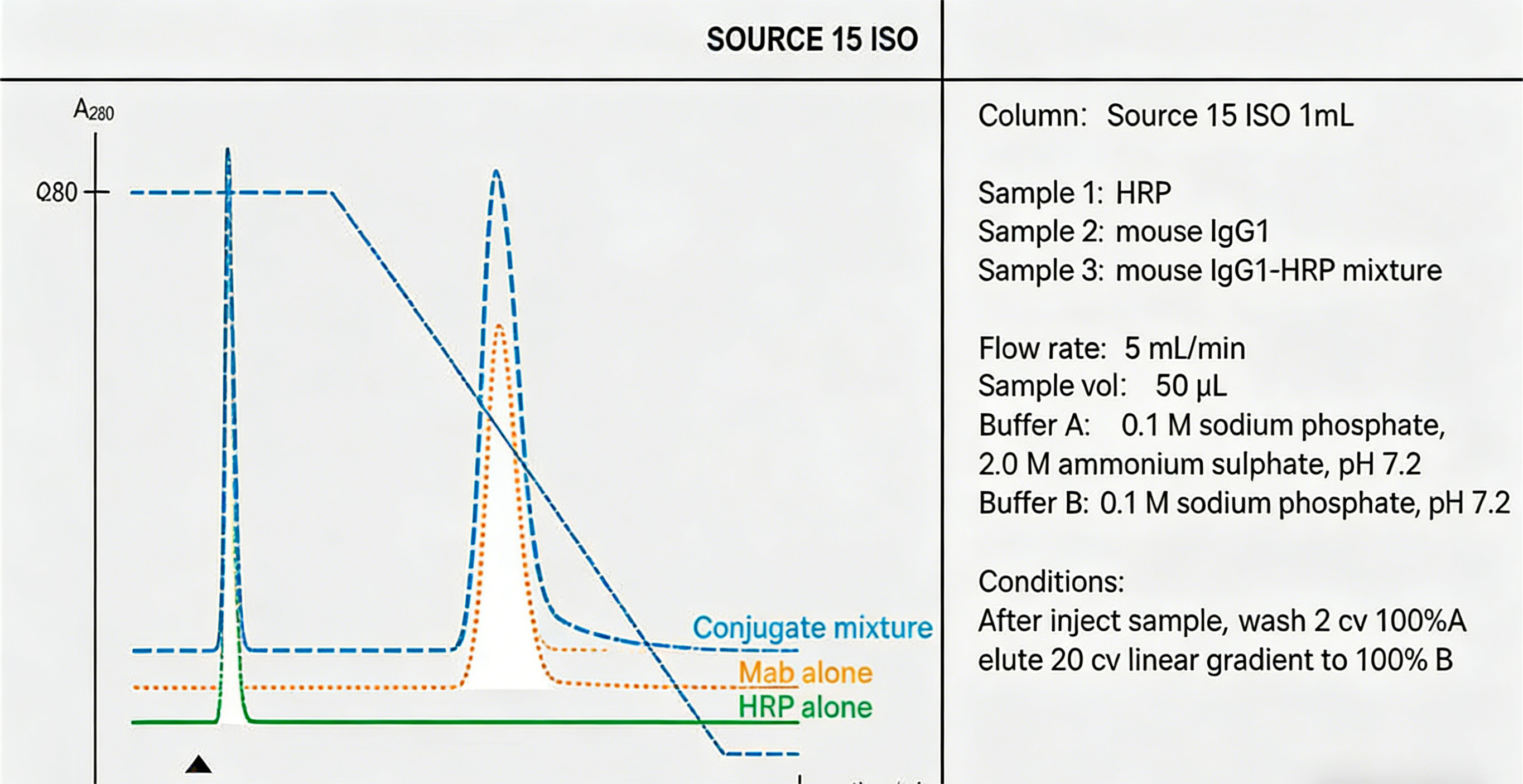
图 2 疏水层析分离 HRP - 抗体偶联物
(利用偶联后疏水性差异,实现复合物与未偶联抗体的高效分离)
2. AP 标记抗体纯化
AP(碱性磷酸酶)分子量约 140 kDa,与抗体偶联后分子量差距明显,纯化难度更低。
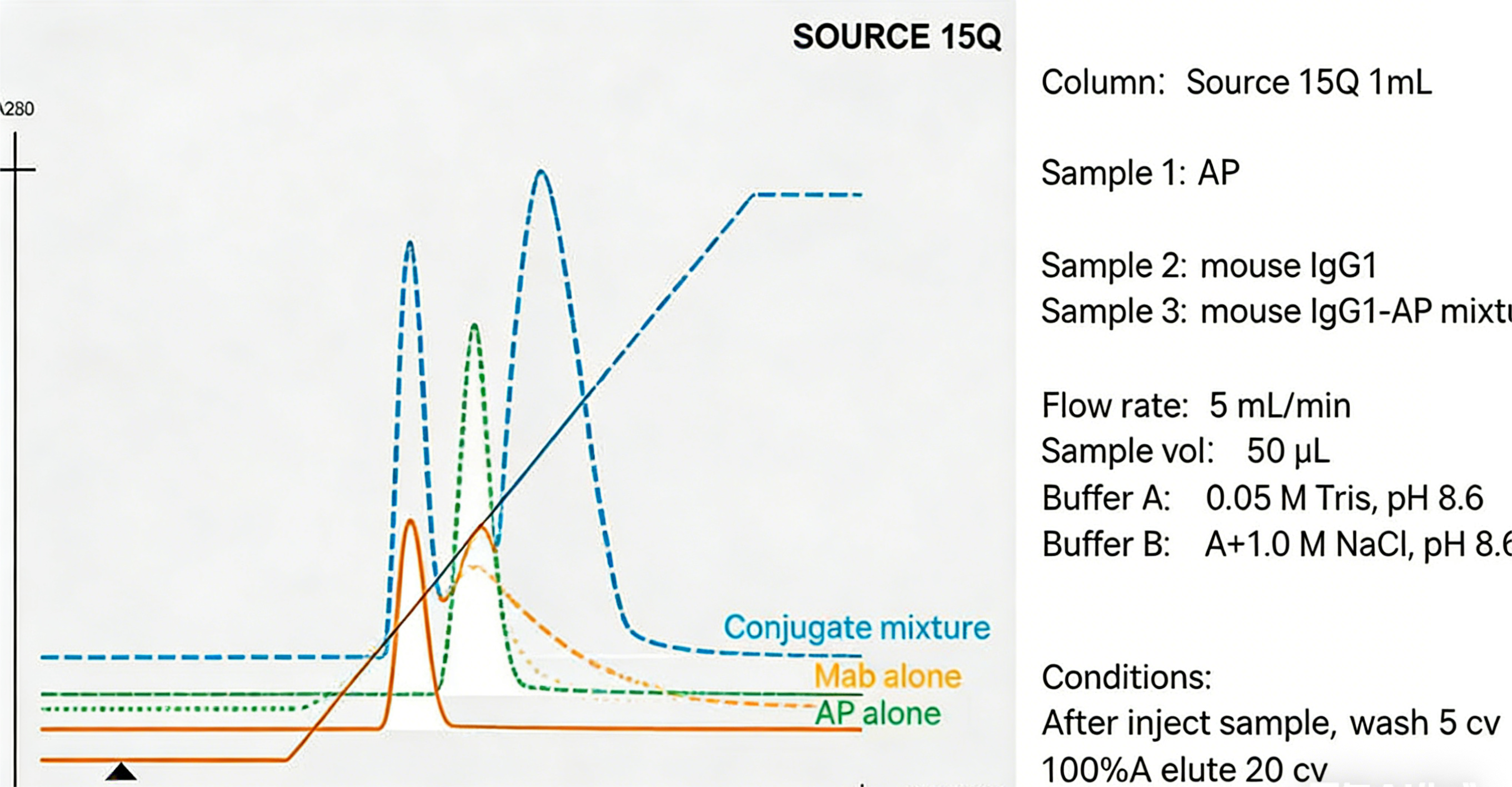
图 3 阴离子交换层析分离 AP - 抗体偶联物
(AP 标记抗体在阴离子交换柱上保留更强,可清晰分离游离抗体与偶联产物)
三、荧光标记抗体的纯化方案
荧光素多为疏水性小分子,偶联后会显著改变抗体电荷与疏水性,凝胶过滤效果差,优先使用离子交换与疏水层析。
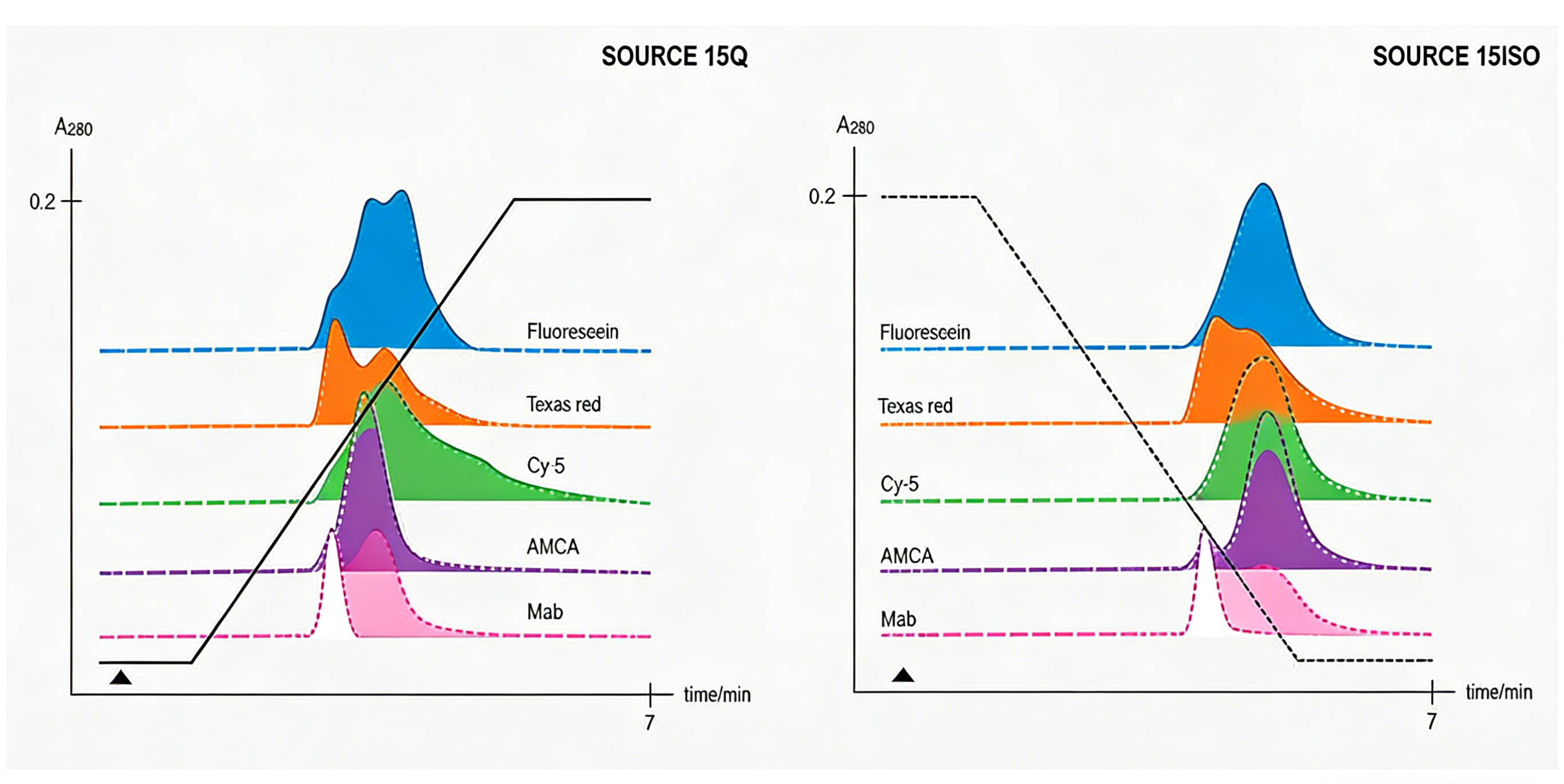
图 4 离子交换 & 疏水层析分离荧光素标记抗体
(两类方法均可高效区分不同标记程度的抗体偶联物)
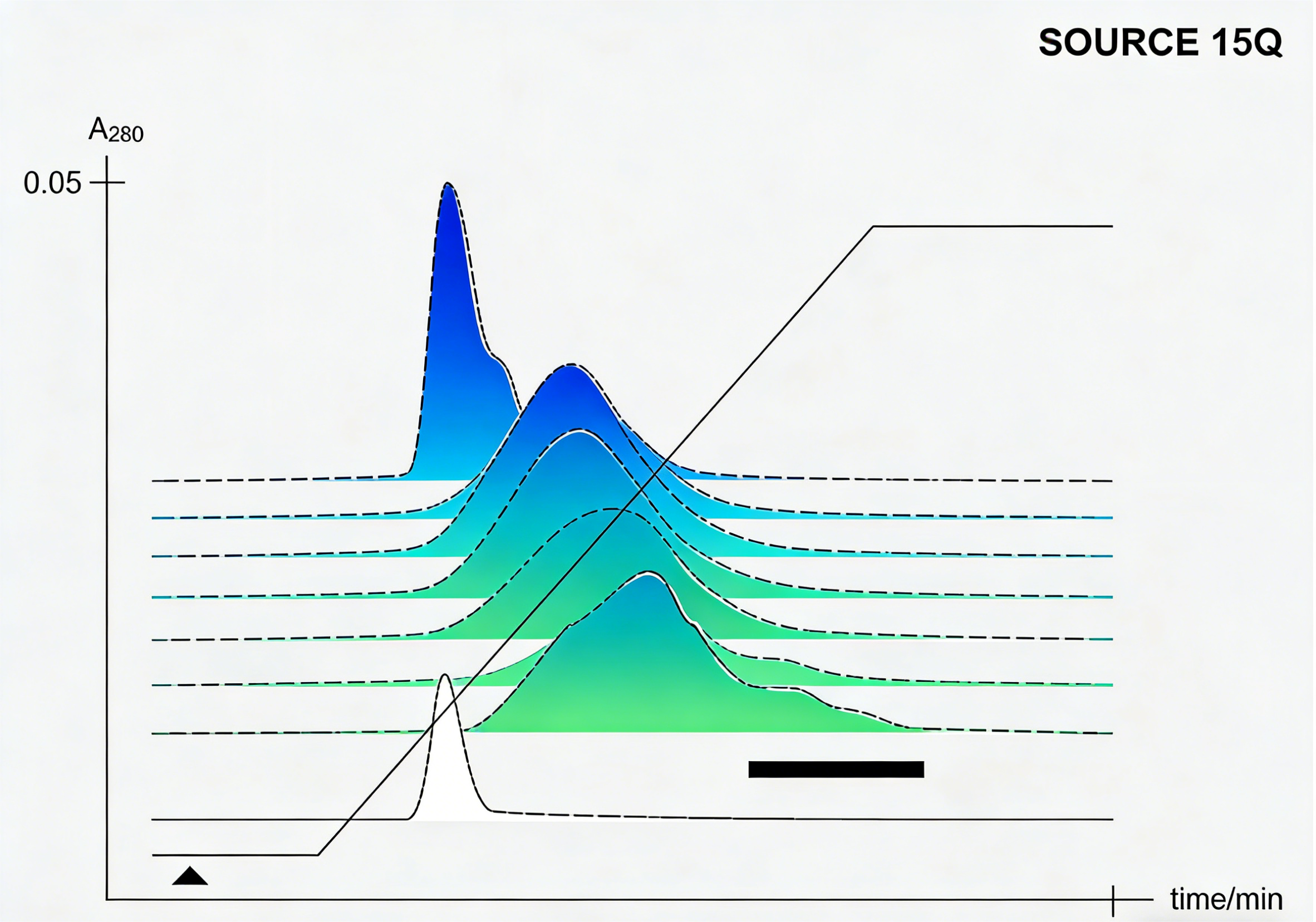
图 5 阴离子交换层析分离不同偶联比例 FITC 标记抗体
(上图依次为:低偶联比例、适宜偶联比例、过度偶联比例;黑色框为过度修饰导致的聚集沉淀峰)
四、生物素 / 亲和素标记抗体纯化
生物素标记比例通常较高(>5),对偶联物电荷与疏水性影响显著。
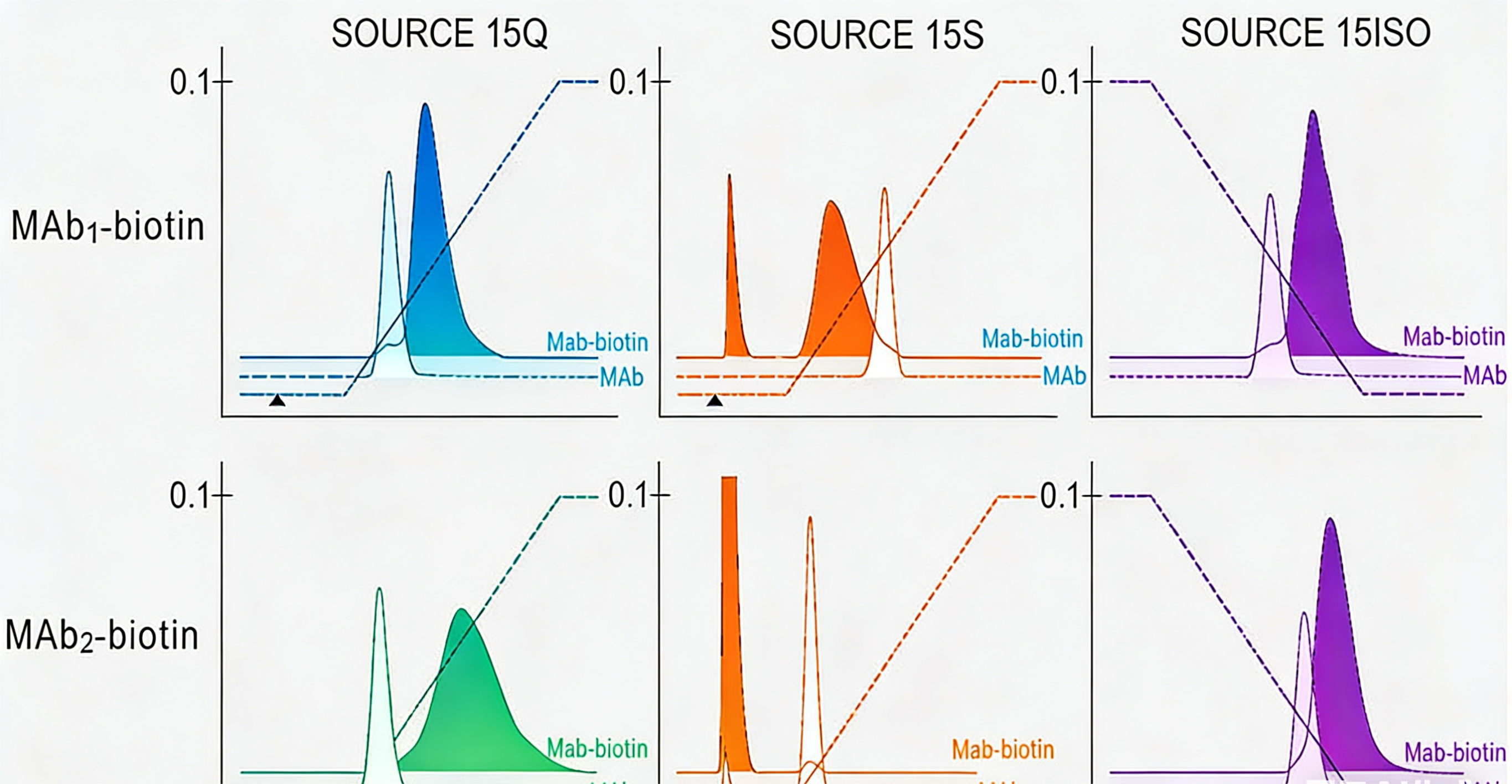
图 6 离子交换 & 疏水层析分离生物素标记抗体
(阴离子交换、阳离子交换、疏水层析均可用于不同抗体的生物素偶联物分离)
亲和素与链霉亲和素标记抗体特点:
亲和素:等电点高、带正电多、非特异结合强,在阳离子交换柱上保留更强
链霉亲和素:无糖基、无二硫键,疏水性更强,更适合疏水层析分离
小结
抗体偶联物无需依赖单一纯化方式,可根据实际情况组合使用:
分子量差异大 → 凝胶过滤层析
电荷差异明显 → 离子交换层析
疏水性差异大 → 疏水层析
优宁维提供全系列层析填料、预装柱及纯化方案支持,助力您获得高均一性、高活性的抗体偶联物。
常见问题 FAQ
1,抗体偶联物纯化,优先选哪种层析方法?
优先看差异:分子量差大选凝胶过滤,电荷差大选离子交换,疏水性差大选疏水层析。
2,怎么判断偶联比例是否合适?
酶标抗体建议低比例;荧光 / 生物素抗体看峰形,无聚集、无拖尾为适宜比例。
3,过度偶联会有什么后果?
会出现蛋白聚集、活性下降、荧光淬灭、非特异性结合升高等问题。
4,优宁维可以提供哪些相关产品?
凝胶过滤、离子交换、疏水层析填料 / 预装柱、层析系统、缓冲液及整体实验方案。
BLUE SEPHAROSE 6 FAST FLOW, 50ML
EA
Series S Sensor Chip SA
EA
相关新闻资讯
查看更多