107869-45-4
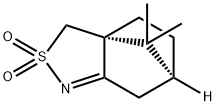 107869-45-4 结构式
107869-45-4 结构式
基本信息
(+)-10-樟脑内磺酰亚胺
(+)-10-樟脑磺内酰亚胺
(1R)-(+)-樟脑内磺酰亚胺
(7R)-(+)-10,10-二甲基-3-噻吩-4-氮三环[5.2.1.01,5]十二-4-烯-3,3-二氧化物
(1R)-(+)-10,10-二甲基-3-硫杂-4-氮杂三环[5.2.1.01,5]癸-4-烯-3,3-二氧化物
(7R)-(+)-10,10-二甲基-3-硫杂-4-氮杂三环[5.2.1.01,5]癸-4-烯-3,3-二氧化物
(3AR)-(+)-4,5,6,7-四氢-8,8-二甲基-3H-3A,6-亚甲基-2,1-苯并异噻唑基-2,2-二氧化物
(1R)-(+)-CAMPHORSULFONYLIMINE
(+)-10-CAMPHORSULFONIMINE 97+%
(1R)-(+)-(10-CAMPHORSULFONYL)IMINE
(7R)-10,10-DIMETHYL-3-THIA-4-AZATRICYCLO[5.2.1.01,5]DEC-4-ENE-3,3-DIOXIDE
(7R)-(+)-10,10-DIMETHYL-3-THIA-4-AZATRICYCLO[5.2.1.01,5]DEC-4-ENE 3,3-DIOXIDE
(1R)-(+)-10,10-Dimethyl-3-thia-4-azatricyclo[5.2.1.01,5]dec-4-ene 3,3-dioxide
(7R)-(+)-10,10-DIMETHYL-5-THIA-4-AZATRICYCLO[5.2.1.0(3,7)]DEC-3-ENE-5,5-DIOXIDE
(3AR)-4,5,6,7-TETRAHYDRO-8,8-DIMETHYL-3H-3A,6-METHANO-2,1-BENZISOTHIAZOLE-2,2-DIOXIDE
(3aR,6S)-8,8-Dimethyl-4,5,6,7-tetrahydro-3H-3a,6-methanobenzo[c]isothiazole 2,2-dioxide
物理化学性质
安全数据
制备方法
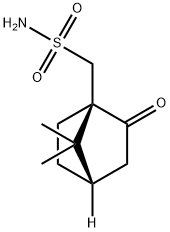
72597-34-3

107869-45-4
例1; (1R)-(+)-2,10-樟脑磺酰胺(方案3,3-1)的合成:在回流条件下,向(-)-樟脑磺酸(1.45 kg,6.25 mol)的氯仿(7 L)溶液中缓慢加入亚硫酰氯(0.896 kg,7.5 mol),历时1小时。反应混合物回流16小时后,使用冰浴冷却至4℃。将冷却的反应混合物缓慢加入浓缩的NH4OH(15 L)中,同时控制加入速度以保持温度低于15℃。添加完毕后,混合物在室温下搅拌4小时。分离有机层,水层用氯仿(2×2 L)萃取。合并的有机萃取液用盐水(4 L)洗涤,并经MgSO4干燥。过滤后,滤液真空浓缩并干燥,得到1.2 kg(83%收率)的樟脑磺酰胺。在另一实验中,使用145 g规模的樟脑磺酸,以二氯甲烷替代氯仿进行反应和萃取,得到相当的产率。向樟脑磺酰胺(1.2 kg,5.2 mol)的甲苯(15 L)悬浮液中加入Amberlyst H+树脂(150 g),混合物加热回流4小时,同时使用Dean-Stark分水器共沸除去生成的水。反应混合物热过滤以除去树脂。冷却滤液得到白色固体,过滤收集,得到1.02 kg(92%收率)的目标亚胺。向上述亚胺(100 g,0.47 mol)的乙醇(0.75 L)溶液中加入Raney镍(100 g),混合物在40 psi下氢化2小时。过滤除去催化剂,滤液真空浓缩,得到产物3-1,为白色固体。
参考文献:
[1] Tetrahedron, 1986, vol. 42, # 14, p. 4035 - 4044
[2] Chemical Communications, 1998, # 15, p. 1549 - 1550
[3] Journal of the American Chemical Society, 1988, vol. 110, p. 8477
[4] Patent: US2006/128789, 2006, A1. Location in patent: Page/Page column 7
[5] Organic Process Research and Development, 2005, vol. 9, # 2, p. 193 - 197
