95635-55-5
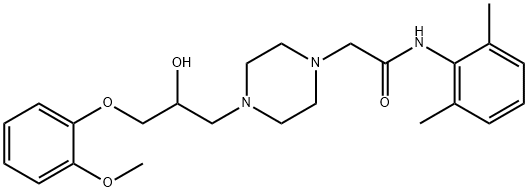 95635-55-5 结构式
95635-55-5 结构式
基本信息
雷诺嗪
1-[3-(2-甲氧苯氧基)-2-羟丙基]-4-[(2,6-二甲基乙酰)苯胺]哌嗪(雷诺嗪游离碱)
RANOLAZINE
1-[3-(2-methoxyphenoxy)-2-hydroxypropyl]-4-[(2,6-dimethylphenyl)aminocarbonylmethy]piperazine
CVT 303
Ranexa
Renexa
RS 43285-003
1-Piperazineacetamide,N-(2,6-dimethylphenyl)-4-[2-hydroxy-3-(2-methoxyphenoxy)propyl]-
物理化学性质
制备方法
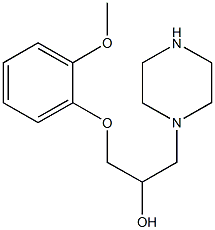
162712-35-8
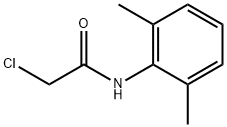
1131-01-7

95635-55-5
以雷诺嗪杂质B和2,6-二甲基氯代乙酰苯胺为原料合成N-(2,6-二甲基苯基)-2-(4-(2-羟基-3-(2-甲氧基苯氧基)丙基)哌嗪-1-基)乙酰胺的一般步骤:将1-(2-甲氧基苯氧基)-3-哌嗪-1-基-丙-2-醇(2g,7.52mmol)、2-氯-N-(2,6-二甲基苯基)乙酰胺(1.84g,9.34mmol)、无水碳酸钾(2g,14.5mmol)和碘化钠(74mg,0.5mmol)溶于二甲基甲酰胺(5mL)中,于30-35℃反应约18小时。反应完成后,用水淬灭反应混合物,并进行标准萃取后处理,得到粗产物。粗产物通过硅胶快速柱色谱法纯化(色谱柱尺寸:2×16cm,洗脱剂:二氯甲烷/甲醇/三乙胺=100/2/1),最终得到N-(2,6-二甲基苯基)-2-(4-(2-羟基-3-(2-甲氧基苯氧基)丙基)哌嗪-1-基)乙酰胺(1.1g,收率34%)。产物经1H NMR(300MHz,CDCl3)确认:δ7.11(s,3H),6.98-6.90(m,4H),4.19(br.s,1H),4.05(d,2H,J=5.4Hz),3.87(s,3H),3.30-3.24(m,2H),2.76-2.63(m,10H),2.25(s,6H)。LC-MS显示m/z=428(MH+),HPLC纯度为99%。
参考文献:
[1] Patent: US2008/312247, 2008, A1. Location in patent: Page/Page column 31-32
[2] Patent: WO2006/8753, 2006, A1. Location in patent: Page/Page column 7; 8
[3] Organic Process Research and Development, 2012, vol. 16, # 10, p. 1660 - 1664
常见问题列表
| Target | Value |
| Calcium channel |
Ranolazine被发现更紧密地结合到失活状态而不是静息状态的钠通道,表观解离常数分别为K(DR)=7.47 mM和K(DI)=1.71 mM。Ranolazine在5 mM和10 mM可逆缩短TC的持续时间和废除收缩。 在晚期钠增加时,Ranolazine抑制钠电流后期分量,并衰减的动作电位时程延长,无论是在IK-阻断药物的缺乏和存在。Ranolazine(10 mM)减少了89% 10 nM的ATX-Ⅱ诱导的增加的APD的变异性引起的13.6倍。
在狗左心室肌细胞中,Ranolazine以浓度依赖性的方式显著和可逆地在0.5或0.25赫兹刺激的缩短肌细胞的动作电位持续时间(APD)。 在工作的大鼠心脏中,Ranolazine(10 mM)显著增加葡萄糖氧化条件下的1.5倍至3倍,其中葡萄糖的总体ATP产生的贡献低(低钙,高FA,胰岛素),贡献高(高钙,低FA,同起搏),或者中间体。在含氧量正常的大鼠的Langendorff心脏中,Ranolazine(10 mM)同样增加葡萄糖氧化(高钙,低FA;15 毫升/分钟)。Ranolazine显著改善再灌注局部缺血的工作心脏的功能,这是与显著增加葡萄糖氧化功能相关的。
