千呼万唤,心衰治疗的突破
心力衰竭(简称心衰)是由于任何心脏结构或功能异常导致心室充盈或射血能力受损的一组复杂临床综合征,主要临床表现为呼吸困难和液体潴留。全球患病人数估计有2600万人,中国心衰患病人数预计在400万人左右,心衰是65岁以上人群住院治疗的主要原因,诊断后的一年和五年死亡率分别是28%和59%,目前每年全球心衰治疗费用约1080亿美元。是当今最重要的心血管病之一。
尽管心衰治疗药物较多,但患者仍面临着死亡高风险且生活质量差。1970-2000年,心衰治疗新药上市较多,最近十多年来,因为心血管药物开发的成功率较低,且药物安全要求较高,心衰治疗方面几无进展,此前诺华开发的心血管药物serelaxin就因为安全性问题,被FDA和欧盟拒之门外。
图1 心衰在研药物开发靶点
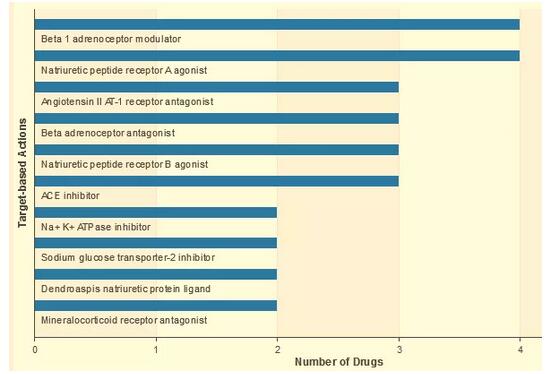
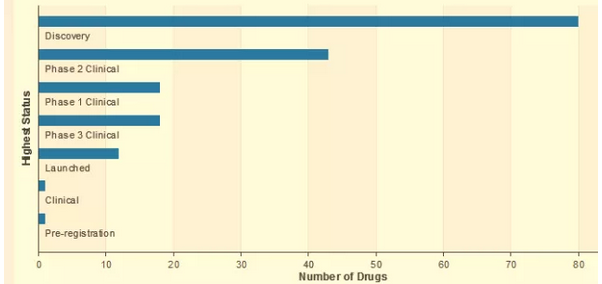
图2 心衰药物在研情况
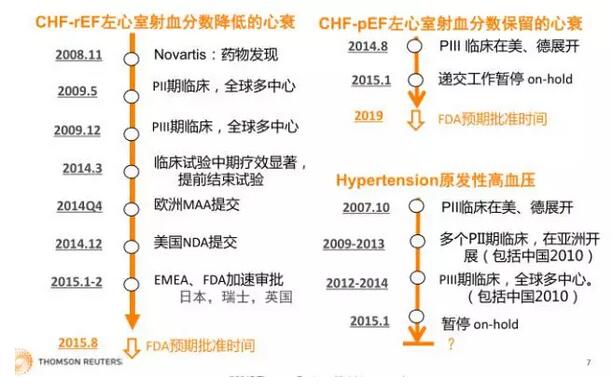
诺华在2008年11月发现LCZ696,随后开展了一系列临床试验,由于显著性的有效性和安全性数据,LCZ696在2015分别获得EMA和FDA的加速审评和快车道资格,是首个获得EMA加速审评资格的心血管药物,并分别于2015.7.17、2015.11.19获得FDA和EMA批准上市。
图3 LCZ696药物开发历程
寄予厚望的全新机制
LCZ696是由缬沙坦和sacubitril(分子量为1:1)组成的复合物,是一种双效血管紧张素受体脑啡肽酶抑制剂。与其他心衰药物只抑制肾素-血管紧张素-醛固酮系统(RAAS)相比,LCZ696通过加强对神经内分泌系统(NP系统)保护,同时抑制RAAS的过度活跃的有害影响。
表2 LCZ696的药物信息
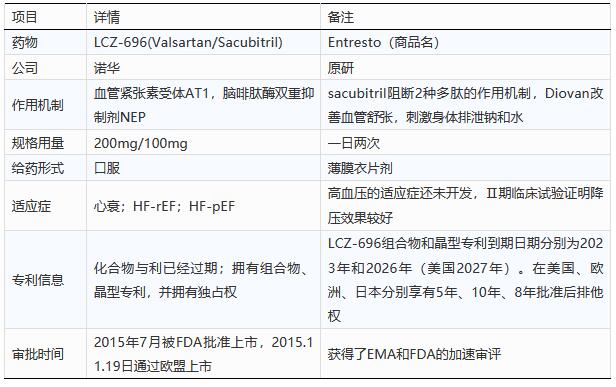
药物的有效性
诺华开展了多项临床试验,其中Ⅲ期的PARADIGM-HF试验是在心衰患者群体中开展的有史以来规模的研究,为LCZ696提供了非常具有说服力的临床数据。
表3 LCZ696 Ⅲ期PARADIGM-HF临床试验方案的设计
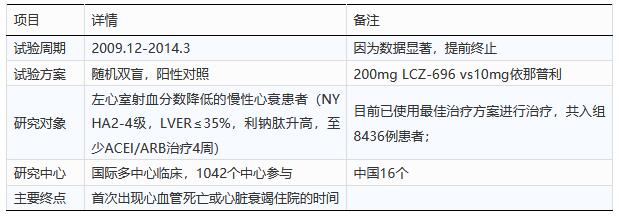
对各治疗组随访27个月,发现LCZ696与标准护理ACE抑制剂依那普利治疗组相比,从治疗早期便表现出了可持续的治疗利益:
(1)心血管疾病死亡风险降低20%(p=0.00004);
(2)心脏衰竭住院率降低21%(p=0.00004);
(3)全因死亡风险降低16%(p=0.0005);
(4)总体而言,综合衡量心血管死亡或心脏衰竭住院主要终点,风险降低20%(p=0.0000002)。
基于强劲的中期试验数据,数据监测委员会建议提前结束试验,诺华提前5个月于2014.3.28终止心衰药物LCZ696III期试验。
表4 LCZ696 Ⅲ期PARADIGM-HF临床试验结果
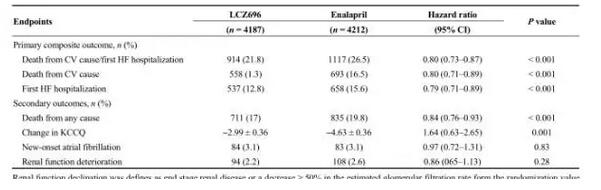
虽然PARADIGM-HF研究的目标患者为射血分数降低的人群,这类患者的心肌不能有效地收缩,为了进一步证明药物的安全有效性和扩大使用人群,诺华也在计划开展其他的临床试验,包括一项用于射血分数有保留的小规模患者人群,这类患者的心室在需要时不能松弛。
表5 LCZ696的其他临床试验
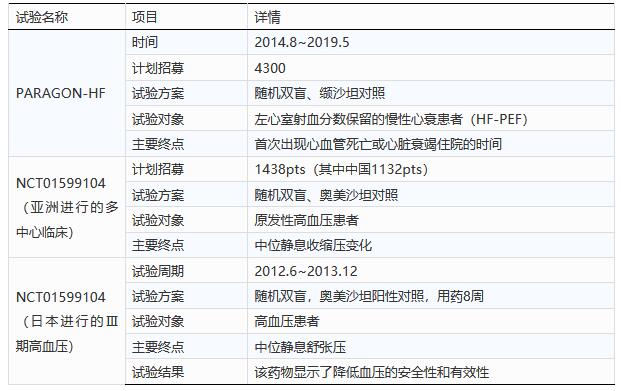
药物的安全性
LCZ696显示出比常规药物的更高安全性,治疗患者除了较少肾损伤、肾功能不全、高钾及咳嗽等常规不良反应,低血压及非严重性肿胀的副作用更低。
综上所述,LCZ696显著降低心血管死亡或心衰住院风险,疗效和安全性超越临床标准药物依那普利(enalapril),使该药成为过去10年中心脏病学领域取得的最重要的进展之一,同时在未来数年,心血管领域将无任何药物能与LCZ696抗衡。
一些分析师预测,LCZ696销售峰值高达80亿美元,鉴于LCZ696降低心血管关键风险的优越表现,德意志银行分析师预计该药的销售峰值将达到60亿美元。尽管各方数据稍有差异,但毫无疑问的是,LCZ696将成为超级重磅明星,引领心血管治疗大跨步进入新的时代。
上市销售,差强人意
尽管LCZ696的安全有效性数据非常显著,并且获得了美国心脏病学会(ACC)、美国心脏协会(AHA)和美国心衰学会以及欧洲心脏病学会(ESC)联合发布的心力衰竭新指南的I类推荐,但是上市销售业绩离预期存在较大差距。
据统计,2015年销售额为2100万美金,其中第四季销售额为500万美金;2016年上半年销售额为4900万美金,季销售收入1700万美元,未达到预期的2000~3000万美元,第二季销售额为3200万美金,第三季度继续增长,销售额为5300万美金。销售额达不到预期的原因主要有:
1. 药物定价过高,美国每日费用为$12.5,欧盟每日费用为€5-5.5,差不多年费用为$4560,缬沙坦药物每年费用为$48;
2. 心脏医生依旧使用传统老药(依那普利),诺华针对处方医生的营销尚未全面展开;
3. 药物纳入医保目录的时间比较晚,并且药物报销比例低。
尽管销售启动较慢,未达到预期,伴随着新一轮有力促销、药物进入医药目录及广告攻势,诺华和医药分析师还是对Entresto基于厚望,Clarivate Analytics(原汤森路透知识产权与科技)给出2020年销售达30亿美元的预测。诺华也宣布在50个国家开展40个临床试验计划,同时将探索新的定价和支付方式。分析师仍然认为药物的销售峰值为50亿美金。
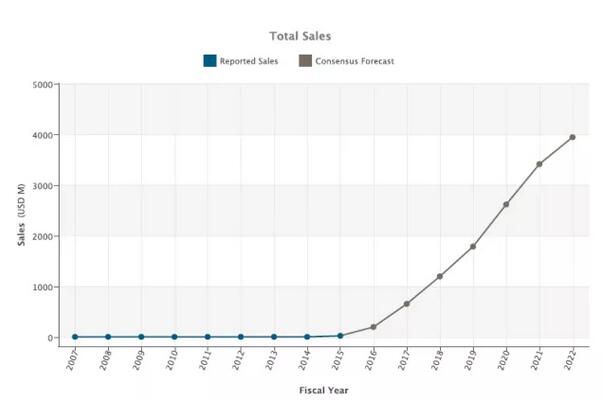
图4 LCZ696销售预计
竞争激烈,成仿制热点
Entresto在中国专利CN101098689B/CN102702119A,诺华已在国内获得临床批件,但还未获批上市,而以吉林四环制药、正大天晴药业、连云港润众制药为代表的一大波中国制药企业,经3.1/3.2注册分类,已经迅速申报沙库比曲缬沙坦,目前也在上市审评阶段。
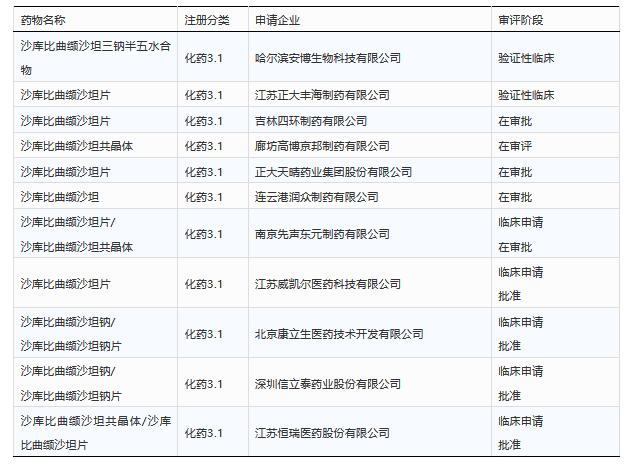
表6 国内制药企业申报沙库比曲缬沙坦情况
思考
LCZ696的上市之路说明在新靶点新机制为主的研制思路中,组合及老药新用依然有可能填补临床空白,但前期开发省下的时间和资源要舍得在临床试验的时候砸下去,也要有对疾病深刻理解。而心衰用药的门槛比较高,所以临床资源强大的药企才能玩得得心应手。
