概述【1】
二甲基汞(DMeHg)被认为是毒性最强的汞化合物之一,因其具有很强的生物累积性和生物放大效应,对人体健康构成了严重的威胁.DMeHg具有很强的挥发性,能以气态形式存在于空气中.水生环境是DMeHg产生的主要场所之一,生物(微生物如硫酸盐还原菌和铁还原菌等)甲基化过程和非生物(甲基供体如甲基钴胺素、碘甲烷和甲基硒化合物等)甲基化过程会产生大量的挥发性DMeHg.DMeHg 见光易分解,是空气中甲基汞(MeHg)的主要来源。且 DMeHg 标准样品浓度较高,微量的二甲基汞即可致死。
性质【3】
剧毒的二甲基汞(DMM)在农业土壤的水溶液中除向气相中挥发外,同时还向一甲基汞(MM)及其它难挥发的汞形态进行转化,并且挥发与转化量随土壤的特性及时间的不同而变化,土一水一气体系中,DMM在紫外光照射下,能够向Hg°转化。
来源【1】
1.在海洋表层检测到大量的DMeHg,海水中的DMeHg一部分可以被光降解、热解和生物吸收,另一部分则可以挥发到大气.
2.在垃圾填埋场及其下风向,检测到的DMeHg浓度是已报道的空气DMeHg背景值的3—4倍,且某些垃圾填埋场的DMeHg浓度是背景空气中总气态汞浓度的1倍多.
3.此外,在红树林沉积物、泛滥平原的土壤、背景空气及城市地区,均检测到了DMeHg.
制备方法【2】
1.系统包括三部分,即气态二甲基汞发生系统、吹脱系统和分析系统.气态DMeHg发生系统主要由低温恒温槽及硼硅玻璃起泡器组成.将一定质量浓度比的甲基钴胺素和汞的标准溶液置于起泡器内,利用H2SO4和NaOH将反应溶液的pH值调至4,并利用NaCl将盐度调为0—0.01mol?L-1,通过低温恒温槽控制二甲基汞的发生温度.吹脱系统由高纯氮气瓶、气体流量计及金管构成.其原理是通过恒温槽控制起泡器里气态二甲基汞的反应温度,利用高纯氮气(经金管净化,以去除痕量的Hg0;流速为20mL?min-1)将瞬时产生的二甲基汞全部吹脱出来并富集在BE捕集管上.二甲基汞分析系统由载气、解析装置、气相色谱仪和冷原子荧光测汞仪构成.吸附二甲基汞的BE捕集管经解析装置245℃解析后由气相色谱仪(色谱柱型号:MERXGC06514)和冷原子荧光检测器(型号:MERX手动烷基汞冷原子荧光检测器)分析.
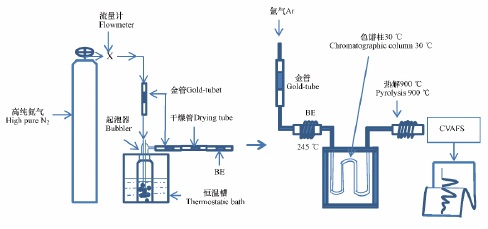
图1为稳定气态二甲基汞发生及分析装置示意图 (BE: 二甲基汞吸附管; CVAFS: 冷原子荧光检测器)
2.DMeHg的分析条件:DMeHg的分析原理与MeHg一致,即先在245℃解析,再由气相色谱-冷原子荧光检测器(GC-CVAFS)检测.与MeHg不同的是在42℃的色谱柱温及35mL?min-1的载气流速下,DMeHg与Hg0不能得到很好的分离.经多次试验,最终确定DMeHg与Hg0的分离条件是:色谱柱柱温为30℃,载气流速为13mL?min-1,具体色谱图如图2,其中峰1为Hg0、峰2为DMeHg.
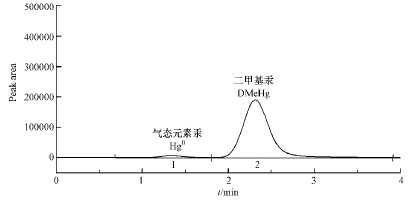
图2为分析谱图
3.DMeHg的定量:由于高浓度DMeHg的剧毒性及规避实验过程可能对操作者的伤害,利用MeHg标准溶液定量DMeHg.其原理是:BE捕集管对MeHg和DMeHg的捕集效率一致且均接近100%,且MeHg和DMeHg经GC分离后均热解为Hg0,然后由CVAFS检测.因此,利用MeHg标准溶液来定量DMeHg是安全可靠的.MeHg首先乙基化、预富集,然后由GC-CVAFS检测,测定方法参照标准方法EPA1630.
MeHg与DMeHg的热解方程式如下:
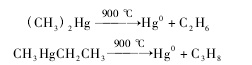
图3为MeHg与DMeHg的热解方程式
4.DMeHg的发生条件:甲基钴胺素(MeCo),维生素B12的甲基化形式,是微生物活动的一种产物,也是环境中的一种甲基供体.MeCo能为Hg(Ⅱ)提供甲基,将Hg(Ⅱ)甲基化为MeHg和DMeHg9,是很好的甲基供体.反应方程式为:
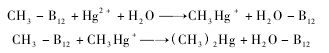
图4为DMeHg产生的反应方程式
生产方法
由甲基溴化镁或甲基锂与氯化汞在四氢呋喃或乙醚中反应制得。
测定方法【2】
银、金吸收耸串联测定二甲甚汞:将银、金吸收管串联后接于大气采样机上,以0.2一0.3升/分的流速抽气,并注人1微升二甲基汞蒸气,通过银吸收管再进人金吸收管,然后分别测定银、金管中二甲基汞的量。
结果见表1.
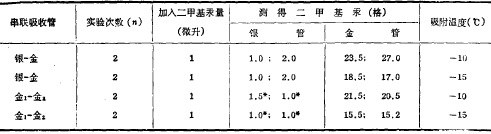
表1为银、金串联管测定二甲基汞
从表1可明显看出,银吸收管不吸附二甲基汞,表中银吸收管及第二支金管测得值认为是实验室本底,因而在银一金串联时,二甲基汞穿过银管后,全部被金管吸收,利用此串联管可有效地分离大气中的元素汞和二甲基汞。
本方法以镀金湖砂为吸附剂,以收集大气中挥发态总汞,或与银丝吸收管串联,可分别测定大气中总汞和二甲基汞。方法简便、快速,相对标准偏差为6%,最低检出限为0.5ng,线性范围0-50ng,可用于洁净空气本底值及污染区大气中汞的状态分析.
用途
用于制备三甲基镓。
主要参考资料
[1]孙婷,王章玮,陈剑,张晓山.气态二甲基汞的发生系统与产生速率[J].环境化学,2016,35(09):1792-1798.
[2]庞叔薇,邱光葵,徐良才.选择性吸收管及冷原子吸收技术快速测定大气中总汞及二甲基汞[J].分析化学,1984(07):564-568.
[3]袁兰.二甲基汞在土-水-气体系中迁移及转化规律的研究[J].农业环境科学学报,1992(04):152-155+192.
