背景及概述
手性有机膦配体参与的金属催化反应在不对称合成领域得到了广泛应用。 三配位的三价有机膦化合物可以与过渡金属形成配合物,这主要由于膦原子上的孤对电子能够与金属原子的空 d 轨道形成 σ 配位键,而过渡金属中非键合的 d π 电子又反馈给膦原子的空 3d π 轨道,这使得 σ 和 π 得到相互加强。 该类金属络合物在应用于不对称合成中时,配体的位阻效应常常会对不对称合成产生巨大的影响,利用这种影响可以有效改善产品的光学纯度。传统的手性配体 2,2’-双(二苯基膦基)-1,1’-联萘(BINAP)在不对称氢化、羰基还原等反应已广泛应用于工业化生产中,但是该类配体与钌形成的配合物在合成手性仲醇时,其光学纯度只能达到 88%,若将配体中的苯基换成 3,5-二甲基苯基时,合成仲醇的光学纯度接近 100% 。(S)-联萘(3,5-二甲苯基)膦英文名称:(S)-(-)-2,2'-Bis[di(3,5-xylyl)phosphino]-1,1'-binaphthyl,中文别名:(S)-(-)-2,2'-双[二(3,5-二甲苯基)膦]-1,1'-联萘,CAS号:135139-00-3,分子式:C52H48P2,分子量:734.885。
制备
本文以三溴化磷为原料,与二(3,5-二甲基苯基)氧化膦反应以 92% 收率得到二(3,5-二甲基苯基)溴化膦,然后在以 Ni(dppe)Cl 2 为催化剂、锌粉为还原剂的条件下发生偶联,得到(S)-联萘(3,5-二甲苯基)膦;同时考察了催化剂、还原剂的种类、反应温度、反应时间等对反应过程的影响。 该路线采用三溴化磷制备二(3,5-二甲基苯基)溴化膦作为膦给予体,克服了传统合成方法的不足,反应条件更加温和,更利于工业化生产。
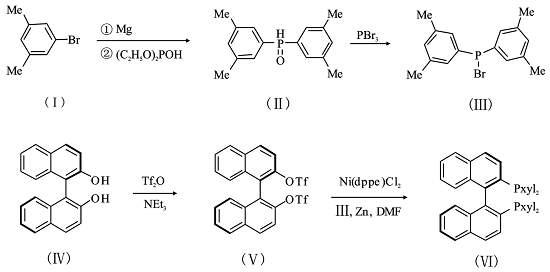
图1 (S)-联萘(3,5-二甲苯基)膦的合成路线图
实验操作:
化合物Ⅱ的合成
在氩气保护下,配有回流冷凝管、滴液漏斗、温度计的500 mL 三口瓶中,加入镁粉 12. 2 g(0. 51 mol),50 mL 无水四氢呋喃及0. 1 g碘。 在滴液漏斗中加入 3,5-二甲基溴苯90. 0 g(0. 5 mol)的四氢呋喃溶液(200 mL),滴入10 mL 四氢呋喃溶液,待引发后,再继续滴加剩余的溶液,注意滴加速度保持溶液微沸,滴加完毕后加热回流1 h,镁粉基本消失。 冰浴条件下向反应体系中滴加亚磷酸二乙酯 31. 8 g(0. 23 mol),滴加完毕后室温搅拌过夜。 小心加入 200 mL 1 mol/ L 盐酸淬灭反应。 加入200 mL 乙酸乙酯进行萃取,分出有机层。 水相再分别用 100 mL 乙酸乙酯萃取 2 次。 合并有机相,干燥、过滤,减压蒸馏除去溶剂,柱层析分离(石油醚∶ 乙酸乙酯 = 5∶ 1),得白色固体产品49. 3 g,收率 83%, 纯度 98. 2%, 熔点 82. 3 ~83. 6 ℃。
化合物Ⅲ的合成
在氩气保护下,配有冷凝管和滴液漏斗的 250 mL 三口瓶中,加入化合物Ⅱ44 g(0. 17 mol) 以及 100 mL 甲苯,滴加三溴化磷51 g(0. 19 mol),室温下反应 12 h,有大量红色沉淀生成。 氩气保护下砂芯漏斗过滤,滤饼用 50 mL 甲苯洗涤,滤液减压蒸馏除去甲苯及低沸点杂质后,收集 200 ℃ /133. 3 Pa 馏分得到淡黄色液体50. 0 g,收率 92%,纯度 97. 0%[根据 31 P NMR(167 Hz,C 6 D 6 )δ:33. 6 判断其中含有约 3% 氧化杂质二(3,5-二甲基苯基)膦酰溴]。
化合物Ⅴ的合成
在氩气保护下,配有冷凝管和滴液漏斗的250 mL 三口瓶中,加入化合物Ⅳ28. 6 g(0. 1 mol)以及 100 mL 二氯甲烷。 然后在-78 ℃下滴加三乙胺 25. 3 g(0. 25 mol),待滴完后继续滴加三氟甲磺酸酐 64. 9 g(0. 23 mol),滴完后室温反应12 h。 小心加入100 mL 1 mol/ L 盐酸淬灭反应,分液。 有机层用无水硫酸镁干燥。 过滤后减压蒸馏除去溶剂,柱层析分离(石油醚∶ 二氯甲烷 =1∶ 1) 得白色固体产品 52. 3 g,收率 95%,纯度98. 5%,熔点 74 ~75 ℃。
化合物Ⅵ的合成
在氩气保护下,配有滴液漏斗的 250 mL 三口瓶中,加入化合物Ⅴ33. 0 g(0. 06 mol),Ni(dppe)Cl 2 3. 2 g(0. 006 mol),锌粉10. 0 g(0. 15 mol)以及 100 mL N,N-二甲基甲酰胺,缓慢滴加化合物Ⅲ 42. 0 g(0. 13 mol)的 N,N-二甲基甲酰胺溶液(20 mL),滴加完毕后,100 ℃ 反应20 h。 加入 100 mL 甲醇,有沉淀生成,抽滤。 滤饼用二氯甲烷与甲醇重结晶,得到白色固体产品29. 5 g,收率 67%,纯度 98. 1%。
结果与讨论
溶剂对二(3,5-二甲基苯基) 溴化膦收率的影响
在Ⅱ与三溴化磷的反应中,由于目标产品Ⅲ对水和氧气敏感;另外,生成的亚磷酸类副产物若前期去除不彻底,后续蒸馏时对Ⅲ的收率会产生影响,选择合适反应溶剂至关重要。 在 n(Ⅱ) ∶ n(三溴化磷) = 1∶ 1. 1 的条件下,考察反应溶剂对二(3,5-二甲基苯基)溴化膦收率的影响, 以甲苯作为溶剂时,收率最高,达到 92%。 因此,选择甲苯作为反应溶剂。
三溴化磷用量对二(3,5-二甲基苯基)溴化膦收率的影响
在Ⅱ与三溴化磷的反应中,三溴化磷用量对Ⅲ收率影响较大,这主要是由于当三溴化磷用量不足时,生成的Ⅲ能够与Ⅱ发生反应,生成Ph 2 PPPh 2 ·HBr 和 Ph 2 P(O)OH。 在甲苯为反应溶剂时,考察三溴化磷用量对二(3,5-二甲基苯基)溴化膦收率的影响, 当 n(Ⅱ)∶ n(三溴化磷) = 1∶ 0. 5时,几乎没有二(3,5-二甲基苯基)溴化膦的生成,随着三溴化磷用量的增加,Ⅲ的收率逐渐增加,当n(Ⅱ)∶ n(三溴化磷) = 1∶ 1. 1 时,Ⅲ的收率达到值,因此,三溴化磷的用量为 1∶ 1. 1。
结论
以三溴化磷为原料,与二(3,5-二甲基苯基)氧化膦反应,以 92%收率得到二(3,5-二甲基苯基)溴化膦,然后在 Ni(dppe)Cl 2 为催化剂、锌粉为还原剂的条件下与(R)-( - )-1,1’-联-2-萘酚二(三氟甲磺酸酯)偶联,得到(R)-( + )-2,2’-双[二(3,5-二甲苯基)膦]-1,1’-联萘。 该路线采用三溴化磷制备二(3,5-二甲基苯基)溴化膦作为膦给予体,提高了该反应的收率,更利于工业化生产。
参考文献
[1] 陈辉,张银龙,杨振强,等. 手性2,2’-双二苯基膦基-1,1’-联萘的合成[J]. 精细化工,2015,35:1437-1440.
