氧化锰
| 中文名称 | 氧化锰 |
|---|---|
| 中文同义词 | 氧化锰;辉锰;黑锰矿;四氧化三锰;黑锰矿,辉锰,氧化锰;活性氧化锰;四氧化三锰 1KG;纳米四氧化三锰 |
| 英文名称 | Trimanganese tetraoxide |
| 英文同义词 | Manganese(II,III);Manganeseoxidebrownpowder;manganomanganic oxide (saline oxide);MANGANESE(II, III) OXIDE 97%;MANGANESE (II,III) OXIDE, 99.5% 0.6-1.2 UM;MANGANESE (II,III) OXIDE, 97+% MN 70+%;Mn70%min.;MANGANESE(II,III) OXIDE (MN3O4) |
| CAS号 | 1317-35-7 |
| 分子式 | Mn3O4-2 |
| 分子量 | 228.81 |
| EINECS号 | 215-266-5 |
| 相关类别 | Ck锰盐;无机化工产品;无机盐;通用试剂;其它金属;催化和无机化学;锰;生化试剂;常规氧化物粉体-四氧化三锰;氧化物-四氧化三锰;化工;金属粉末;锰粉;化工原料;氧化物;Inorganics;Manganese;Metal and Ceramic Science;Oxides;metal oxide;无机化工原料 |
| Mol文件 | 1317-35-7.mol |
| 结构式 | 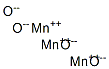 |
氧化锰 性质
| 熔点 | 1705°C |
|---|---|
| 密度 | 4.8 g/mL at 25 °C(lit.) |
| 蒸气压 | 0Pa at 25℃ |
| 溶解度 | 不溶于水;溶于HCl |
| 形态 | 粉末 |
| 颜色 | 棕色 |
| 比重 | 4.856 |
| 水溶解性 | insoluble H2O [KIR81]; soluble HCl, releasing Cl2 [MER06] |
| Merck | 13,5759 |
| 稳定性 | 稳定的。 |
| CAS 数据库 | 1317-35-7(CAS DataBase Reference) |
| EPA化学物质信息 | Manganese tetraoxide (1317-35-7) |
氧化锰又称二氧化锰,化学式为MnO2,天然品存在于软锰矿中。黑色或棕黑色晶体,有四方晶系 (又分α-体及β-体)、斜方晶系(γ- 体)、六方晶系(ε-体)。相对分子质量86.94。相 对密度5.026(β-体)。高于535℃分解释出氧气。难溶于水、弱酸、弱碱、硝酸、冷硫酸,加热情况下溶于浓盐酸而产生氯气。在热硫酸中反应,生成硫酸锰,并放出氧气。氧化锰是强氧化剂,不能与有机物或其他还原性物质如硫、硫化物、磷化物一起加热或摩擦。氧化锰为两性氧化物。在酸性介质中是强氧化剂。 γ-MnO2具有活性,可用作电池阴极材料,可消除极化作用。
 黑色的氧化锰是人类最早应用的颜料之一,距今大约17000年历史,在一些古老而遥远的洞穴岩画中还能看到它的踪迹。现代锰的开发和利用更加丰富和精细。锰矿,锰合金,锰颜料等。氧化锰常用于坯体和泥浆中,正常细度会粗些导致斑点出现,是效果也是缺点,可以预先加磨加细,增加分散性。锰氧化反应是一种重要的化学反应:
黑色的氧化锰是人类最早应用的颜料之一,距今大约17000年历史,在一些古老而遥远的洞穴岩画中还能看到它的踪迹。现代锰的开发和利用更加丰富和精细。锰矿,锰合金,锰颜料等。氧化锰常用于坯体和泥浆中,正常细度会粗些导致斑点出现,是效果也是缺点,可以预先加磨加细,增加分散性。锰氧化反应是一种重要的化学反应:
MnO3+3H2=Mn+3H2O(高温)
MnO+H2SO4=MnSO4+H2O
2MnO2+C=Mn2O3+CO(高温)
Mn2O3+H2SO4=MnSO4+MnO2+H2O
MnO2+HCI(淡盐酸)=MnC12+H2O+O2
这种反应是利用锰与淡盐酸中的氢离子反应,使淡盐酸的氢离子电荷(H+)形成氯离子(Cl-),使锰离子溶解到水溶液中,形成MnCI2溶液。氧化锰(MnO₂)是一种氧化剂,加入融熔玻璃中可以澄色剂样去除带色杂质,加入干电池有消除极化作用。将二氧化锰(MnO₂)与铝粉混合在熔炉中点燃可以制得纯锰。二氧化锰可用于制造干电池、颜料、 搪瓷、釉药、催化剂;锰化合物的原料;含铁玻璃的脱绿色剂;紫色玻璃的原料;锰钢的添加剂;漂白粉原料;肥料、涂料及染料原料。硫酸锰法将菱锰矿粉与硫酸按质量比值l:1.8~1:2.0混合进行反应,生成硫酸锰,正常情况下使用电解槽的循环酸,并补充部分硫酸,待Ph4时,加入少量二氧化锰粉,将溶液中Fe2+氧化成Fe3+,再加石灰乳中和至Ph近中性,加人硫化钡饱和溶液,使重金属离子生成硫化物沉淀,经过滤配制成电解液组成:MnSO4120±20 g/L、H7SO430±10 g/L,在温度93±5℃,槽电压2~3 V下,通常经20~30天电解,在阳极上沉积生成块状粗品,粗品经剥离、粉碎、用水多次漂洗,并加入碳酸氢钠中和至Ph 5~7,再经过滤、干燥、粉碎,制得电解二氧化锰产品。其
MnCO3+H2SO4→MnSO4+H2O+C02↑
2FeSO4+MnO2+2H2SO4→Fe2(SO4)3+MnSO4+2H2O
Fe2(SO4)3+6H2O→3H2SO4+2Fe(OH)3↓
MnSO4+2H2O[电解]→MnO2+H2SO4+H2
氯化锰法将菱锰矿与过量盐酸进行反应,生成氯化锰溶液,待反应完成后,加入石灰进行中和,控制Ph4左右,加入氧化剂过氧化氢使Fe2+氧化生成氢氧化铁沉淀而除去,净化的氯化锰溶液加入硝酸锰配成电解液,使氯化锰浓度0.5~2.0 mol/L,HCl的浓度0.01~1.0 mol/L。电解液中可加入含量10%~15%的硝酸锰,在温度85~95℃下电解,这样可解决电解过程中微量氯放出反应所造成的空气污染及腐蚀问题。电解得到纤维状二氧化锰,再经粗品剥离、粉碎、中和漂洗、过滤、干燥、粉碎,制得电解二氧化锰产品。其
MnCO3+2HCl→MnCl2+H20+CO2↑
Mncl2+2H2O[电解]→MnO2+2HCl+H2↑
 黑色的氧化锰是人类最早应用的颜料之一,距今大约17000年历史,在一些古老而遥远的洞穴岩画中还能看到它的踪迹。现代锰的开发和利用更加丰富和精细。锰矿,锰合金,锰颜料等。氧化锰常用于坯体和泥浆中,正常细度会粗些导致斑点出现,是效果也是缺点,可以预先加磨加细,增加分散性。锰氧化反应是一种重要的化学反应:
黑色的氧化锰是人类最早应用的颜料之一,距今大约17000年历史,在一些古老而遥远的洞穴岩画中还能看到它的踪迹。现代锰的开发和利用更加丰富和精细。锰矿,锰合金,锰颜料等。氧化锰常用于坯体和泥浆中,正常细度会粗些导致斑点出现,是效果也是缺点,可以预先加磨加细,增加分散性。锰氧化反应是一种重要的化学反应:MnO3+3H2=Mn+3H2O(高温)
MnO+H2SO4=MnSO4+H2O
2MnO2+C=Mn2O3+CO(高温)
Mn2O3+H2SO4=MnSO4+MnO2+H2O
MnO2+HCI(淡盐酸)=MnC12+H2O+O2
这种反应是利用锰与淡盐酸中的氢离子反应,使淡盐酸的氢离子电荷(H+)形成氯离子(Cl-),使锰离子溶解到水溶液中,形成MnCI2溶液。氧化锰(MnO₂)是一种氧化剂,加入融熔玻璃中可以澄色剂样去除带色杂质,加入干电池有消除极化作用。将二氧化锰(MnO₂)与铝粉混合在熔炉中点燃可以制得纯锰。二氧化锰可用于制造干电池、颜料、 搪瓷、釉药、催化剂;锰化合物的原料;含铁玻璃的脱绿色剂;紫色玻璃的原料;锰钢的添加剂;漂白粉原料;肥料、涂料及染料原料。硫酸锰法将菱锰矿粉与硫酸按质量比值l:1.8~1:2.0混合进行反应,生成硫酸锰,正常情况下使用电解槽的循环酸,并补充部分硫酸,待Ph4时,加入少量二氧化锰粉,将溶液中Fe2+氧化成Fe3+,再加石灰乳中和至Ph近中性,加人硫化钡饱和溶液,使重金属离子生成硫化物沉淀,经过滤配制成电解液组成:MnSO4120±20 g/L、H7SO430±10 g/L,在温度93±5℃,槽电压2~3 V下,通常经20~30天电解,在阳极上沉积生成块状粗品,粗品经剥离、粉碎、用水多次漂洗,并加入碳酸氢钠中和至Ph 5~7,再经过滤、干燥、粉碎,制得电解二氧化锰产品。其
MnCO3+H2SO4→MnSO4+H2O+C02↑
2FeSO4+MnO2+2H2SO4→Fe2(SO4)3+MnSO4+2H2O
Fe2(SO4)3+6H2O→3H2SO4+2Fe(OH)3↓
MnSO4+2H2O[电解]→MnO2+H2SO4+H2
氯化锰法将菱锰矿与过量盐酸进行反应,生成氯化锰溶液,待反应完成后,加入石灰进行中和,控制Ph4左右,加入氧化剂过氧化氢使Fe2+氧化生成氢氧化铁沉淀而除去,净化的氯化锰溶液加入硝酸锰配成电解液,使氯化锰浓度0.5~2.0 mol/L,HCl的浓度0.01~1.0 mol/L。电解液中可加入含量10%~15%的硝酸锰,在温度85~95℃下电解,这样可解决电解过程中微量氯放出反应所造成的空气污染及腐蚀问题。电解得到纤维状二氧化锰,再经粗品剥离、粉碎、中和漂洗、过滤、干燥、粉碎,制得电解二氧化锰产品。其
MnCO3+2HCl→MnCl2+H20+CO2↑
Mncl2+2H2O[电解]→MnO2+2HCl+H2↑
安全信息
| 提供商 | 语言 |
|---|---|
|
中文
|
|
|
英文
|
| 更新日期 | 产品编号 | 产品名称 | CAS号 | 包装 | 价格 |
|---|---|---|---|---|---|
| 2024/01/16 | 20026480 | 四氧化三锰 manganese(ⅱ,ⅲ) oxide;trimanganese tetraoxide | 1317-35-7 | 10G | 191元 |
