139110-80-8
中文名称
扎那米韦(抗流感药)
英文名称
ZANAMIVIR HYDRATE
CAS
139110-80-8
分子式
C12H20N4O7
分子量
332.31
MOL 文件
139110-80-8.mol
更新日期
2026/05/26 12:19:05
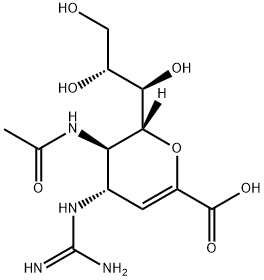 139110-80-8 结构式
139110-80-8 结构式
基本信息
中文别名
扎那米韦扎那米韦系列
扎那米韦溶液
扎那米韦一水合物
扎那米韦(标准品)
扎那米韦(抗流感药)
扎那米韦溶液, 100PPM
(2R,3R,4S)-3-乙酰氨基-4-(氨基亚氨基甲基氨基)-2-[(1R,2R)-1,2,3-三羟基丙基]-3,4-二氢-2H-吡喃-6-羧酸
扎那米韦/(2R,3R,4S)-3-乙酰氨基-4-(氨基亚氨基甲基氨基)-2-[(1R,2R)-1,2,3-三羟基丙基]-3,4-二氢-2H-吡喃-6-羧酸
英文别名
GANAGG 167
Relenza
Zanamir
Zanamivir
Hsdb 7437
GR 121167X
Unii-L6o3xi777i
GANA (inhibitor)
ZANAMIVIR HYDRATE
所属类别
原料药:其它抗生素类药物理化学性质
熔点2560C (dec.)
比旋光度D20 +40.9° (c = 0.9 in water)
密度1.75±0.1 g/cm3(Predicted)
储存条件-20°C冷冻
储存条件2-8°C
溶解度在水中的溶解度为10mg/mL,澄清
酸度系数(pKa)3.82±0.70(Predicted)
形态粉末
颜色白色至米色
旋光度 (Optical Rotation)[α]/D +30 to +40°, c = 1 in H2O
水溶解性Soluble to 5 mM in water
稳定性吸湿性
InChIKeyARAIBEBZBOPLMB-UFGQHTETSA-N
SMILES[C@H]1(NC(=O)C)[C@@]([C@H](O)[C@H](O)CO)([H])OC(C(=O)O)=C[C@@H]1NC(N)=N
CAS 数据库139110-80-8
安全数据
常见问题列表
抗流感病毒药
扎那米韦是由澳大利亚Biota公司研发的一种抗流感病毒药,1999年在英国上市销售,商品名Relenza,扎那米韦是神经氨酸酶抑制剂,通过抑制流感病毒的神经氨酸酶,从而改变流感病毒在感染细胞内的聚集和释放。神经氨酸酶是呼吸道病毒复制的关键酶,能够使唾液酸和细胞表面蛋白之间的化学键断裂,从而使新生成的病毒粒子与已感染细胞分离,进而感染附近正常细胞。抑制神经氨酸酶可以防止病毒向呼吸道其他细胞扩散。本品可用于治疗和预防流感病毒在呼吸道的扩散, 且在症状开始的48 h内使用很有效。本品为干粉吸入剂,吸入后分布于呼吸道,如鼻 咽,能有效抑制神经氨酸酶活性。本品口服无效。体外研究中,本品对流感病毒的抑制浓度受定量方法和病毒个体的影响较大,IC50和IC90分别在0.005~16.0μmol/L和0.05~> 100μmol/L之间。
本信息由ChemicalBook的晓楠编辑整理。
性状
无色晶体,熔点>240℃(分解)。[α]D20+41.0°(c=0.9,H2O)。药效学研究
体外结合试验表明,扎那米韦对A/Tokyo/3/67(N2)流感病毒的抑制是以慢性结合的方式进行的,其与流感病毒唾液酸酶的结合常数(Ki值)比与人唾液酸酶的Ki值高得多。由此说明,扎那米韦有高度特异性。研究人员指出,慢结合是该药物分子中胍基部分的作用,且对流感A型病毒有特异性,对B型病毒作用较弱。胍基能将A型病毒唾液酸酶活性部位的、呈结合状态的水分子逐出而产生紧密结合,达到抑制效果。扎那米韦对流感A型和B型多种病毒株(包括实验室和最近临床分离的病毒株以及对金刚烷胺、金刚乙胺耐药的病毒株)的体外活性研究结果发现,该药对所有分离的病毒均有极强活性,对实验传代病毒株中的流感A型病毒的IC50为0.004~0.014 μmol/L,对B型病毒IC50为0.005μmol/L。而金刚烷胺和金刚乙胺的IC50分别为1.1~7.3μmol/L和0.45~0.62μmol/L。扎那米韦对流感A型和B型病毒的临床分离病毒株的IC50为0.002~16μmol/L,在用药浓度为10mmol/L时尚未见其有细胞毒性。对人呼吸道上皮流感病毒B/HongKong/5/72毒株也有较强活性,24h和48h的IC90值分别为0.54μmol/L和0.25μmol/L,在浓度高达100μmol/L时未见对人呼吸道上皮细胞有毒性,而利巴韦林的浓度在10μmol/L和100 μmol/L时,对人呼吸道上皮细胞生长有明显的抑制作用,根据体外研究的数据表明,扎那米韦是迄今所发现的作用最强、酶特异性的广谱抗流感药物。但对单纯性疱疹A型和B型病毒、带状疱疹病毒、人巨细胞病毒、人鼻Ⅱ型和14型病毒以及副流感Ⅱ型和Ⅲ型病毒均无作用。在体内实验中,用动物模型研究了扎那 米韦的抗病毒活性。该药对流感A型病毒中的A/Singapore/1/57 (H1N1) 和 A/ Mississippi/1/85(H3N2)两个病毒株的抑制活 性比金刚烷胺强100倍;比神经氨-5-乙酰-2- 烯强300倍;比利巴韦林强1200倍。并能明 显降低小鼠肺中病毒的滴度和受感染小鼠的 死亡率,且未见病毒复燃。
药动学研究
采用经口给药、鼻内给药、皮内或静脉注射给药等多种途径研究了扎那米韦在小鼠体内的药动学。实验结果表明,除口服给药外,其他途径给药均有较好的生物 利用度。静注的消除半衰期为10 min。经口、皮内和鼻内给药的尿液排泄率分别为3%、68%和43%。在人体药动学研究中,分别进行了不同剂量下单剂量静脉注射给药和多剂量给药的药动学实验。静注扎那米韦后,体内消除迅速,消除半衰期为1.6 h,多以原形经尿液排泄,尿中原药量为给药量的87%;体内分布仅限于细胞外液,Vdss为16L。经鼻给药后,尿中原药排泄量比静注给药少得多,为4%~10%,血浆半衰期为3.4h,生物利用度为10%~25%;吸入给药的半衰期为2.9h。在 剂量为16mg时,每日4次,连续7d多剂给药,药动学线性未见改变。本品经口服吸入给药后,约有4%~17%被吸收,血清半衰期为2.5~5h,血浆蛋白结合率小于10%,药物在人体内不发生代谢,以原形经肾排出,未吸收药物通过粪便排泄。
临床应用
可用于成年病人和12岁以上的青少年病人,治疗由A型和B型流感病毒引起的流感。成年病人和12岁以上的青少年病人,每日2次,间隔约12h。每次10mg,分两次吸入,一次5mg。连用5d。随后数日2次的服药时间应尽可能保持一致,剂量间隔12h(如早晨或傍晚)。不良反应
本品不良反应发生率为 1.5%,常见为鼻腔症状,其他还可发生头痛、 胃肠道反应(腹泻、恶心、呕吐)、支气管炎、咳 嗽、窦炎、耳鼻喉感染和眩晕。少数可发生不适,虚弱,发烧,腹痛,肌痛,关节痛和荨麻疹。 动物试验显示本品无致畸或致癌作用,对生殖系统也无影响。注意事项
对哮喘或慢性阻塞性肺疾病病人治疗无效,甚至可能引起危险。引起支气管痉挛的病人应停药并通知其主治医生。FDA建议如果病人出现过敏反应的症状和体征,应停止用药。专利
WO9116320;US 5360817