背景及概述[1-2]
甲基乙二醛化学式CH3COCHO。分子量72.06。黄色流动液体。有辛辣气味、吸湿性。沸点72℃,相对密度1.045524,折光率1.400217.5。溶于水,溶于醚和苯呈黄色,溶于醇为无色。极易聚合为黏稠性半固体,溶于水,放出热量,又恢复为单体溶液。加热形成黄绿色气体,在封闭管中能维持数天。商品一般为20%~40%水溶液。对石蕊试纸略显酸性。甲基乙二醛是人体内正常的代谢产物,可由碳水化合物、脂质及蛋白质代谢产生,正常生理情况下它在人体内的合成量极低,而在高血糖状态下如糖尿病患者体内会显著增高,甲基乙二醛是一种高活性化合物并具有细胞毒性。早在1958年,人们发现丙酮醛不仅具有抗疟疾、抗病毒的作用而且有抗肿瘤的效应,随后人们从体外、体内实验以及临床患论证了甲基乙二醛的抗肿瘤作用。
抗肿瘤机制[2]
甲基乙二醛具有极高的活性,能够与蛋白质、核酸等生物大分子反应并对其修饰,从而导致细胞功能改变。研究表明,甲基乙二醛具有多种细胞毒性作用,如抑制细胞生长、诱导细胞凋亡、抑制酶的活性以及激活信号通路等。甲基乙二醛在多种类型肿瘤组织中的含量比正常组织中低,在干扰乙二醛酶或者加入乙二醛酶抑制后可出现明显的肿瘤抑制作用,而这一抑制作用是通过升高甲基乙二醛浓度实现的。甲基乙二醛可通过抑制增殖、诱导凋亡、抑制肿瘤转移以及增强机体的免疫力和提高对现有抗肿瘤药物的敏感性等方面发挥抗肿瘤效应。
1. 抑制增殖
早在19世纪60年代,甲基乙二醛就被认为是天然的生长调节因子,是一种抑素,能够阻止细胞分裂。甲基乙二醛能够抑制人白血病HL-60细胞的生长,并能够抑制接种了艾式腹水癌(ehrlichascitescarcinoma,EAC)细胞、白血病L4946细胞、腺癌细胞及肉瘤S180细胞等的荷瘤小鼠体内肿瘤的生长,说明丙酮醛能够抑制肿瘤细胞的增殖。研究表明,其抑制增殖的机制在于它能够抑制蛋白质的合成,丙酮醛能够修饰RNA的鸟苷酸残基导致蛋白质聚合体稳定性下降,从而阻滞蛋白质合成的起始过程。丙酮醛还能够与DNA的眯基残基端发生反应对其进行修饰,从而使DNA双链断裂、形成DNA-蛋白质交联物等抑制DNA的合成,同时甲基乙二醛也会轻微的影响RNA的合成。随后人们发现,甲基乙二醛可以通过影响代谢进而抑制肿瘤细胞的增殖,一方面,丙酮醛能够干预肿瘤细胞的糖酵解过程,研究表明,用2mmol/L和5mmol/L的甲基乙二醛作用于ECA细胞后,葡糖糖的利用分别被抑制50%和80%,乳酸生成量分别被抑制55%和90%,并发现甲基乙二醛能够极大地抑制恶性肿瘤细胞中3-磷酸甘油醛脱氢酶的活性,由于肿瘤细胞赖以生存及快速增殖的原料来自于其活跃的低氧糖酵解过程,因而甲基乙二醛能够有效并特异地抑制其增殖;另一方面,甲基乙二醛直接抑制线粒体氧化呼吸过程,主要是通过抑制线粒体复合物I参与的电子链传递导致肿瘤细胞的氧耗和ATP的生成减少从而极大地削减了能量供应。此外,甲基乙二醛还能阻止细胞由DNA合成前期(G1期)向DNA合成期(S期)转变,它首先下调前列腺癌PC3细胞周期蛋白cyclinD1的表达,继而下调细胞周期蛋白依赖性激酶2(cyclin-dependentkinase2,cdk2)和cdk4,使视网膜母细胞瘤蛋白(retinoblastomaprotein,pRB)去磷酸化最终导致G1期阻滞、生长停止。因此,甲基乙二醛能够通过抑制蛋白质、DNA合成,抑制肿瘤细胞的糖酵解和氧化磷酸化过程以及调节细胞周期等抑制肿瘤细胞的增殖。
2. 诱导凋亡
近年来人们发现,甲基乙二醛发挥抗肿瘤作用最主要的途径是通过诱导细胞凋亡,研究表明,将甲基乙二醛作用于包括前列腺癌细胞、肝癌细胞、肉瘤细胞等在内的多种恶性肿瘤细胞后,细胞的形态发生极大改变并裂解、细胞内DNA碎片增多并形成凋亡小体等。甲基乙二醛诱发凋亡的机制有以下几种。
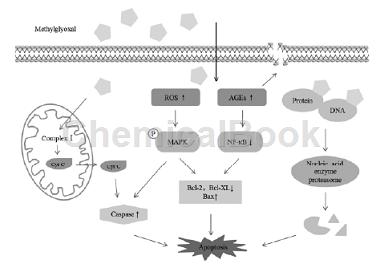
(1)甲基乙二醛能使细胞内活性氧(reactiveoxygenspecies,ROS)水平升高,甲基乙二醛在糖基化反应过程中产生的超氧化物阴离子和过氧化氢以及它对ROS清除酶类的抑制分别从增加来源与减少去路两方面提高了细胞内ROS的生成量。升高的ROS可作为上游信号分子激活分裂原激活的蛋白激酶p38(p38MAPK)、p42/44MAPK信号通路介导细胞凋亡;同时ROS的产生还能触发线粒体释放细胞色素c,进而激活细胞凋亡蛋白酶caspase-3、caspase-9,并下调DNA修复酶聚腺苷二磷酸–核糖聚合酶(PARP)进一步损伤细胞。
(2)甲基乙二醛作为强大的糖化剂能够与蛋白质等其他胞内重要成分发生糖化反应产生晚期糖化终末产物(AGEs),其中,精氨嘧啶(AP)是甲基乙二醛修饰蛋白质的精氨酸残基后主要的产物之一,它能够在激活核转录因子NF-κB(nuclearfactor-KappaB)信号通路,触发线粒体凋亡机制的同时上调凋亡蛋白Bax(Bcl-2-associatedXprotein)、下调抗凋亡蛋白Bcl-2(B-celllymphoma-2)和Bcl-XL的表达,最终导致细胞凋亡增加;AP还能通过直接破坏细胞骨架蛋白肌动蛋白actin和微管蛋白α-tubulin来促进凋亡。
(3)在对肉瘤的研究中发现,甲基乙二醛在降低线粒体复合物I活性的过程中,除了能极大地降低ATP的产生外,还能够降低线粒体跨膜电位,进而改变线粒体膜通透性,释放线粒体促凋亡因子细胞色素c,最终破坏线粒体膜的完整性并导致细胞死亡。因此,甲基乙二醛能够通过直接或间接的方式激活凋亡信号通路以及线粒体凋亡途径促进凋亡。另外,甲基乙二醛对DNA残基进行糖化修饰形成的MGDN加合物能够激活核酸内切酶类,对蛋白质进行修饰后,蛋白质的生物活性与稳定性会受到一定影响,甚至会被蛋白酶体识别而降解,这些也是丙酮醛促进凋亡的原因之一。
3. 抑制侵袭、黏附能力
肿瘤细胞的黏附、迁移以及侵袭能力是肿瘤进行转移的必备的关键因素。甲基乙二醛能够抑制肝癌Huh-7和HepG2细胞的黏附与侵袭能力,这一抑制作用是由抑癌基因p53介导的,当p53被抑制或干扰后则不存在这一抑制作用。甲基乙二醛能促进p53转运至核内增强它的转录活性,并将Y220C突变型p53恢复至野生型p53所具有的构象和活性,随着野生型p53功能的恢复肿瘤细胞的移动和侵袭受到抑制,而恢复p53功能已被推荐为抗肿瘤治疗的一种,因此甲基乙二醛能够通过p53途径抑制肝癌的转移。
4. 免疫调节
免疫调节已被认为是预防和治疗肿瘤的另一种选择,免疫系统的防御机制主要是通过主动或被动免疫激活机体免疫应答来清除肿瘤细胞,预防肿瘤转移和复发。研究表明,甲基乙二醛能够增加肉瘤180细胞小鼠模型体内巨噬细胞的数量和吞噬能力以及杀伤性T细胞的产生和杀伤作用,增强小鼠的细胞免疫以抵抗肿瘤,同时小鼠体内一些免疫调节因子和表面受体:干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、IL-6、Toll样受体-4(TLR-4)以及TLR-9也的表达出现明显的升高。甲基乙二醛主要通过调节巨噬细胞集落刺激因子促进巨噬细胞的产生,p38MAPK、NF-κB信号通路也参与其中。因此,甲基乙二醛在增强巨噬细胞和淋巴细胞的活性以及通过免疫调节抵抗肿瘤过程中发挥着重要的作用。
5. 提高化疗药物敏感性
乙二醛酶I的高表达会引起多柔比星、依托泊苷、丝裂霉素C及其他化疗药物的多重耐药。研究发现,许多对现有的临床化疗药物多重耐药的人类肿瘤细胞系中乙二醛酶I的mRNA水平普遍较高,上调非多重耐药的肿瘤细胞内乙二醛酶I的表达量后该细胞也会出现多重耐药现象。乙二醛酶I高表达引起化疗药物的多重耐药的具体机制现在尚不清楚,但可以肯定的是与甲基乙二醛密切相关,将乙二醛酶I抑制剂对溴苯甲基谷胱甘肽环戊二酯作用于细胞后,细胞内甲基乙二醛含量明显升高,且细胞重新获得对抗肿瘤药物的敏感性。另外,有文献报道,甲基乙二醛能够通过激活蛋白激酶C(proteinkinaseC,PKC)的δ亚基来增强顺铂对骨髓瘤细胞的杀伤作用,联合丙酮醛可将顺铂的抗肿瘤效应放大约4倍。
分解[2]
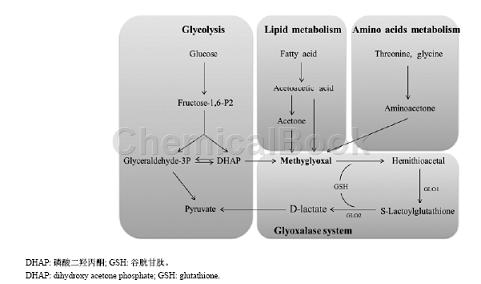
甲基乙二醛的分解代谢有乙二醛酶、醛糖还原酶、醛脱氢酶以及羰基还原酶途径等,最主要的分解途径是乙二醛酶系统。乙二醛酶系统包括乙二醛酶I和乙二醛酶II,还原型谷胱甘肽为辅助因子。丙酮醛能够与还原型谷胱甘肽经非酶促反应自发形成缩醛,它能与乙二醛酶I(glyoxalaseI,GLO1)的两个活性位点结合,在乙二醛酶I催化作用下转化成S-D-乳酸谷胱甘肽。继而在乙二醛II(glyoxalaseII,GLO2)的作用下,S-D-乳酸谷胱甘肽被水解成D-乳酸,同时重新生成还原型谷胱甘肽并进入乙二醛酶I催化的步反应中被循环利用。D-乳酸能够在线粒体中被2-羟基酸脱氢酶代谢合成丙酮酸。乙二醛酶I是甲基乙二醛分解过程中的关键酶,它的活性程度会直接影响甲基乙二醛浓度的高低。
制备[3]
方法1:在500mL四颈瓶中加入160mL水、50mL丙酮、37.2mL冰醋酸及4.0g氯酸钾,安装好机械搅拌器、温度计、回流冷凝管和长颈滴液漏斗。开动机械搅拌,将水浴温度控制在60~75℃、瓶内温度在60℃左右,用滴液漏斗滴加35.4mL溴,控制滴加速度,不使未反应的溴累积。加溴毕,继续反应0.5h,待溶液颜色褪去后加入80mL冰水稀释反应液,并冷却至10℃,然后加入100g无水碳酸钠至刚果红中性。分出油层,用8g无水氯化钙干燥,减压蒸馏,收集40~42℃/1733Pa的馏分,产率达63.5%(文献为50%~51%)。将收集的馏分与DMSO按适当的配料比加入到250mL的三颈瓶中,通入空气,控制在适宜温度下,电磁搅拌,回流反应8h。反应毕,常压分馏,收集71.5~73.0℃的馏分,折光率n24.6D=1.3803(文献n20D=1.4209)。
方法2:称取二水合重铬酸钾89.4g(0.3mol),用400mL水溶解,边搅拌边慢慢滴加浓硫酸63.9mL(1.2mol),搅匀,冷却后,转移到滴液漏斗中。在1000mL的三颈瓶中,先加入1,2-丙二醇32.9mL(0.45mol)和1.0g硫酸锰做催化剂,然后在中间口接蒸馏装置,一口接滴液漏斗,另一口插入带玻塞的玻璃管,玻管的下口要插入到液面以下。先从玻管向三颈瓶中导入氮气,再用带调压器的电热套给三颈瓶加热。几分钟后,由滴液漏斗滴入上述配好的溶液,约50~70min滴完。
滴完后继续加热蒸馏15min(注意关上滴液漏斗的活塞),收集约250mL黄绿色馏出液。馏出液用450mL无水乙醚分4次萃取,萃取后弃去水层,合并萃取液。用饱和碳酸氢钠水溶液洗至中性,分出水层,醚层用无水硫酸镁干燥4h。过滤,水浴45~50℃蒸去乙醚,然后沸水浴分馏,收集71~73℃的馏分,得到黄绿色带有特殊臭味的液体,产率49%~50%。产物在0℃下通入氮气保存。经检验,该馏分能使希夫试剂显紫红色,使斐林试剂出现砖红色沉淀,与2,4-二硝基苯阱生成橘红色沉淀(在硝基苯中重结晶),测其熔点为308~309℃(文献为308~309℃)。经纯化,微量法测得丙酮醛的沸点为72℃(文献为72℃)。
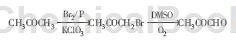
主要参考资料
[1] 化合物词典
[2] 甲基乙二醛抗肿瘤机制的研究进展
[3] 甲基乙二醛的合成研究
