【背景及概述】[1][2][3]
维生素C又称抗坏血酸(asco-bic acid),首先于1928年由匈牙利的Szent-Gyorgyi分离得到的,并于1933年由Hirst和Haworth测定了其结构,TadeusReichstein发明了维生素C的人工合成方法并合成成功。维生素C的分子式是C6H8O6,是一种强还原剂,分子中2位及3位碳原子的两个烯醇式羟基易解离而释放H+,从而氧化形成脱氢维生素C。维生素C和脱氢维生素C形成了可逆的氧化还原系统,在人体内发挥着重要的作用。维生素C为白色结晶,溶于水,性质极不稳定,易受热、氧化、光、金属离子和硷破坏,在酸性溶液中较稳定。维生素C是含6个碳的多羟化合物,其中有两个烯醇式羟基,很容易离解出氢离子或释放出氢原子,故有很强的还原性。它在体内主要以还原型抗坏血酸存在,也以氧化型抗坏血酸存在,两者处于可逆平衡状态,构成氧化一还原系统,在生物氧化过程中起递氢体作用。
维生素C参加体内的氧化还原反应,可以保持巯基酶的活性和谷胱甘肽的还原状态,起到解毒的作用;参与体内多种羟化反应,可以促进胶原蛋白的合成,促进胆固醇的代谢;刺激免疫系统,可防治感染,抑制病毒的增生,阻止致癌物质的生成。抗坏血酸还有促进胶元蛋白、四氢叶酸的合成、铁的吸收以及解毒、提高机体抵抗力、改善心肌功能等作用。对提高运动员耐久力,消除运动后疲劳和治疗过度训练有一定作用。缺乏时可引起坏血病,主要症状为出血如牙龈出血、萎缩,儿童患者骨质疏松。还常出现营养不良、贫血、易感染、伤口愈合缓慢等。新鲜蔬菜水果是的来源,酸枣、山楂、西红柿、橙、桔、辣椒中含量较多。食物贮存、烹调中维生素C易受损失。供给量一般成人为每天60~70毫克,运动员训练期100~150毫克,比赛期200~250毫克。
【生理功能】[3]
维生素C 具有一系列的生理功能。概括而言,维生素C 的生理功能主要体现在以下10 个方面。
1. 增强人体免疫功能
维生素C可促进入体内抗体的形成,提高白细胞的吞噬能力,提高人体对疾病的抵抗力和对寒冷的耐受力,从而增强人体的免疫功能。
2. 预防和治疗缺铁性贫血
食物中铁存在的离子形式包括Fe2+ 和Fe3+2 种,人体能够吸收的只有Fe2+。铁是合成血红细胞的重要材料,人体缺铁可患缺铁性贫血症(IDA),又称营养性贫血。维生素C具有较强的还原性,可将食物中的Fe3+还原成Fe2+,促进食物铁在肠道内的吸收,有利于预防和治疗缺铁性贫血(IDA)。
3. 预防和治疗恶性贫血
人体缺乏叶酸(VB11)时可患恶性贫血(巨幼红细胞性贫血)。叶酸对氧较为敏感,而维生素C具有较强的还原性(抗氧化性),一方面,维生素C的存在对叶酸具有保护功效,可以减少叶酸在烹调加工过程中的损失,提高膳食中叶酸的有效供应量;另一方面,维生素C可将叶酸(F)还原成具有生物活性的四氢叶酸(FH4),促进叶酸的活化。维生素C对叶酸可发挥保护及活化等双重作用,从而有利于预防和治疗恶性贫血(巨幼红细胞性贫血)。
4. 预防和治疗坏血病
人体轻度缺乏维生素C时,早期症状表现为感觉疲劳、牙龈出血等,严重缺乏维生素C 时,则可导致坏血病。保证膳食中维生素C 的足量供应,有利于预防和治疗坏血病。
5. 促进胶原的形成和类固醇的代谢
一方面,胶原是含有大量羟脯氨酸和羟赖氨酸的纤维状蛋白质,它们分别是由脯氨酸和赖氨酸羟基化所形成的。维生素C的作用在于活化脯氨酸羟化酶和赖氨酸羟化酶,促进脯氨酸和赖氨酸向羟脯氨酸和羟赖氨酸的转化,进而促进组织细胞间质中胶原的形成。另一方面,维生索C 可参与类固醇的羟基化反应,如促进胆固醇转化为胆汁酸、皮质激素及性激素等。
6. 有利于维持骨骼和牙齿的正常功能
维生素C是一种酸性化合物,可在消化道中形成酸性介质,能防止不溶性钙络合物的生成,促进膳食钙的吸收;维生素C还可进一步促进钙在骨骼和牙齿中的沉积,有利于维持骨骼和牙齿的正常功能。
7. 有利于维持细胞膜的完整性
人体内的不饱和脂肪酸(UFA)易被氧化而生成脂性过氧化物,可使各种细胞膜破裂。还原性谷胱甘肽(G-SH)可使脂性过氧化物还原成羟基化合物,自身转变成氧化型谷胱甘肽(GS-SG),从而消除脂性过氧化物对细胞膜的破坏作用。维生素C 具有较强的还原性(抗氧化性),在谷胱甘肽还原酶的作用下,可使GS-SG还原为G - SH。
8. 对某些有毒物质具有解毒作用
铅化物、砷化物、苯、细菌毒素等是日常膳食中常见的有毒有害物质,对人体健康存在潜在危害。当致毒剂量的铅化物、砷化物、苯以及细菌毒素等进入人体内时,充足的维生素C 有利于缓解其毒性,从而降低这些有害物质对人体健康的危害程度。
9. 具有抗衰老作用
科学实验证明,自由基和过氧化脂质是人体衰老的重要诱因。充足的维生素 C 可抑制体内自由基、过氧化脂质等有害物质的形成,从而延缓人体的衰老。
10. 具有防癌抗癌作用
亚硝基化合物是食物中存在的一类重要的致癌物质,其中尤以亚硝胺的致癌性最为突出。维生素C具有较强的还原性,可阻断亚硝基化进程,抑制亚硝胺的形成,有利于预防胃癌、肠癌等消化道癌症。维生素C还可促进胶原蛋白抗体的形成,胶原蛋白可包围癌细胞,从而表现出抗癌作用。
【需求及来源】[3]
维生素C是人体膳食供应量的一种维生素。根据中国居民膳食营养素参考摄入量(DRIs),我国普通成年人的RNI(营养素参考摄入量)为100mg/d,孕妇和乳母的RNI 为130mg/d。1982 年我国的第二次全国营养调查,全国城乡居民VC 的平均摄入量约为129mg/d;1992 年我国的第三次全国营养调查,全国城乡居民VC 的平均摄入量约为100mg/d;而2002 年我国的第四次全国营养调查,全国城乡居民VC 的平均摄入量约为90mg/d,VC 的膳食摄入量呈下降趋势。—些特殊人群需要适量增加维生素C的膳食供应量,以充分满足机体对VC 的正常生理需求。VC 是老年人容易缺乏的一种维生素,老年人应注意适当增加维生素C的摄入量,营养学家建议老年人可每天额外服用200~300mg维生素C 补充剂,以增强抗衰老和提高免疫力的功效。高温环境下的工作人员,由于维生素C随汗液大量排出体外,VC 的供应量应为普通人的3~5 倍。因为维生素C 是水溶性的,短期内摄入较大剂量的维生素C,一般不会给人体带来副作用,但如果长期大剂量摄入维生素C,则不利于人体健康。有事实表明,如果长时间每天摄入维生素C 数量超过1g,则可能引起某些代谢的变化而出现副作用,例如:容易产生肾脏或尿道结石,可增加患坏血病的风险等。长期摄入大剂量维生素C还可使人体产生依赖现象,当摄入量恢复到正常剂量时就不能满足生理需要,从而出现维生素C 的不足或缺乏。
维生素C在食物中的分布表现为明显的集中性。维生素C 主要存在于水果、蔬菜等植物性食物中,动物性食物几乎不含维生素C。根据维生素C在食物中的含量状况,可将维生素C 的食物来源划分为4 个层次,即食物来源、良好食物来源、一般食物来源和稀缺食物来源。维生素C 的食物来源包括:维生素C 的宝库-刺梨,活的维生素C 丸-鲜枣,维生素C 之王-猕猴桃等。维生素C 的良好食物来源主要包括:辣椒、苦瓜、柑橘、番茄、菜花、草莓、荔枝、绿色叶菜等。维生素C 的一般食物来源主要包括:白菜、西芹、莴笋、南瓜、梨、苹果、香蕉、桃子、樱桃等。维生素C 的稀缺食物来源包括:畜禽肉、鱼、蛋、乳等动物性食物以及干大豆等几种植物性食物。
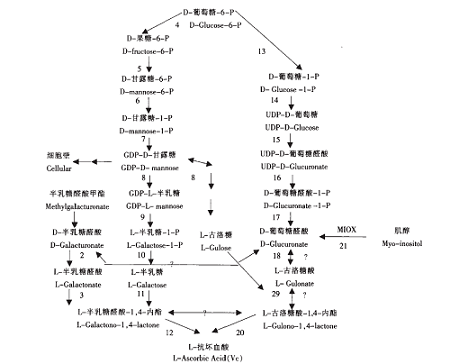
【合成】 [4]
维生素C 的生物合成途径目前仍不完全清楚,目前研究表明,半乳糖途径在植物维生素C 的生物合成中占主导地位,但不能排除其它途径的可能,尤其是已经报道的糖醛酸衍生物可转化为维生素C 的现象。迄今为止已经有4 种可能的植物维生素C 合成途径被提出即:半乳糖途径、糖醛酸途径、古洛糖途径和肌醇途径。
【临床应用】[5]
1. 维生素C和坏血病
坏血病的临床表现主要反映了维生素C在胶原蛋白合成过程中发挥的重要作用。特定的组织和毛细血管的脆弱主要是在胶原蛋白合成过程中脯氨酸羟化过程受阻,从而导致胶原蛋白无法合成。胶原蛋白归于结缔组织,是骨及毛细血管等的重要组成部分,而结缔组织是伤口愈合的步,所以胶原蛋白合成受阻就会出现毛细血管破损、瘀血、紫癜、牙龈出血、伤口愈合延迟、骨质脆弱、关节疼痛等症状,严重情况则会导致死亡。维生素C是胶原脯氨酸羟化酶的辅因子,缺少维生素C就会导致脯氨酸无法形成羟脯氨酸,影响胶原蛋白的合成。对于坏血病患者补充适量的维生素C就可以治疗坏血病。
2. 维生素C和iPSCs
iPSCs全称为induced pluripotent stem cells,即诱导性多功能干细胞,它是通过诱导机体细胞特定的基因表达,从而转变为多功能干细胞。维生素C在iPSCs的产生过程中发挥着一定的作用。研究表明,细胞培养过程中加入维生素C就可以得到高质量的iPSCs,维生素C可以增强机体细胞的重编程,增加GFP+/AP+的比率,从而形成iPSCs。细胞的重编程需要许多转录因子,如Sox2,Klf4,Oct4,c-Myc(SKOM)。
3. 维生素C与癌症
维生素C可以消除过氧化氢,防止细胞的癌变。其中维生素C对过氧化物诱发的抑制缺口衔接点细胞间交流(GJIC)有预防作用。GJIC是维持正常细胞生长所必需的,与抑制癌症发生的过程尤其是与引发肿瘤紧密相关。过氧化氢是一种肿瘤引发剂,它通过改变一种特殊蛋白质-间隙连接蛋白43来抑制GJIC,从而诱导细胞的癌变。当用维生素C处理大鼠肝脏上皮细胞时,研究人员发现过氧化氢诱发的GJIC抑制作用被制止。
4. 维生素C和SVCT
维生素C在机体内的吸收依靠钠离子依赖的维生素C转运蛋白(SVCT),SVCT1和SVCT2是该家族中研究比较清楚的两个蛋白,这两种蛋白都可以专一性的转运维生素C。维生素C的摄取过程与Na+具有协同性:每转运一个维生素C分子,就需要同时转运2个Na+。SVCT1在小肠、肝脏、肾脏等中介导维生素C的吸收,其组织特异性较为明显;而SVCT2 则分布的较为广泛,在神经元、骨骼、大脑、肾上腺等多个组织中表达并介导维生素C的吸收。许多研究表明维生素C具有一定的抗癌作用,SVCT可以保持机体内维生素C的稳态,从而为维生素C的抗癌作用提供一个间接依据。SVCT的遗传多态性与肿瘤的发生密切相关,如胃癌、直肠癌等。
【主要参考资料】
[1] 运动解剖学、运动医学大辞典.
[2] 杜冀晖. 维生素 C 在肿瘤治疗中的作用研究进展[J]. 医学综述, 2010 (4): 554-557.
[3] 曾翔云. 维生素 C 的生理功能与膳食保障[J]. 中国食物与营养, 2005 (4): 52-54.
[4] 刘永立, 胡海涛, 兰大伟. 维生素 C 的生物合成及其基因调控研究进展[J]. 果樹學報, 2006, 23(3): 431-436.
[5] 杨建辉. 维生素 C 生物学活性研究进展[J]. 现代诊断与治疗, 2012 (5).
