
胃蛋白酶是施旺于1836年发现的,十九世纪中叶科学家发现它能够将蛋白质分解成胨(peptones,属于多肽)。后来,人们发现它能够有效治疗消化道疾病,这一发现,极大地促进了胃蛋白酶的生产和纯化技术,最终在十九世纪末取得了成功。但是它的化学本质和特性一直没有搞清楚。直到1930年才由约翰诺斯罗普(John H. Northrop)提取出来(结晶),并证明了它是蛋白质。这是科学家次发现和结晶动物体内的蛋白质酶。约翰诺斯罗普也因此在1946年和其他科学家(Sumner, and Stanley )共同分享了诺贝尔化学奖。之后,新的分离技术如结晶、层析得到进一步发展。通过这些技术,胃蛋白酶和胃蛋白酶原的氨基酸排列顺序得以确定。1959年Ryle and Porter两人首次从猪的胃中分离出了胃蛋白酶B和C(多数为胃蛋白酶A),20世纪七十年代中叶随着X-衍射技术的改进胃蛋白酶的三维立体结构得以确定,使人们能够更好地理解酶促反应的本质。21世纪初,由于HIV-蛋白酶作为天冬氨酸蛋白酶系的确立,胃蛋白酶型及其抑制剂的研究再度兴起。
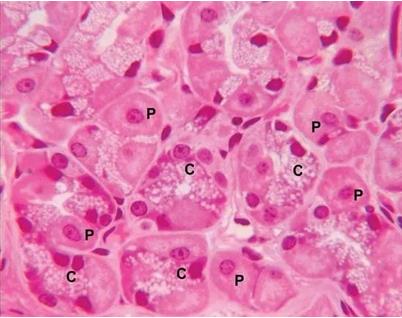
这里我们主要说一下胃蛋白酶( 理论上分子量为34.5 kDa )。当人和动物进食时,胃泌素和迷走神经会触发胃粘膜中的某些腺体细胞分泌胃蛋白酶原(分子量为41.4 kDa)和盐酸。胃蛋白酶原刚分泌出来时是没有活性的,在盐酸形成的酸性环境下,它以一种自动催化的方式(in an autocatalytic manner)伸展并断裂,迅速形成具有生物活性的胃蛋白酶。胃液的PH值在1至3范围,它不仅能够使胃蛋白酶原变成胃蛋白酶,而且可以触发更多的胃蛋白酶的形成(自动催化)。当PH值超过7时胃蛋白酶会永久性失活,也就是说小肠中PH大约为7,胃蛋白酶进入小肠后就完全失活,不能再分解蛋白质。少量的胃蛋白酶会进入血管,消化那些被小肠吸收的尚未较大的蛋白质碎片。
胃蛋白酶能够将食物中的蛋白质分解成为多肽,进而在肽酶的作用下分解成氨基酸。但胃蛋白酶是具有广泛特异性的酶,偏爱含有芳香环或羧基的L-氨基酸的肽键,也就是喜欢裂解苯丙氨酸和亮氨酸的C末端,极少裂解谷氨酸连接部位,不裂解缬氨酸、丙氨酸和甘氨酸连接部位。胃蛋白酶的活性除了受酸碱度的影响外,还受到环氧化合物、脂肪质醇类及胃酶抑素A的抑制。
商业上使用的胃蛋白酶大都来自猪的胃。原始的胃蛋白酶主要用于皮革生产过程中取出皮革表面的毛和残留组织,也可以通过分解固着银化合物的明胶(蛋白质)层从废弃的电影胶片中回收银,其他的应用还有许多,如分解抗体、化妆用胶原蛋白的制备、食品化学中蛋白质消化能力的评价及哺乳动物上皮细胞的次生培养等。
